
【题目】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为__________________________________。
利用反应6NO2+8NH3![]() 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______________ L
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是______________ L
(2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=________kJ·mol-1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________。
SO3(g)+NO(g)的ΔH=________kJ·mol-1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=__________。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH______0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________________。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH______0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________________。

【答案】 3NO2+H2O=NO+2HNO3 6.72 -41.8 b 8/3 < 此压强下,反应速率快,转化率较高,若再增大压强对设备要求高,成本高
【解析】试题解析:(1)二氧化氮与水反应生成硝酸和一氧化氮;3NO2+H20=HNO3+NO;6NO2+8NH3![]() 7N2+12 H2O也可处理NO2。该反应转移电子24摩尔e-, 生成氮气7摩尔;当转移1.2 mol电子时,消耗的NO2在标准状况下1.2×7×22.4/24=6.72L; 2)根据盖斯定律,处理两个方程式,消去氧气,得到NO2(g)+SO2(g)
7N2+12 H2O也可处理NO2。该反应转移电子24摩尔e-, 生成氮气7摩尔;当转移1.2 mol电子时,消耗的NO2在标准状况下1.2×7×22.4/24=6.72L; 2)根据盖斯定律,处理两个方程式,消去氧气,得到NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH="-41.8" kJ·mol、1。达到平衡状态:a.反应前后为体积不变的反应,所以反应体系压强任何时候都保持不变;错误;b.混合气体颜色保持不变,即二氧化氮气体的浓度不变,达平衡状态;正确;c.SO3和NO为生成物,任何时候体积比都保持不变,无法确定;错误;d.每消耗1 mol SO3为逆反应速率,同时生成1 mol NO2为逆反应速率,方向相同,无法判断;错误;答案为b;测得上述反应平衡时NO2与SO2体积比为1︰6,
SO3(g)+NO(g)的ΔH="-41.8" kJ·mol、1。达到平衡状态:a.反应前后为体积不变的反应,所以反应体系压强任何时候都保持不变;错误;b.混合气体颜色保持不变,即二氧化氮气体的浓度不变,达平衡状态;正确;c.SO3和NO为生成物,任何时候体积比都保持不变,无法确定;错误;d.每消耗1 mol SO3为逆反应速率,同时生成1 mol NO2为逆反应速率,方向相同,无法判断;错误;答案为b;测得上述反应平衡时NO2与SO2体积比为1︰6,
NO2(g)+SO2(g)![]() SO3(g)+NO(g)
SO3(g)+NO(g)
起始 a 2a 0 0
变化 x x x x
平衡 a-x 2a- x x x
(a-x)/(2a-x)=1/6,x=4a/5;则平衡常数K=x2/(a-x)×(2a-x)=8/3;(3)CO(g)+2H2(g)![]() CH3OH(g)。压强不变,温度由350℃降到300℃,一氧化碳的转化率增大,平衡右移,正反应放热;ΔH《0;实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是此压强下,一氧化碳转化率接近100%;
CH3OH(g)。压强不变,温度由350℃降到300℃,一氧化碳的转化率增大,平衡右移,正反应放热;ΔH《0;实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是此压强下,一氧化碳转化率接近100%;


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】密闭容器中自由移动的活塞两边分别充入空气和H2、O2的混合气体,开始体积比为1:3,若将H2、O2的混合气体点燃引爆,恢复到原来温度(水为液态),活塞右滑停留于容器的正中央,则原来H2、O2的体积比可能为( ) 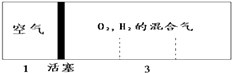
A.2:7
B.5:4
C.1:1
D.7:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为一种常见酸的浓溶液,能使蔗糖变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是

A. X使蔗糖变黑的现象主要体现了X的脱水性
B. 若A为铁,则足量A与X在室温下即可完全反应
C. 若A为碳单质,则将C通入少量的澄清石灰水中,一定可以观察到白色沉淀产生
D. 工业上,B转化为D的反应条件为高温、高压、使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是( )
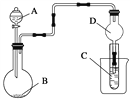
A. 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
B. 若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
D. 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有物质的量浓度相同的5种溶液:(a)NaHSO4,(b)NaHCO3;(c)H2SO4 (d)Al2(SO4)3;(e)Na2CO3,其pH由小到大的顺序为 ( )
A. (c)(a)(b)(d)(e) B. (c)(a)(d) (b)(e)
C. (e)(b)(d)(a)(c) D. (c)(a)(d)(e)(b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是( ) 
A.Mg2+、Al3+、Fe2+
B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+
D.只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸与木炭粉在加热条件下反应.已知酸性KMnO4溶液可以吸收SO2 , 试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物.
编号 | ① | ② | ③ | ④ |
装置 |
|
|
|
|
(1)写出木炭与浓硫酸反应的化学方程式 . 标准状况下,若生成6.72L的气体,则转移电子的物质的量为 . 这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):
→→→ .
(2)实验时可观察到:装置①中A瓶的溶液褪色,C瓶的溶液不褪色.B瓶溶液的作用是 , C瓶溶液的作用是 .
(3)装置②中所加的固体药品是 , 可确证的产物是 , 确定装置②在整套装置中位置的理由是 .
(4)盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com