
【题目】下列关于电解质溶液的判断正确的是
A. 100℃时,NaCl溶液的pH<7,则溶液呈酸性
B. 将pH=4的 CH3COOH溶液加水稀释,溶液中所有离子的浓度均减小
C. 常温下,CH3COOH分子可能存在于pH>7的碱性溶液中
D. 向氨水中加入盐酸至中性,溶液中![]() 一定增大
一定增大
【答案】C
【解析】
A.100℃时,水的电离程度增大,溶液中氢离子的浓度增大,所以该温度下氯化钠溶液的pH<7,因为氯化钠溶液中c(H+)=c(OH-),所以氯化钠溶液为中性溶液,故A错误;
B.pH=4的CH3COOH溶液加水稀释,因为水的离子积不变,所以稀释过程中氢离子浓度减小,则氢氧根离子浓度增大,故B错误;
C.常温下,CH3COOH分子可能存在于pH>7的碱性溶液中,如醋酸钠溶液中醋酸根离子水解成醋酸和氢氧根离子,即醋酸钠溶液中存在醋酸分子,故C正确;
D.氨水中加入盐酸,若恰好完全反应,溶液呈酸性,要使溶液呈中性,则氨水过量,所以溶质为氯化铵和一水合氨,但![]() 为一水合氨的电离平衡常数,温度不变,是一定值,故D错误。
为一水合氨的电离平衡常数,温度不变,是一定值,故D错误。
故选C。


科目:高中化学 来源: 题型:
【题目】已知五种短周期元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成的离子化合物A2B中,所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子分子。试回答下列问题:
(1)写出对应元素的名称:A_____,C_____,E_____。
(2)写出下列物质的电子式:
①D元素形成的单质____;②A、B、E形成的化合物____;③D、E形成的化合物______。
(3)A和B可形成A2B、A2B2两种化合物,E与B可形成E2B、E2B2两种化合物,则下列说法不正确的是_____。
A.A2B2和E2B2中都含有非极性共价键
B.A2B和E2B都含离子键
C.A2B和A2B2中阴阳离子个数比均为1∶2
D.A2B和A2B2均能溶于E2B,并发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置(部分夹持装置及石棉网已省略)或操作能达到实验目的的是

A. 用装置①制乙烯B. 用装置②分离苯和苯酚
C. 用装置③制备乙酸乙酯D. 用装置④验证硫酸、碳酸、苯酚酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示)。下列有关该工艺的说法错误的是( )

A.铝镓合金可以循环使用
B.该过程中,能量的转化形式只有两种
C.铝镓合金与水反应的化学方程式为:2Al+3H2O  Al2O3+3H2↑
Al2O3+3H2↑
D.总反应式为2H2O 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐MN溶于水存在如图过程,下列有关说法中不正确的是

A. 该过程可表示MN的水解过程
B. 相同条件下结合H+的能力N->OH-
C. 该过程使溶液中的c(OH-)>c(H+)
D. 溶液中存在c(HN)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 比较金属镁和铝的活泼性 | 分別向两只盛有等体积等浓度的稀硫酸烧杯中加入打磨过的同样大小的镁片和铝片,比较反应现象 |
B | 除去Mg粉中混有的Al 粉 | 加入足量的NaOH 溶液,过滤、洗涤、干燥 |
C | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
D | 配制0.4000mol·L1的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,直接向烧杯中加入250mL水 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向25 mL 0.1 mol·L-1NaOH溶液中逐滴滴加0.2 mol·L-1的HN3(叠氮酸)溶液,pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的是一元弱酸)。下列说法正确的是

A. 在C点,滴加的V(HN3)=12.5 mL
B. 在B点,离子浓度大小为 c(OH-)>c(H+)>c (Na+)>c(N3-)
C. 水电离出的c(H+):A点小于B点
D. 在D点,c(Na+)=2c(HN3)+2 c(N3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下一定能大量共存的是
A. 强酸性溶液中:H+、NO3-、SO32-
B. pH=12的溶液中:OH-、K+、Cl-、HCO3-
C. 加入铝粉能放出氢气的溶液中一定存在:NH4+、NO3-、AlO2-、SO42-
D. 25C时pH=7的无色溶液中:Na+、Cl-、SO42-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】泄盐(MgSO4·7H2O)是一种中药药剂,还可用于制革、肥料、瓷器、印染料等工业。一种利用氯碱工业的废渣(主要成分是Mg(OH)2,杂质为MnCO3、FeCO3、Al(OH)3、SiO2等)生产泄盐的流程如下:
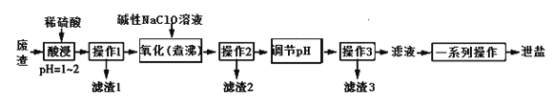
已知部分氢氧化物沉淀pH如下表:
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | Al(OH)3在pH=7.8时开始溶解,pH=10.0完全溶解 |
开始沉淀的pH | 2.3 | 10.8 | 3.7 | |
完全沉淀的pH | 4.3 | 12.4 | 5.2 |
回答下列问题:
(1) “酸浸”是工业对矿物利用的一种方法,该操作关键是提供浸取率和浸取速率,写出提高该工艺流程中“酸浸”速率的2种方法:___________________。
(2) “操作1” “操作2”和“操作3”相同,实验室在进行该操作时,用到的玻璃仪器有________,“滤渣1”的成分是________(写化学式)。
(3) “氧化(煮沸)”操作的目的是使溶液中的锰元素转化为MnO2,写出该反应的离子方程式:____________________。
(4)“调节pH”时最好选用__________, pH范围应控制为____________,高温加热“滤渣3”可得到_________(写化学式)。
(5) “一系列操作”是指_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com