
【题目】普通玻璃是传统的无机非金属材料,在日常生活中非常普遍,制造普通玻璃的主要原是纯碱(Na2CO3)、石灰石(CaCO3)和__(填化学式),其中主要的化学反应有:_____、____;氢氟酸可以腐蚀玻璃,请写出化学反应方程式:______。
【答案】SiO2 Na2CO3+SiO2![]() Na2SiO3+CO2↑ CaCO3+SiO2
Na2SiO3+CO2↑ CaCO3+SiO2![]() CaSiO3+CO2↑ SiO2+4HF=SiF4↑+2H2O
CaSiO3+CO2↑ SiO2+4HF=SiF4↑+2H2O
【解析】
生产玻璃的原料是纯碱、石英和石灰石,高温下碳酸钠和二氧化硅以及碳酸钙和二氧化硅发生反应;常温下,二氧化硅与氢氟酸反应生成四氟化硅和水,据此分析解答。
制造普通玻璃需要的主要原料有纯碱、石灰石和石英,石英的主要成分是SiO2;发生的主要反应有:Na2CO3+SiO2![]() Na2SiO3+CO2↑、CaCO3+SiO2
Na2SiO3+CO2↑、CaCO3+SiO2![]() CaSiO3+CO2↑;常温下,二氧化硅与氢氟酸反应生成四氟化硅和水,反应的化学方程式为:SiO2+4HF=SiF4↑+2H2O,故答案为:SiO2;Na2CO3+SiO2
CaSiO3+CO2↑;常温下,二氧化硅与氢氟酸反应生成四氟化硅和水,反应的化学方程式为:SiO2+4HF=SiF4↑+2H2O,故答案为:SiO2;Na2CO3+SiO2![]() Na2SiO3+CO2↑;CaCO3+SiO2
Na2SiO3+CO2↑;CaCO3+SiO2![]() CaSiO3+CO2↑;SiO2+4HF=SiF4↑+2H2O。
CaSiO3+CO2↑;SiO2+4HF=SiF4↑+2H2O。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。请回答下列问题:
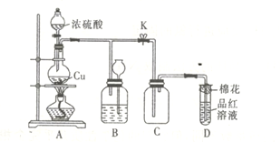
(1)装置A中发生反应的化学方程式为________________________。
(2)装置D中试管口放置的棉花应用一种液体浸泡一下,这种液体是_____,其作用是______。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭弹簧夹K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是___________________。B中应放置的液体是___(填字母)。
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(4)实验中,取一定质量的铜片和一定体积18mol·L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现圆底烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是_______________________。
②下列药品中能用来证明反应结束后的圆底烧瓶中确有余酸的是_________(填字母)。
a.铁粉 b.BaC12溶液 c.银粉 d.Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1L 0.4mol/L HN03溶液中加入Fe粉和Cu粉的混合物9g,充分反应,放出NO气体且金属有剩余。则反应后溶液中c(NO3-)为(忽略溶液体积的变化)
A. 0. 2mol/L B. 0.225 mol/L C. 0.3mol/L D. 0.325 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做同主族元素性质相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
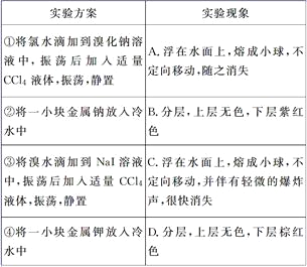
请你帮助该同学整理并完成实验报告。
(1)实验目的:_____________________。
(2)实验用品:
①试剂:金属钠、金属钾、新制氯水、溴水、0.1mol·L-1溴化钠溶液、0.1 mol·L-1碘化钠溶液、四氯化碳等;
②仪器:________、________、________、镊子、小刀、玻璃片等。
(3)实验内容(填写与实验方案对应的实验现象的标号和化学方程式):________

(4)实验结论:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列文字表述与反应方程式对应且正确的是
A. 苯与液溴的反应:![]()
B. 2-丙醇的催化氧化反应:2CH3CH(OH)CH3 + O2 ![]() 2CH3CH2CHO + 2H2O
2CH3CH2CHO + 2H2O
C. 邻羟基苯甲酸与足量的NaHCO3溶液反应:![]() +2NaHCO3
+2NaHCO3![]()
![]() +2CO2↑+2H2O
+2CO2↑+2H2O
D. 实验室制取乙炔的反应:CaC2+2H2O → Ca(OH)2 + CH≡CH↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把40g含二氧化硅的碳酸钙固体在高温下加热到质量不再改变为止,冷却后称得质量为26.8g。求:
(1)生成的二氧化碳在标准状况下的体积为____升?
(2)原混合物中SiO2的质量为_____克?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。

步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收。2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水。
步骤二:通过仪器分析得知X的相对分子质量为106。
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3。如图Ⅰ。
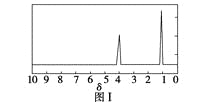
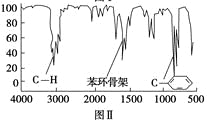
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ。
试填空:
(1)X的分子式为________;X的名称为 。
(2)步骤二中的仪器分析方法称为________。
(3)写出X与足量浓硝酸和浓硫酸混合物反应的化学方程式: 。
(4)写出X符合下列条件的同分异构体结构简式 。
①芳香烃 ②苯环上一氯代物有三种
(5)X以醋酸为溶剂在催化剂作用下用氧气氧化得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度:25 ℃时0.25 g、50 ℃时0.97 g、95 ℃时7.17 g。得到的粗产品中有部分不溶性杂质,请简述实验室中提纯PTA的实验方案: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多巴胺是一种重要的中枢神经传导物质,能影响人对事物的欢愉感受。多巴胺可用香兰素与硝基甲烷等为原料按下列路线合成:
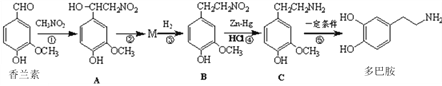
(1)香兰素暴露在空气中易变色,其原因是_____。
(2)多巴胺属于_____有机物(填写序号)①酸性 ②碱性 ③两性;在多巴胺的核磁共振氢谱中可以发现有_____个特征吸收峰。
(3)写出反应②的化学方程式 _______。
(4)上述合成路线中,反应①、④的反应类型分别为_____、_____。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:_____。
①具有天然α-氨基酸的共同结构
②能与FeCl3溶液发生显色反应
③有6种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 石油是混合物,汽油是纯净物B. 石油中只含有液态烷烃
C. 石油含有碳、氢、硫、氧、氮等元素D. 石油具有固定的沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com