
【题目】向1L 0.4mol/L HN03溶液中加入Fe粉和Cu粉的混合物9g,充分反应,放出NO气体且金属有剩余。则反应后溶液中c(NO3-)为(忽略溶液体积的变化)
A. 0. 2mol/L B. 0.225 mol/L C. 0.3mol/L D. 0.325 mol/L
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】欲进行下列实验,其方案设计合理的是( )
A | B | C | D |
检验装置气密性 | 实验室制Fe(OH)2 | 验证浓H2SO4的脱水性、 强氧化性 | 比较NaHCO3和Na2CO3溶解度 |
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是________。
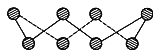
(2)O、S、Se元素的电负性由大到小的顺序为______________________。
(3)H2Se的酸性比H2S_______(填“强”或“弱”),气态SeO3分子的立体构型为__________。
(4)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:__________________________;
②H2SeO4比H2SeO3酸性强的原因:____________________________________________。
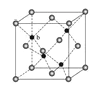
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0 pm,密度为________________g·cm-3(列式并计算),(1pm=10-10 cm)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知某元素的原子结构示意图: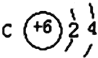 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
(2)已知某元素的原子结构示意图: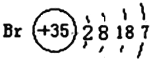 则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
则可知:该元素原子的电子层数为:______,最外层电子数为:______,该元素在周期表的位置是第______周期第______族。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的“原子经济性”反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合绿色化学原理的是
A.乙烯与氧气在银催化作用下生成环氧乙烷(![]() )
)
B.乙烷与氯气制备氯乙烷
C.苯和乙醇为原料,在一定条件下生产乙苯
D.乙醇与浓硫酸共热制备乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)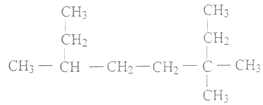 的名称为_____________;
的名称为_____________;
(2) 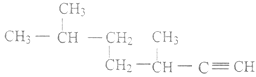 的名称为_________________;
的名称为_________________;
(3)邻甲基乙苯的结构简式为_________________;
(4)顺-2-戊烯的结构简式为_________________;
(5)分子式为C6H12的某烯烃所有碳原子一定共平面,则该烯烃的结构简式为_________________;
(6)某高聚物的结构简式如图:
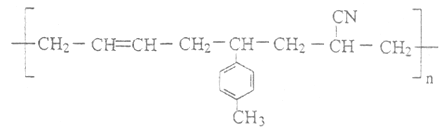
则形成该高分子化合物的单体的结构简式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏合香醇可以用作食用香精,其结构简式如图1所示。
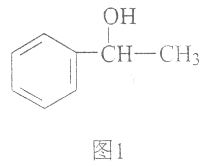
(1)苏合香醇的分子式为_________,它不能发生的有机反应类型有(填数字序号)_________。
①取代反应 ②加成反应 ③消去反应 ④加聚反应
⑤氧化反应 ⑥水解反应
(2)有机物丙是一种香料,其合成路线如图2。其中A为烃,相对分子质量为56;甲的相对分子质量通过质谱法测得为88,它的核磁共振氢谱显示只有三组峰;乙与苏合香醇互为同系物。
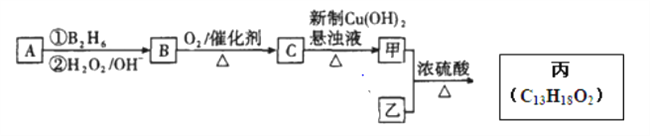
图2
已知:R-CH=CH2 ![]() R-CH2CH2OH
R-CH2CH2OH
R-CHO ![]() R-COOH
R-COOH
①A的名称是_________。
②写出由B到C的化学反应方程式_________。
③B的同分异构体能与钠反应生成氢气,不能发生催化氧化反应,其结构简式为__________________。
④丙中含有两个-CH3,则甲与乙反应的化学方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通玻璃是传统的无机非金属材料,在日常生活中非常普遍,制造普通玻璃的主要原是纯碱(Na2CO3)、石灰石(CaCO3)和__(填化学式),其中主要的化学反应有:_____、____;氢氟酸可以腐蚀玻璃,请写出化学反应方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用下图所示的装置进行有关的实验。
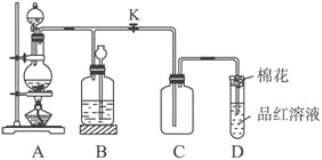
请回答:
(1)装置A中发生反应的化学方程式为_______________。
(2)装置D中试管口放置的棉花中应用某种溶液浸湿,这种溶液是_____,其作用是_______。
(3)实验中,取一定质量的铜片和一定体积18mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组同学根据所学的化学知识认为还有一定量的硫酸剩余,其原因是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com