
【题目】某学生欲称取5.5 g食盐晶体。但在操作时将食盐晶体与砝码的位置放颠倒了,则实际称得的食盐晶体的质量为(1 g 以下用游码)
A. 6.5 g B. 6.0 g C. 5.5 g D. 4.5 g
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3 . 请回答下列问题:
(1)Na3N的电子式是 , 该化合物由键形成.
(2)Na3N与盐酸反应生成种盐,其电子式分别是 , .
(3)Na3N与水的反应属于(填基本反应类型)反应.
(4)比较Na3N中两种粒子的半径:r(Na+)(填“>”“=”“<”) r(N3﹣).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《太平惠民和剂局方》中对精制蜡过程有如下记载:.....先将蜡六两熔化作汁,以重绵滤去滓,以好酒一升,于银石器内煮蜡熔,数沸倾出,候酒冷,其蜡自浮,取蜡称用。”文中涉及的操作方法是( )
A. 蒸馏 B. 升华 C. 干馏 D. 蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关使用托盘天平的叙述,不正确的是
A. 称量前先调节托盘天平的零点
B. 称量时左盘放被称量物,右盘放砝码
C. 潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量
D. 用托盘天平可以准确称量至0.1 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①烧杯、②坩埚、③锥形瓶、④蒸发皿、⑤试管、⑥烧瓶、⑦表面皿,用酒精灯加热时,需要垫石棉网的是
A. ②④⑤ B. ①⑥⑦
C. ③④⑥ D. ①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂对工业污泥中的Cr元素回收与再利用的工艺如下(己知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | — | 一 | — |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(1)实验室用98% (密度为1.84 g·cm-3)的浓硫酸配制200mL4.8 mol·L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为_________mL (保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外,还需_____________________。
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏大的操作是___________(填序号)
a. 转移溶液时,没有等溶液冷却至室温 b.量取浓硫酸时,俯视刻度线
c.当容量瓶中液体占容积2/3左右时,未振荡摇匀 d. 定容时俯视刻度线
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42- 或Cr2O72-),以便于与杂质离子分离;另一方面是_____________________________。(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是___________________。
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是________________。
(6)通SO2气体时,其化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定的温度下,将一定量的氢气和氮气的混合气体充入等压密闭容器中进行反应,达到平衡时维持温度不变,测得混合气体的密度是反应前密度的1.25倍,则达到平衡时,氨气的体积分数为
A. 25% B. 27.5 % C. 30% D. 37.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见右图)。下列说法错误的是
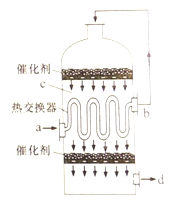
A. a、b两处的混合气体成分含量相同,温度不同
B. c、d两处的混合气体成分含量相同,温度不同
C. 热交换器的作用是预热待反应的气体,冷却反应后的气体
D. c处气体经热交换后再次催化氧化的目的是提高SO2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的工业制法中,正确的是( )
A.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
B.制铁:以铁矿石为原料,CO还原得铁
C.制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁
D.制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com