
����Ŀ�������ŷŵ�β���Ǵ�����Ⱦ����֮һ����μ�����Ⱦ������ŷ��ǿ�ѧ���о������ſ��⡣��ش��������⣺
(1)��֪��CO��ȼ����Ϊ283.0kJ��mol-1��N2(g)+2O2(g)![]() 2NO2(g) ��H= +64kJ��mol-1����NO2(g)+2CO(g)=
2NO2(g) ��H= +64kJ��mol-1����NO2(g)+2CO(g)=![]() N2(g)+2CO2(g) ��H=____kJ��mol-1�����÷�Ӧ����14g��ԭ��������Ӧ����ת�Ƶ���___mol��
N2(g)+2CO2(g) ��H=____kJ��mol-1�����÷�Ӧ����14g��ԭ��������Ӧ����ת�Ƶ���___mol��
(2)ʹ�����ŷŵ�CO��NO��һ�������·�����Ӧ��2NO(g)+2CO(g)![]() N2(g)+2CO2(g)������Ч�ؼ��ٿ�����Ⱦ������һ���¶��£���6mol NO��8mol CO����10L�̶��ݻ��������з���������Ӧ����Ӧ�����и����ʵ�Ũ�ȱ仯��ͼ1��ʾ��
N2(g)+2CO2(g)������Ч�ؼ��ٿ�����Ⱦ������һ���¶��£���6mol NO��8mol CO����10L�̶��ݻ��������з���������Ӧ����Ӧ�����и����ʵ�Ũ�ȱ仯��ͼ1��ʾ��
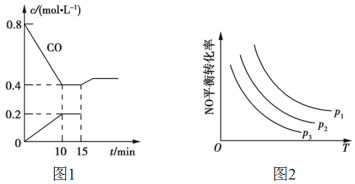
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ��K=___��NO��ƽ��ת����=____��
��15minʱ�����ı䷴Ӧ����������COŨ�ȷ�����ͼ1��ʾ�ı仯����ı������������___(����)��
a.��С������� b.����CO2���� c.�������ͨ��������� d.�������
�۵�NO��CO����ʼŨ�����ʱ����ϵ��NO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ2��ʾ��������˵����ȷ����____ (����)��
A���÷�Ӧ��H<0
B��p1<p2<p3
C�������¶�����Ӧ���ʼ�С���淴Ӧ��������
D���¶Ȳ��䣬����ѹǿ��ƽ�ⳣ������
������˵�������жϷ�Ӧ2NO(g)+2CO(g)![]() N2(g)+2CO2(g)�ﵽƽ�����____(����)��
N2(g)+2CO2(g)�ﵽƽ�����____(����)��
A����Ӧ�������������ʵ������
B����λʱ��������1mol NOͬʱ����1mol CO2
C���������ѹǿ���ٷ����仯
D��NO��Ũ�Ȳ��ٱ仯
����Ӧ�������ٷֱ�����������壬��ʹNOת�����������____(����)��
A��O2 B��N2 C��CO D��NO
���𰸡�-598 1 5(��5L��mol-1) 66.7% b A BCD C
��������
(1)CO��ȼ����Ϊ283.0kJ��mol-1����CO(g)+![]() O2(g)=CO2(g)��H3= -283.0kJ/mol�����ݸ�˹���ɷ������
O2(g)=CO2(g)��H3= -283.0kJ/mol�����ݸ�˹���ɷ������
(2)�ٸ���ͼ��Ӧ�ﵽƽ��״̬ʱ��c(CO)=0.4mol/L�����2NO(g)+2CO(g)![]() N2(g)+2CO2(g)�������ƽ��ʱ�����ʵ�Ũ���ټ���K���ڸ���ͼ��15minʱ���ı䷴Ӧ����������COŨ����������ƽ���ƶ���Ӱ�����ط����жϣ��۸����¶Ⱥ�ѹǿ��ƽ���Ӱ������жϣ��ܸ���ƽ��״̬�����������жϣ��ݸ���Ũ�ȶ�ƽ���Ӱ������жϡ�
N2(g)+2CO2(g)�������ƽ��ʱ�����ʵ�Ũ���ټ���K���ڸ���ͼ��15minʱ���ı䷴Ӧ����������COŨ����������ƽ���ƶ���Ӱ�����ط����жϣ��۸����¶Ⱥ�ѹǿ��ƽ���Ӱ������жϣ��ܸ���ƽ��״̬�����������жϣ��ݸ���Ũ�ȶ�ƽ���Ӱ������жϡ�
(1)��CO��ȼ����Ϊ283.0kJ��mol-1���Ȼ�ѧ����ʽΪCO(g)+![]() O2(g)=CO2(g)��H3= -283.0kJ/mol����N2(g)+2O2(g)
O2(g)=CO2(g)��H3= -283.0kJ/mol����N2(g)+2O2(g)![]() 2NO2(g) ��H= +64kJ/mol�����ݸ�˹���ɣ�������2-����
2NO2(g) ��H= +64kJ/mol�����ݸ�˹���ɣ�������2-����![]() �ã�NO2(g)+2CO(g)=
�ã�NO2(g)+2CO(g)=![]() N2(g)+2CO2(g) ��H=(-283.0kJ/mol)��2-(+64 kJ/mol)��
N2(g)+2CO2(g) ��H=(-283.0kJ/mol)��2-(+64 kJ/mol)��![]() = -598kJ��mol-1����Ӧ�Ļ�ԭ��ΪCO��14g CO�����ʵ���Ϊ
= -598kJ��mol-1����Ӧ�Ļ�ԭ��ΪCO��14g CO�����ʵ���Ϊ![]() =0.5mol��ת�Ƶ���1mol��
=0.5mol��ת�Ƶ���1mol��
(2)�ٸ���ͼ��Ӧ�ﵽƽ��״̬ʱ��c(CO)=0.4mol/L������Ӧ��COΪ8 mol-0.4mol/L��10L=4mol������2NO(g)+2CO(g)![]() N2(g)+2CO2(g)����Ӧ��NOΪ4mol�����ɵ�N2��CO2�ֱ�Ϊ2mol��4mol����ƽ��ʱc(N2)=0.2mol/L��c(CO2)=0.4mol/L��c(NO)=
N2(g)+2CO2(g)����Ӧ��NOΪ4mol�����ɵ�N2��CO2�ֱ�Ϊ2mol��4mol����ƽ��ʱc(N2)=0.2mol/L��c(CO2)=0.4mol/L��c(NO)=![]() =0.2mol/L��K=
=0.2mol/L��K=![]() =5 Lmol-1��NO��ƽ��ת����=
=5 Lmol-1��NO��ƽ��ת����=![]() ��100%=66.7%��
��100%=66.7%��
�ڸ���ͼ��15minʱ���ı䷴Ӧ����������COŨ��������
a. ��С���������CO��ͻȻ������ԭͼ�����ӣ���a����
b. ����CO2������ƽ�������ƶ���COŨ��������b��ȷ��
c. �������ͨ�����������ƽ�ⲻ�ƶ���COŨ�Ȳ��䣬��c����
d. ���������ƽ�ⲻ�ƶ���COŨ�Ȳ��䣬��d����
�ʴ�Ϊ��b��
��A������ͼ�������¶ȣ�NO��ƽ��ת���ʼ�С��˵��ƽ�������ƶ����淴ӦΪ���ȷ�Ӧ��������ӦΪ���ȷ�Ӧ����H<0����A��ȷ��
B������2NO(g)+2CO(g)![]() N2(g)+2CO2(g)���¶���ͬ�ǣ�����ѹǿ��ƽ�������ƶ���NO��ƽ��ת�����������p1��p2��p3����B����
N2(g)+2CO2(g)���¶���ͬ�ǣ�����ѹǿ��ƽ�������ƶ���NO��ƽ��ת�����������p1��p2��p3����B����
C�������¶������淴Ӧ���ʾ�����C����
D���¶Ȳ��䣬ƽ�ⳣ�����䣬��D����
�ʴ�Ϊ��A��
��A����Ӧ�������������ʵ�����ȣ�����˵�����ʵ������䣬�����ж��Ƿ�Ϊƽ��״̬����A����
B����λʱ��������1mol NOͬʱ����1ml CO2��˵�����淴Ӧ������ȣ�Ϊƽ��״̬����B��ȷ��
C��2NO(g)+2CO(g)![]() N2(g)+2CO2(g)Ϊ��������ʵ��������仯�ķ�Ӧ���������ѹǿ���ٷ����仯��˵�����ʵ������䣬�ܹ�˵���ﵽƽ��״̬����C��ȷ��
N2(g)+2CO2(g)Ϊ��������ʵ��������仯�ķ�Ӧ���������ѹǿ���ٷ����仯��˵�����ʵ������䣬�ܹ�˵���ﵽƽ��״̬����C��ȷ��
D��NO��Ũ�Ȳ��ٱ仯��˵����Ӧ�ﵽƽ��״̬����D��ȷ��
�ʴ�Ϊ��BCD��
��A������O2������2NO + O2=2NO2��NOŨ�Ƚ��ͣ�ƽ�������ƶ���NOת���ʼ�С����A����
B������N2��������Ũ������ƽ�������ƶ���NOת���ʼ�С����B����
C������CO��ƽ�������ƶ���NOת��������C��ȷ��
D������NO��NOת���ʼ�С����D����
�ʴ�Ϊ��C��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ������ij���淴Ӧ��ijһ��Ӧ��ӿ�ʼO�㵽�ﵽƽ��״̬C��Ĺ��̵�Ũ�ȱ仯����������й�˵����ȷ����
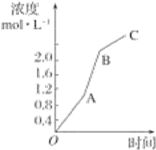
A.�˿��淴ӦΪA![]() B��C
B��C
B.��Ӧ������OA�ε��������
C.��Ӧ������AB�ε��������
D.��Ӧ������BC�ε��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.4molX�����0.6molY��������2L�ܱ������У�ʹ���Ƿ������·�Ӧ��4X(g)+5Y(g) ![]() nZ(g)+6W(g)��2minĩ������0.3molW������֪��Z��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.05mol/(L��min)���Լ���
nZ(g)+6W(g)��2minĩ������0.3molW������֪��Z��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.05mol/(L��min)���Լ���
��1��ǰ2min����W��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ_______________��
��2��2minĩʱY��Ũ��Ϊ_____________________________��
��3����ѧ��Ӧ����ʽ��n=_____________________________��
��4��2minĩ���ָ�����Ӧǰ�¶ȣ���ϵ��ѹǿ�Ƿ�Ӧǰѹǿ��__________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��8��13���й���ѧ�Һϳ�������ȱ���յ��ľ�̬�������ε�һ��ְ����Ba2 [Sn��OH��6][B��OH��4] 2������˸û������LED���������о��������Ϊ�ⷢ�����ƺ�Ӧ���ṩһ���µ���Ч���ԡ�
��1����̬Snԭ�Ӽ۲���ӵĿռ��˶�״̬��___�֣���̬��ԭ�ӵļ۲�����Ų�ʽ���ܱ�ʾΪ![]() ����Ϊ��Υ����____ԭ��������
����Ϊ��Υ����____ԭ��������
��2��[B��OH��4] ������ԭ�ӵ��ӻ��������Ϊ____��[B��OH��4] ���Ŀռ乹��Ϊ______�� [Sn��OH��6] 2���У�Sn��O֮��Ļ�ѧ����������___��
a ![]() �� b ���� c ��λ�� d ���Լ�
�� b ���� c ��λ�� d ���Լ�
��3��̼�ᱵ��̼��þ�ֽ�õ��Ľ����������У��۵�ϵ͵���_____���ѧʽ������ԭ����___________��
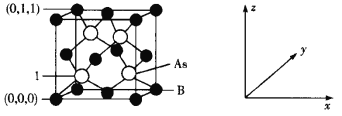
��4�������ȵ��ʰ뵼����������黯��BAs���ľ����ṹ����ͼ��ʾ����1����ԭ�ӵ�����Ϊ____����֪�����ӵ�������ֵΪNA����������Asԭ�ӵ�Bԭ���������Ϊa pm����þ�����ܶ�Ϊ__g��cm��3���г���a��NA�ļ���ʽ���ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��̲��漰������ԭ��Ӧ����( )
A.�ڻ�ҩ�ı�ը
B.��ɰ(![]() )��֮��ˮ���������ֳɵ�ɰ
)��֮��ˮ���������ֳɵ�ɰ
C.����������Һ���ͭ��
D.ʪ����ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������֪ʶ�ж�����˵����ȷ����( )
A.��X�ǵ��������е�һ���������Ԫ�أ���X���ʲ�����ˮ��Ӧ
B.��![]() ��
��![]() ���Ӳ�ṹ��ͬ����ԭ������
���Ӳ�ṹ��ͬ����ԭ������![]() �����Ӱ뾶
�����Ӱ뾶![]()
C.�����Ȼ�����Һ�����Ȼ����ҺŨ����ȣ�������������Һ�е�Kw��������
D.����Ӧ![]() ��һ���������ܹ��Է����У���Ӧ��
��һ���������ܹ��Է����У���Ӧ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��Na2SO4��Al2(SO4)3�Ļ����Һ�У����Al3��Ũ��Ϊ0.1 mol��L��1����������0.3 mol��L��1��BaCl2��Һǡ��ʹ![]() ��ȫ������������Һ��Na����Ũ��Ϊ________��
��ȫ������������Һ��Na����Ũ��Ϊ________��
(2)��0.1 mol��L��1��K2SO4��Һ��0.2 mol��L��1��Al2(SO4)3��Һ�ʹ�ˮ��ϣ�Ҫʹ���Һ��K����Al3����![]() ��Ũ�ȷֱ�Ϊ0.1 mol��L��1��0.1 mol��L��1��0.2 mol��L��1����K2SO4��Һ��Al2(SO4)3��Һ����ˮ���ߵ������________(��������ı仯)��
��Ũ�ȷֱ�Ϊ0.1 mol��L��1��0.1 mol��L��1��0.2 mol��L��1����K2SO4��Һ��Al2(SO4)3��Һ����ˮ���ߵ������________(��������ı仯)��
(3)�ڱ�״���£���һ������HCl����������ļ���ƿ������ʢˮ��ˮ���У�ˮ������������ƿ�ݻ���![]() ���Ѽ���ƿ��ˮ��ȡ��(����HClȫ�����ڼ���ƿ��)������Һ�ܶȵı仯���Բ��ƣ���HCl�����ʵ���Ũ��Ϊ________ mol��L��1��
���Ѽ���ƿ��ˮ��ȡ��(����HClȫ�����ڼ���ƿ��)������Һ�ܶȵı仯���Բ��ƣ���HCl�����ʵ���Ũ��Ϊ________ mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��õ�Ũ�ȵ�NaOH��Һ���ֱ�ζ�Ũ�Ⱦ�Ϊ0.1 mol/L��������(HA��HB��HD)��Һ���ζ���������ͼ��ʾ�������ж���ȷ����( )
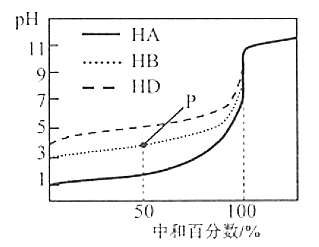
A.��Ũ�ȵ��������к͵�����NaOH��Ҫ������������V(HA)��V(HB)��V(HD)
B.�ӵζ���ʼ��pH=7ʱ��������Һ��ˮ�ĵ���̶�������
C.�ζ���P��ʱ����Һ�У�c(HB)+c(H+)=c(B-)+c(OH-)
D.���кͰٷ�����100%ʱ����������Һ��Ϻ�c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��5.6 g����Ͷ�뵽������100 mL 2 mol��L1��ϡ�����У�2 minʱ���۸պ��ܽ⣬���б�ʾ�����Ӧ��������ȷ����
A.v(Fe)��0.5 mol��L1��min1B.v(H2SO4)��1 mol��L1��min1
C.v(H2SO4)��0.5 mol��L1��min1D.v(FeSO4)��1 mol��L1��min1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com