
����Ŀ����һ�������£���һ���������ܱ������г���2mol A��1mol B���������з�Ӧ��
2A��g��+B��g��2C��g����H��0���ﵽƽ�����t1ʱ�̸ı���������ѧ��Ӧ������ʱ��仯��ͼ�����ж�t1ʱ�̸ı��������Ʋ�����ȷ���ǣ� ��
A.����ѹǿ���䣬���߷�Ӧ�¶�
B.�����¶Ȳ��䣬�����������
C.�����¶Ⱥ�����������䣬����1 mol C��g��
D.�����¶Ⱥ�ѹǿ���䣬����1 mol C��g��
���𰸡�D
���������⣺A���÷�Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ����淴Ӧ���ʶ��������淴Ӧ�������߶���ԭֱ���Ϸ����淴Ӧ������������������Ӧ��������ı���������ƽ�����淴Ӧ�����ƶ�����A����
B�������¶Ȳ��䣬����������������������ڼ�Сѹǿ�����淴Ӧ���ʶ���С�������淴Ӧ�������߶���ԭֱ�ߵ��·�������Ӧ���ʼ�С�ı��������淴Ӧ���ʼ�С�ı���������ƽ�����淴Ӧ�����ƶ�����B����
C�������¶Ⱥ�����������䣬����1molC��g����˲�䣬���������Ũ�������������������Ũ�Ȳ��䣬�����淴Ӧ���ʴ�������Ӧ���ʣ�������Ӧ������ԭ�����нӴ��㣬��C����
D�������¶Ⱥ�ѹǿ���䣬����1molC��g����˲�䣬����������������������Ũ������Ӧ���Ũ�ȼ�С���淴Ӧ���ʴ�������Ӧ���ʣ�ƽ�����淴Ӧ�����ƶ�����D��ȷ��
��ѡD��
�����㾫����������Ҫ�����˻�ѧƽ��״̬���ʼ����������֪ʶ�㣬��Ҫ���ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч��������ȷ�����⣮


 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д� ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ�������ȷ�����ܴﵽĿ���ǣ� �� 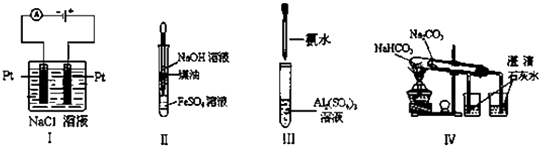
A.ʵ����Ʊ�������
B.ʵ�����ȡ�������������۲�����ɫ
C.ʵ�����ȡ��������������
D.ʵ������Ƚ��������ʵ����ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦA��g��+3B��g��2C��g��+2D��g�����ڲ�ͬ�����µĻ�ѧ��Ӧ�������£����б�ʾ�ķ�Ӧ���������ǣ� ��
A.�ԣ�A��=0.5mol/��Lmin��
B.�ԣ�B��=0.12mol/��Ls��
C.�ԣ�C��=0.1mol/��Ls��
D.�ԣ�D��=0.4mol/��Lmin��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ�ⶨһ��������ijͭ���������ͭ���������������������ʵ�鷽���� �� ������ͭ������� ![]() �ⶨ������������
�ⶨ������������
������ͭ������� ![]() �ⶨʣ������������
�ⶨʣ������������
A.��ҺA����ҺB�������������NaOH��Һ
B.ʵ�����з����������ʵʩ
C.����ҺBѡ��Ũ���ᣬ���ͭ����������ƫ��
D.����һ���ܲ�������������������ʣ��ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.Һ����Һ�ȶ����Դ����ڸ�ƿ��
B.��̬������ǿ�ȼ��
C.��觺�ˮ������Ҫ�ɷֶ��Ƕ�������
D.��Ԫ������Ȼ��Ĵ�����ʽ�����ʡ�����������ε�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ij�������ṹΪ![]() �����ķ���ʽΪ________��һ�ȴ�����________�֡�
�����ķ���ʽΪ________��һ�ȴ�����________�֡�
(2)����ʽΪC6H12��ij��������̼ԭ�Ӷ���ͬһƽ���ϣ�������Ľṹ��ʽΪ__________________________��
������ʽΪC4H6��ij�������е�̼ԭ�Ӷ���ͬһ��ֱ���ϣ�������Ľṹ��ʽΪ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�������������������ȷ����
A. ������Һ̬��ʽ�ɳ�Ϊ��ˮ��Һ��
B. ���ȵ�ͭ˿��������ȼ�գ�������ɫ�Ȼ�ͭ����
C. �������μӵķ�Ӧ��������Һ�н���
D. ����������ȼ�գ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���������ճ������г����Ľ��������ǵĵ��ʼ��仯�����ڿ�ѧ�о���ũҵ�����о��й㷺��;�� ��ش��������⣺
��1����ϸͭ�ۿ�����������ϡ������ȣ����Ʊ�������ͼ1�� 
��Cu2+�ļ۵����Ų�ͼ�� NH4CuSO3��N��O��S����Ԫ�صĵ�һ�������ɴ�С˳��Ϊ����Ԫ�ط��ţ���
��SO42���Ŀռ乹��Ϊ �� SO32����������ԭ�ӵ��ӻ���ʽΪ ��
��2����д����Cu��NH3��4SO4ˮ��Һ��ͨ��SO2ʱ������Ӧ�����ӷ���ʽ��
��3��ijѧ����CuSO4��Һ�м���������ˮ������ɫ�������������������ˮ�����ܽ⣬�õ�����ɫ����Һ����������Һ�м���һ�����Ҵ�������SO4H2O���壮 ������˵����ȷ����
a��������������ˮ������ΪNH3���Ӻ�H2O����֮���γ�3�ֲ�ͬ�����
b��NH3���Ӻ�H2O���ӣ����ӿռ乹�Ͳ�ͬ���������ӵļ���С��ˮ���ӵļ���
c��Cu��NH3��4SO4�����еĻ�ѧ�������Ӽ������Թ��ۼ�����λ��
d��Cu��NH3��4SO4���Ԫ���е縺�������ǵ�Ԫ��
������ͼ����Ҵ������������ԭ��
��4��Cu����Ķѻ���ʽ��ͼ2��ʾ����Cuԭ�Ӱ뾶Ϊr��������Cuԭ�ӵ���λ��Ϊ������Ŀռ�������Ϊ����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����200mLNa2CO3��NaAlO2�Ļ����Һ����μ���1molL��1�����ᣬ�����Һ�е�CO32����HCO3����AlO2����Al3+���ӵ����ʵ��������������Һ������仯��ϵ������ͼһ��ʾ�� 
��1��ԭ�����Һ��Na2CO3�����ʵ���Ũ��ΪmolL��1
��2��V1��V2= ��
��3�����μ���������еõ�����0.975g�������������������ΪmL��
��4����ͼ�������л����û����Һ����μ���1molL��1�����ᣬ���ó��������ʵ��������������Һ������仯��ϵ�� 
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com