
����Ŀ����1�����������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
�ٴ��������У���H2��NO3����ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ����÷�Ӧ���ӷ���ʽΪ____��
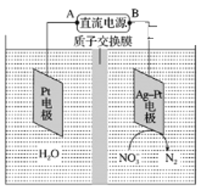
�ڵ绯ѧ����NO3����ԭ����ͼ��ʾ����Դ����Ϊ________���A���� B���������ܷ�Ӧ4NO3-+4H+=5O2+2N2+2H2O����������ӦʽΪ_______��
���ܷ�����ӽ���Ĥ��Ϊ�����ӽ���Ĥ____________����ܡ����ܡ�����
��2���о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����塣
��CO��O2��Ƴ�ȼ�ϵ�أ���KOH��ҺΪ���Һ�����õ�صĸ�����ӦʽΪ______��
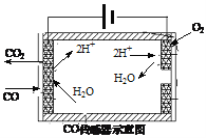
�ڲ�������β���е�COŨ�ȳ��õ绯ѧ����������������ͼ��ʾ�������������ĵ缫��ӦΪ_____________________��
���𰸡�5H2+2NO3-==N2��+2OH-+4H2O A 4NO3-+20e-+24H+=2N2��+12H2O ���� CO-2e-+4OH-=CO32-+2H2O CO-2e-+H2O=CO2+2H+
��������
��1���ٴ��������У���H2��NO3����ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ������ʾ������OH-����÷�Ӧ���ӷ���ʽΪ5H2+2NO3-��N2��+2OH-+4H2O��
�ڴӵ绯ѧ����NO3����ԭ��ͼ�п��Կ�����NO3-ת��ΪN2���˵缫�õ��ӣ�Ϊ�������Ӷ��ó�BΪ��������Դ����ΪA�����ܷ�Ӧ4NO3-+4H+=5O2+2N2+2H2O����������ӦʽΪ4NO3-+20e-+24H+=2N2��+12H2O��
����ΪNO3- ת��ΪN2��Ҫ�����Ի����½��У���Ӧ�����H+��Ҫ�����ṩ�����Բ��ܰ����ӽ���Ĥ��Ϊ�����ӽ���Ĥ��
��2����CO��O2��Ƴ�ȼ�ϵ�أ���KOH��ҺΪ���Һ�����õ�صĸ�����ӦʽΪCO-2e-+4OH-=CO32-+2H2O��
�ڲ�������β���е�COŨ�ȳ��õ绯ѧ���������������ͼ�п��Կ���������CO��H2Oת��ΪCO2��H+�����������ĵ缫��ӦΪCO-2e-+H2O=CO2+2H+��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾAlCl3��Һ��NaOH��Һ��μӹ������������Ĺ�ϵ���ߡ������жϴ�����ǣ� ��
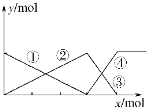
A. ���߱�ʾAl3�������ʵ����ı仯
B. x��ʾAlCl3�����ʵ���
C. ���߱�ʾAl(OH)3�����ʵ����ı仯
D. ���߱�ʾ[Al(OH)4]�������ʵ����ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��������ܴﵽʵ��Ŀ�ĵ��ǣ� ��
A. �ü��ȵķ�����ȥ̼���ƹ����е�̼������
B. ����������Һ�����Եõ�CuCl2����
C. ��������������ˮ�пɳ�ȥ��Ĥ�е�������Һ����е�(NH4)2SO4
D. ����NaBr��KI��Һ���ɷֱ��������ˮ����CCl4��ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���2L���ܱ������м��뷴Ӧ��N2��H2���������·�Ӧ��N2(g)��3H2(g)![]() 2NH3(g)����Ӧ�����еIJ����������±���ʾ������˵����ȷ����
2NH3(g)����Ӧ�����еIJ����������±���ʾ������˵����ȷ����
���ʵ���/ mol ʱ��/min | n(N2) | n(H2) | n(NH3) |
0 | 1.0 | 1.2 | 0 |
2 | 0.9 | ||
4 | 0.75 | ||
6 | 0.3 |
A. 0��2 min�ڣ�NH3�ķ�Ӧ����Ϊ0.1 mol��L��1��min��1
B. 2 minʱ�� H2�����ʵ���0.3 mol
C. 4 minʱ����Ӧ�Ѵﵽƽ��״̬����ʱ�����淴Ӧ�����ʶ�Ϊ0
D. 4��6 min�ڣ�������������ӵ������ʵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǵؿ��к�������Ԫ�ء�
��1����Ԫ�ػ�̬ԭ�Ӻ���δ�ɶԵ�����Ϊ__��
��2��H2O�����ڵ�O��H�������Ӽ�ķ��»����������ǿ��������Ϊ__��
��3��![]() �ķе��
�ķе��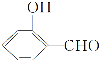 �ߣ�ԭ����___��
�ߣ�ԭ����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ҩ���л���AΪһ����ɫҺ�塣��A�����ɷ�������һϵ�з�Ӧ��
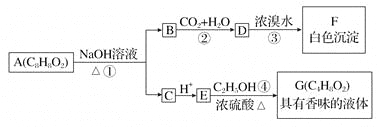
��ش�
��1��д��������F�Ľṹ��ʽ��________________��
��2��д����Ӧ�ٵĻ�ѧ����ʽ��__________________________________________��
��3��д����Ӧ�ܵĻ�ѧ����ʽ��___________________________________________��
��4���л���A��ͬ���칹��ܶ࣬��������������Ļ�����Һ��б����ṹ����________�֡�
��5��E��һ��ͬ���칹��H����֪H���Ժͽ����Ʒ�Ӧ�ų�����������һ�������¿ɷ���������Ӧ����д��H�Ľṹ��ʽ��_________________________________��E����һ��ͬ���칹��R��һ��������Ҳ���Է���������Ӧ�������ܺͽ����Ʒ�Ӧ�ų���������д��R�Ľṹ��ʽ��_____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к��зḻ��þ��Դ��ijͬѧ����˴�ģ�⺣ˮ���Ʊ�MgO��ʵ�鷽����

ģ�⺣ˮ�е�����Ũ��/mol��L��1 | Na�� | Mg2�� | Ca2�� | Cl�� | HCO3�� |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
ע����Һ��ij�����ӵ�Ũ��С��1.0��10��5 mol��L��1������Ϊ�����Ӳ����ڣ�ʵ������У�������Һ������䡣Ksp[CaCO3]��4.96��10��9��Ksp[MgCO3]��6.82��10��6��Ksp[Ca(OH)2]��4.68��10��6��Ksp[Mg(OH)2]��5.61��10��12������˵����ȷ���ǣ� ��
A.������XΪCaCO3
B.��ҺM�д���Mg2����������Ca2��
C.��ҺN�д���Mg2����Ca2��
D.�����������Ϊ����4.2 g NaOH���壬������YΪCa(OH)2��Mg(OH)2�Ļ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£��ı䷴Ӧ����n(SO2)���Է�Ӧ2SO2(g)+O2(g)2SO3(g) ��H<0��Ӱ����ͼ��ʾ������˵����ȷ���ǣ� ��
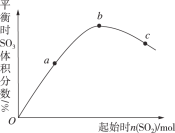
A.��Ӧbc���Ϊƽ��㣬a��δ�ﵽƽ����������Ӧ�������
B.abc�����ƽ�ⳣ��Kb>Kc>Ka
C.����ͼ����Եó�SO2�ĺ���Խ�ߵõ��Ļ��������SO3���������Խ��
D.abc�����У�a��ʱSO2��ת�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
��.���ڿ��淴ӦCO+H2O(g)![]() CO2+H2���ش��������⣺
CO2+H2���ش��������⣺
(1)830 Kʱ������ʼʱc(CO)=2 mol��L-1��c(H2O)=3 mol��L-1��ƽ��ʱCO��ת����Ϊ60%��ˮ������ת����Ϊ _____________;ƽ�ⳣ��K��ֵΪ _____________��
(2)830 Kʱ����ֻ����ʼʱc(H2O)��Ϊ6 mol��L-1����ˮ������ת����Ϊ_____________ ��
(3)��830 Kʱ��ijʱ�̻����ϵ�и������Ũ��Ϊc(CO2)=0.4 mol��L-1c(CO)=0.6 mol��L-1c(H2O)=3 mol��L-1��c(H2)=2 mol��L-1���ж�����ϵ�з�Ӧ���еķ���______________ (�����������������������������ﵽƽ����)��
��������ѹ�£���һ���ݻ��ɱ�������з������·�Ӧ��A(g)+B(g) ![]() C(g)
C(g)
(1)����ʼʱ����1mol A��1mol B���ﵽƽ�������a mol C����ʱA�����ʵ���Ϊ _______ mol��
(2)����ʼʱ����3mol A��3mol B���ﵽƽ�������C�����ʵ���Ϊ _______mol��
(3)����ʼʱ����x mol A2mol B��1mol C���ﵽƽ���A��C�����ʵ����ֱ�Ϊy mol��3a mol����x= ______��y= _________��
(4)����(3)��ƽ���������ټ���3mol C�����ٴδﵽƽ���C�����ʵ��������� _______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com