
【题目】合成某物中间体的片段如下:
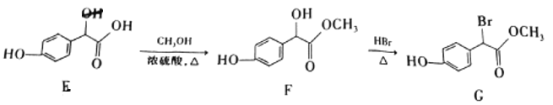
下列说法错误的是( )
A.E→F和F→G反应都是取代反应
B.E、F和G都能与Na、NaOH反应
C.E、F和G分子中碳原子都不可能共平面
D.与E的分子式相同且苯环上含2个-OH、1个-CH2COOH的结构有6种
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
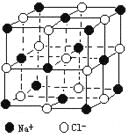
【题目】晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体的晶胞如右图所示。 随着科学技术的发展,测定阿伏加德罗常数的手段越来越多,测定精确度也越来越高。现有一简单可行的测定方法,具体步骤如下:①将固体食盐研细,干燥后,准确称取m gNaCl固体并转移到定容仪器A中。②用滴定管向仪器A中加苯,并不断振荡,继续加苯至A仪器的刻度线,计算出NaCl固体的体积为VmL。回答下列问题:
⑴步骤①中A仪器最好用__________________(填仪器名称)。
⑵能否用胶头滴管代替步骤②中的滴定管______,其原因是____________。
⑶能否用水代替苯_______,其原因是______________________。
⑷经X射线衍射测得NaCl晶胞中最邻近的Na+ 和Cl- 平均距离为acm,则利用上述
方法测得的阿伏加德罗常数的表达式为NA=_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
(1)W2-离子的结构示意图为______________,E元素在周期表中的位置为____________,写出E的最高价氧化物与D的最高价氧化物的水化物反应的离子方程式____________________。
(2)经测定A2W2为二元弱酸,A2W2的电子式为___________,常用硫酸处理BaO2来制备A2W2,写出该反应的化学方程式__________________________。
(3)向含有Fe2+和淀粉KI的酸性溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀成.当消耗2mol I﹣时,共转移3mol电子,该反应的离子方程式是_____________________。
(4)元素D的单质在一定条件下,能与A单质化合生成一种化合物DA,熔点为800℃,能与水反应放氢气,写出该反应方程式______________________,若将1molDA和1molE单质混合加入足量的水,充分反应后生成气体的体积是_________L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请回答:
(1)Y元素的名称是____________。
(2)XZ3化合物的电子式是______________ 分子的立体构型_______________
(3)分别写出X、Y的最高价含氧酸的分子式_____________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为MnO2,含少量Fe2O3、FeO、A12O3、SiO2等杂质)为原料制备锰酸锂的流程如图所示。
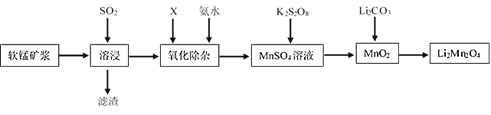
(1)溶浸生产中为提高SO2回收率可采取的措施有__(填序号)
A.不断搅拌,使SO2和软锰矿浆充分接触
B.增大通入SO2的流速
C.减少软锰矿浆的进入量
D.减小通入SO2的流速
(2)已知:室温下,Ksp[A1(OH)3]=1×10-33,Ksp[Fe(OH)3]=l×10-39,pH=7.1时Mn(OH)2开始沉淀。氧化除杂时(室温)除去MnSO4液中的Fe3+、Al3+(使其浓度小于1×l0-6mol/L),需调节溶液pH范围为__。
(3)由硫酸锰与K2S2O8溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。请写出发生反应的离子方程式__。
(4)将MnO2和Li2CO3按4:1的物质的量比配料,混合搅拌,然后升温至600℃750℃,制取产品LiMn2O4。写出该反应的化学方程式__。
(5)锰酸锂可充电电池的总反应为:Li1-xMn2O4+LixC![]() LiMn2O4+C(0<x<1)
LiMn2O4+C(0<x<1)
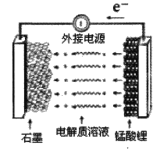
①充电时,电池的阳极反应式为__,若此时转移lmole-,则石墨电极将增重__g。
②废旧锰酸锂电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按系统命名法命名:
有机物CH3CH(C2H5)CH(CH3)2的名称是________________________。
(2)写出下列各种有机物的结构简式:
①2,3二甲基4乙基己烷_________________;
②支链只有一个乙基且相对分子质量最小的烷烃___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“中国芯”的发展离不开单品硅,四氯化硅是制备高纯硅的原料、某小组拟在实验室用下列装置模拟探究四氯化的制备和应用(夹持装置已省略)。
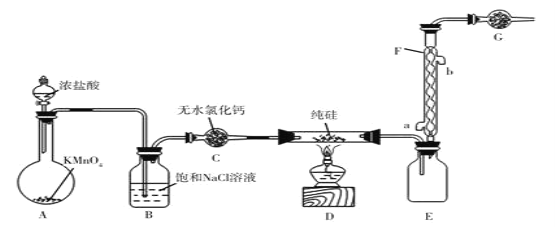
已知有关信息:
①Si+3HCl![]() SiHCl3+H2,Si+2Cl2
SiHCl3+H2,Si+2Cl2![]() SiCl4
SiCl4
②SiCl4遇水剧烈水解,SiCl4的熔点、沸点分别为-70.0℃、57.7℃
请回答下列问题
(1)装浓盐酸的仪器名称是________________。
(2)写出A中发生反应的离子方程式________________。
(3)若拆去B装置,可能的后果是________________(写出一个即可)。
(4)有同学最初将E、F、G装置设计成图Ⅱ装置,图Ⅱ装置的主要缺点是________________。(写出一个即可)
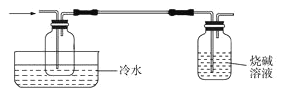

(5)已知NH4Cl在高温条件下易分解生成NH3和HCl。利用SiCl4和NH3制备新型无机非金属材料(Si3N4)的装置如图III。写出该反应的化学方程式:________________利用尾气制备盐酸,宜选择下列装置中的________________(填字母)。

(6)取少量SiCl4产品溶于足量蒸馏水中生成硅酸,该反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种烈化物和两种氧化物。某学习小组在实验用C12和NO制备NOCl并测定其纯度,相关实验(装置略去)如下。请回答:
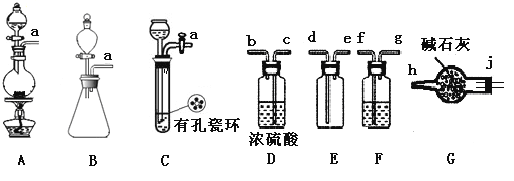
(1)制备Cl2发生装置可______ (填大写字母),反应的离子方程式为_______。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→________(按气流方向,用小写字母表示),若用到F,其盛装药品为_________。
(3)实验室可用下图装置制备亚硝酰氯(NOCl)
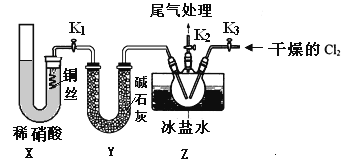
①实验室也可用B装置制备NO,上图X装置的优点为__________(至少写出两点)
②检验装置气密性并装入药品,打开k2,然后再打开____(填“k1”或“k3”),通入一段时间气体,其目的为________,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装肖Y,则Z中NOCl可能发生反应的化学方程式为_________
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL.已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12,则亚硝酰氯(NOC1)的质量分数为____(用代数式表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
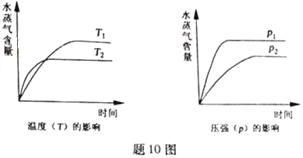
【题目】一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合题图10 的是
A. CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g);△H<0
CO(NH2)2(s)+H2O(g);△H<0
B. CO2(g)+H2(g)![]() CO(g)+H2O(g);△H>0
CO(g)+H2O(g);△H>0
C. CH3CH2OH (g)![]() CH2=CH2(g)+H2O(g);△H>0
CH2=CH2(g)+H2O(g);△H>0
D. 2C6H5CH2CH3(g)+O2(g)![]() 2 C6H5CH=CH2(g)+2H2O(g);△H<0
2 C6H5CH=CH2(g)+2H2O(g);△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com