
【题目】某研究小组同学在实验室用卤块制备少量Mg(ClO3)2·6H2O,其流程如图所示:
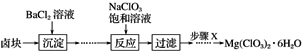
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)的变化曲线如图所示。

③形成氢氧化物沉淀时,不同离子对应溶液的pH如下:Fe2+开始沉淀的pH为5.8,完全沉淀的pH为8.8;Fe3+开始沉淀的pH为1.1,完全沉淀的pH为3.2;Mg2+开始沉淀的pH为8.2,完全沉淀的pH为11。
④可选用的试剂:H2O2、稀硫酸、KMnO4溶液、MgCl2溶液、MgO。
(1)步骤X包含的操作为___________、 ___________、____________、过滤洗涤并干燥。
(2)加入BaCl2溶液沉淀后需经过两步实验步骤才进行下步反应,请写出这两步实验步骤:
①________________________________________________________________________;
② _______________________________________________________________________;
(3)加入NaClO3饱和溶液发生反应的化学方程式为_______________________________。
(4)将Mg(ClO3)2加入到含有KSCN的FeSO4溶液中立即出现红色,写出相关反应的离子方程式______________。
【答案】 蒸发结晶 趁热过滤 冷却结晶 向溶液中加入稍过量双氧水,充分反应 向溶液中加入氧化镁调节pH为3.2~8.2. MgCl2+2NaClO3===Mg(ClO3)2+2NaCl↓ ClO+6Fe2++6H+===6Fe3++Cl-+3H2O
【解析】卤块的成分有MgCl2·6H2O、MgSO4、FeCl2,加入氯化钡溶液后,可以将硫酸根离子转化为硫酸钡沉淀,再向反应后的溶液中加入氧化剂,亚铁离子可以被氧化为三价铁离子,加入氧化镁,调节pH可以促进铁离子的水解,将铁离子转化为氢氧化铁而除去,过滤,得到的滤液是氯化镁,加入饱和氯酸钠溶液得到氯酸镁,可以根据物质的溶解度受温度的影响情况来获得要制取的物质,据此解答。
卤块的成分有MgCl2·6H2O、MgSO4、FeCl2,加入氯化钡溶液后,可以将硫酸根离子转化为硫酸钡沉淀,再向反应后的溶液中加入氧化剂,亚铁离子可以被氧化为三价铁离子,加入氧化镁,调节pH可以促进铁离子的水解,将铁离子转化为氢氧化铁而除去,过滤,得到的滤液是氯化镁,加入饱和氯酸钠溶液得到氯酸镁,可以根据物质的溶解度受温度的影响情况来获得要制取的物质,则
(1)根据物质的溶解度大小可判断,溶液获得晶体的方法:蒸发浓缩,趁热过滤,冷却结晶、过滤、洗涤、干燥;
(2)由于不能引入新杂质,所以选择绿色氧化剂双氧水氧化亚铁离子,利用氧化镁调节pH,即这两步实验步骤分别为向溶液中加入稍过量双氧水,充分反应;向溶液中加入氧化镁调节pH为3.2~8.2;
(3)由于氯化钠的溶解度最小,所以根据以上分析可知加入NaClO3饱和溶液发生反应的化学方程式为MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓。
(4)将Mg(ClO3)2加入到含有KSCN的FeSO4溶液中立即出现红色,这是由于氯酸根离子具有氧化性,可以将亚铁离子氧化为铁离子,反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O。


科目:高中化学 来源: 题型:
【题目】t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t ℃时AgCl的Ksp=4×10-10,下列说法不正确的是
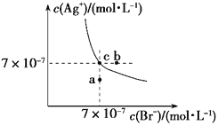
A. 在t ℃时,AgBr的Ksp为4.9×10-13
B. 通过蒸发,可使溶液由a点变到c点
C. 图中b点有AgBr沉淀析出
D. 在t ℃时,AgCl(s)+Br-(aq) ![]() AgBr(s)+Cl-(aq)的平衡常数K≈816
AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于4NH3(g) + 3O2(g) = 2N2(g) + 6 H2O(g) 的反应来说,以下化学反应速率的表示中反应速率最快的是
A. v(NH3)=0.6 mol L-1min-1B. v(O2) =0.4 mol L-1min-1
C. v(N2)=0.2 mol L-1min-1D. v(H2O) =0.3 mol L-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】强酸与强碱的稀溶液反应的热化学方程式为H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,向1L0.5mol·L-1的NaOH溶液中加入下列物质:①稀醋酸、②浓硫酸、③稀硝酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,三者的关系正确的是( )
A.ΔH1>ΔH2>ΔH3B.ΔH1<ΔH3<ΔH2
C.ΔH1=ΔH3>ΔH2D.ΔH1>ΔH3>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向X溶液中缓慢滴加Y溶液,生成沉淀的质量如图所示,符合图像的一组是

X | Y | |
A | AlCl3、Mg(NO3)2、HNO3 | NaOH |
B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 |
C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH |
D | NaAlO2、氨水、NaOH | H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某绿色农药结构简式为,回答下列问题。

(1)N元素的基态原子核外有_____种空间运动状态的电子,该农药组成元素中,第一电离能较大的前三种元素是(按由大到小顺序排列)__________________(用元素符号回答,下同),基态硒原子的价层电子排布式为________________________。
(2)该物质中杂化轨道类型为sp2的原子有__________。
(3)碳、氢、氧元素可形成一系列的化合物,如CH4、C2H6、CH3OH等。与CH4互为等电子体的一种微粒是______。
(4)硒化锌的晶胞结构如图所示,则硒的配位数为_______,若晶胞边长为d pm,设阿伏加德罗常数的值为NA,则硒化锌的密度为____________g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C原子序数依次增大,A3-与B2-、C+电子层结构相同.则下列说法中不正确的是( )
A. 三种元素可组成CAB2和CAB3型化合物
B. 原子半径:A>B>C
C. H2B在同主族元素气态氢化物中最稳定
D. B的某种单质可用于杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A. 1L1.0mo1L-1的NaAlO2水溶液中含有的氧原子数为2NA
B. 标准状况下,11.2LNO与11.2LO2混合后所含分子数为0.75NA
C. Na2O和Na2O2混合物的物质的量为1mol,其中含有的阴离子总数为NA
D. 室温下,将9g铝片投入0.5L 18.4molL-1的H2SO4中,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对下列9种元素,完成以下各小题
周期 | IA | ⅡA | ⅢA | ⅣA | ⅥA | ⅦA | O | |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)常见单质为有色气体的元素是_______(填名称)。
(2)用电子式表示元素④和⑨形成化合物的过程_________。
(3)最高价氧化物对应的水化物中酸性最强的是_________(填化学式)。
(4)④和⑥两者的最高价氧化物对应的水化物反应的离子方程式为_______。
(5)⑦的单质的用途正确的是_____。
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(6)元素①和⑦非金属性较强的是____(填写元素符号),写出一个能表示二者非金属性强弱关系的化学方程式为:_______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com