
【题目】(4分)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6、⑥CH3CH=CH2中,一定互为同系物的是 ,一定互为同分异构体的是 。(填编号)
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】有下列有机物:
① CH2=CH2 ②![]()
③ CH3CH(OH)CH2CH3 ④ (CH3)2C=CH2
⑤ CH3CH2OCH2CH3 ⑥ CH3CH=CHCH=CHCOOH
(1)属于羧酸的是_____(填序号)。
(2)与③互为同分异构体的是_____(填序号)。
(3)与①互为同系物的是_____(填序号)。
(4)用系统命名法给④命名,其名称为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验需要![]() NaOH溶液475mL和
NaOH溶液475mL和![]() 硫酸溶液
硫酸溶液![]() 根据这两种溶液的配制情况回答下列问题:
根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是______![]() 填序号
填序号![]() ,配制上述溶液还需用到的玻璃仪器是______
,配制上述溶液还需用到的玻璃仪器是______![]() 填仪器名称
填仪器名称![]() .
.

(2)下列操作中,不能用容量瓶实现的有______![]() 填序号
填序号![]() .
.
A.配制一定体积准确浓度的标准溶液
B.量取一定体积的液体
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.贮存溶液
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为______![]() 在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度______
在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度______![]() 填”大于”、“等于”或“小于”,下同
填”大于”、“等于”或“小于”,下同![]() 若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度______
若定容时,有少许蒸馏水洒落在容量瓶外,则所得溶液浓度______![]() .
.
(4)根据计算得知,所需质量分数为![]() 、密度为
、密度为![]() 的浓硫酸的体积为______
的浓硫酸的体积为______![]() 计算结果保留一位小数
计算结果保留一位小数![]() 如果实验室有10mL、15mL、20mL、50mL量筒,选用______mL量筒最好.
如果实验室有10mL、15mL、20mL、50mL量筒,选用______mL量筒最好.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验中预计需要使用480mLamol/L的纯碱溶液,下面是某同学在实验室配制该溶液的流程图,回答下列问题:

(1)流程图中的配制过程少了第⑤步,请指出缺少的步骤内容是_____________________________
(2)所选容量瓶最合适的v值为____________,根据图示的相关数据,可求出a=__________.容量瓶在使用之前必须进行的一项操作是________________________。
(3)所给出的流程图中体现出的操作内容有三个明显错误(其中不包括缺少的第⑤步),请写出:
①__________________________②________________________③__________________________。
(4)指出下列实验操作对结果以及对所配制溶液浓度的影响,填写“偏大”“偏小”或者“无影响”.
①溶解后,没有洗涤玻璃棒以及烧杯:_________________
②定容时俯视刻度线:_________________
③未经冷却趁热将溶液注入容量瓶中______________
④容量瓶洗涤后,未经干燥处理_______________
⑤摇匀后发现液面低于刻度线继续加水定容______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应:mA(g)+nB(g)![]() r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是
r C(g)在密闭容器中进行。下图表示此反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线。由曲线分析下列判断正确的是

A. T1>T2,p1>p2,m+n>r,正反应吸热
B. T1<T2,p1<p2,m+n<r,正反应吸热
C. T1>T2,p1>p2,m+n<r,正反应放热
D. T1<T2,p1<p2,m+n>r,正反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________mol;
(2)该气体所含原子总数为____________个;
(3)该气体在标准状况下的体积为____________L;
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为_____________;
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为____________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:S(g) + O2 (g) = SO2(g) ΔH=-Q1kJ/mol ; S(s) + O2 (g) = SO2(g) ΔH=-Q2 kJ/mol。 则Q1 Q2
A. 大于 B. 小于 C. 等于 D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物在科研与生活中有很重要的作用。回答下列问题:
(1)碘可用作心脏起搏器电源——锂碘电池的材料,则碘电极是电池的______(填“正”或“负”)极。
(2)“加碘食盐”中含有少量的KIO3,向其中加入亚硫酸氢钠溶液,能产生使淀粉变蓝的物质,则该反应中氧化剂与还原剂的物质的量之比是_______________。
(3)碘单质与氢气反应的能量变化过程如图所示:

写出碘I2(s)转化成碘I2(g)的热化学方程式:__________________________________。
(4)在合成氨工业中用I2O5来测定CO的含量:5CO(g)+I2O5(s) ![]() 5CO2(g)+I2(s),在装有足量的I2O5固体的2L恒容密闭容器中通入2molCO发生上述反应,测得温度T1、T2下,一氧化碳的体积分数
5CO2(g)+I2(s),在装有足量的I2O5固体的2L恒容密闭容器中通入2molCO发生上述反应,测得温度T1、T2下,一氧化碳的体积分数![]() (CO)随时间t的变化曲线如图所示。回答下列问题:
(CO)随时间t的变化曲线如图所示。回答下列问题:
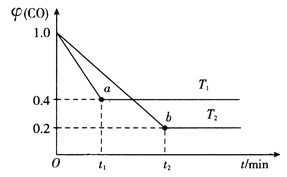
①温度T1下的平衡转化率![]() =________%,b点的平衡常数K2=__________。
=________%,b点的平衡常数K2=__________。
②在温度T2下,反应达到平衡后再充入适量的CO,重新达到平衡时;CO气体的转化率将_______(填“变大”“变小”或“不变”),该反应的△H_____(填“>”“<"或“=”)0。
③下列各种措施能提高该反应的CO转化率的是____________。
A.升温 B.加压 C.添加催化剂 D.移走部分CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是()
A. 在过滤、蒸发、溶解、蒸馏、萃取实验操作中一定要用到玻璃棒的是过滤、蒸发、溶解
B. 200ml 0.25mol/L HCl 溶液与 100ml 0.5mol/L NaCl 溶液所含的 Cl-的物质的量浓度相同
C. 将 5mol/L 的 Mg(NO3)2 溶液 a ml 稀释至 b ml,稀释后溶液中 NO3-的物质的量浓度变为10a/b mol/L
D. 某位同学配制一定物质的量浓度的 NaOH 溶液时,溶解后未冷却至室温就进行后续正常操作, 则造成所配溶液的浓度偏高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com