
【题目】有下列有机物:
① CH2=CH2 ②![]()
③ CH3CH(OH)CH2CH3 ④ (CH3)2C=CH2
⑤ CH3CH2OCH2CH3 ⑥ CH3CH=CHCH=CHCOOH
(1)属于羧酸的是_____(填序号)。
(2)与③互为同分异构体的是_____(填序号)。
(3)与①互为同系物的是_____(填序号)。
(4)用系统命名法给④命名,其名称为_____。
科目:高中化学 来源: 题型:
【题目】化合物A相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1∶2∶2∶3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是( )
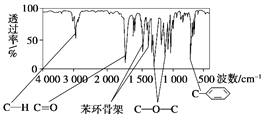
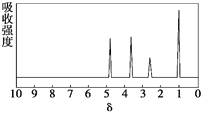
A. 符合题中A分子结构特征的有机物只有1种
B. A属于酯类化合物,在酸性条件下水解产物遇FeCl3溶液显紫色
C. A在一定条件下可与4 mol H2发生加成反应
D. 与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫、钴及其相关化合物用途非常广泛。回答下列问题:
(1)基态Co原子价电子轨道排布式为________,第四电离能I4(Co)<I4(Fe),其原因是_______;Co与Ca同周期且最外层电子数相同,单质钴的熔沸点均比钙大,其原因是_______.
(2)单质硫与熟石灰加热产物之一为CaS3,S32-的几何形状是_______,中心原子杂化方式是_______,与其互为等电子体的分子是_______ (举1例)。
(3)K和Na位于同主族,K2S的熔点为840℃,Na2S的熔点为950℃,前者熔点较低的原因是_______ 。
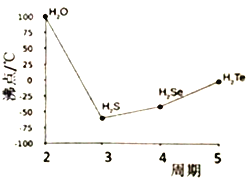
(4)S与O、Se、Te位于同一主族,它们的氢化物的沸点如右图所示,沸点按图像所示变为的原因是_______ 。
(5)钴的一种化合物晶胞结构如下图所示。

①已知A点的原子坐标参数为为(0,0,0),B点为(![]() ,0,
,0,![]() ),则C点的原子坐标参数为_____。
),则C点的原子坐标参数为_____。
②已知晶胞参数为a=0.5485nm,则该晶体的密度为_____g/cm3(列出计算表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 阿伏加德罗常数是12g碳中所含有的碳原子数
B. 已知微粒个数,可通过阿伏加德罗常数计算出微粒的物质的量
C. 阿伏加德罗常数的数值是6.02×1023
D. 阿伏加德罗常数的符号为NA,通常用6.02×1023表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在总结元素化合物性质的过程中,发现化学反应无非是与以下几类物质的反应,并发现同一物质类别具有一定的通性。

(1)若A由短周期金属元素组成,其最外层电子数比电子层数少2。
①组成A的元素在周期表中的位置是_______。
②下列说法正确的是_______(填字母)。
a. A的金属性在短周期元素中最强
b. F可能使酚酞溶液变红
c. A能从D溶液中置换出活泼性较弱的金属单质
(2)若A在通常情况下为黄绿色气体。
①若B为一种金属单质,则A与B反应的方程式为_______。(任举一例)
②若C为NaOH溶液,则与0.5 mol A反应转移电子数为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩尔质量是 ______ 的物质所具有的质量![]() 符号: ______
符号: ______ ![]() 单位: ______ 或 ______ .
单位: ______ 或 ______ .
A. 单位物质的量;M;![]() ;
;![]()
B. 物质的量;m;![]() ;
;![]()
C. 单位物质的量;m;g;![]()
D. 物质的量;M;![]() ;kg
;kg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用电解锰阳极泥(主要成分MnO2、MnO)制备MnO2的工艺流程如下:
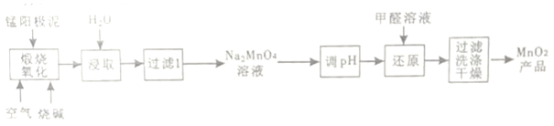
(1)“煅烧氧化”时,1mol MnO煅烧完全转化为Na2MnO4失去电子的物质的量为___________;MnO2煅烧反应的化学方程式为__________________。
(2)“浸取”时,为提高Na2MnO4的浸取率,可采取的措施有____________、____________(列举2点)
(3)“调pH”是将溶液pH 调至约为10,防止pH较低时Na2MnO4自身发生氧化还原反应,生成MnO2和___________;写出用pH试纸测定溶液pH的操作_______________。
(4)“还原”时有无机含氧酸盐生成,发生反应的化学方程式为_____________。
(5)测定产品中MnO2质量分数的步骤如下:
步骤1. 准确称取mg产品,加入c1mol·L-1Na2C2O4溶液V1mL (过量)及适量的稀硫酸,水浴加热煮沸一段时间。(已知:Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4)
步骤2. 然后用c2mol·L-1KMnO4标准溶液滴定剩余的Na2C2O4滴定至终点时消耗KMnO4标准溶液V2mL。(已知:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
步骤2达滴定终点时判断依据是_____________;产品中MnO2的质量分数为ω(MnO2)=____________(列出计算的表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家哈伯因研制合成氨作出重大贡献而获得1918年诺贝尔化学奖,如今可以用电化学的方法合成氨,装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是( )
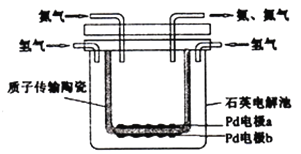
A. Pd电极b为阴极 B. 阴极的反应式为:N2+6H++6e-=2NH3
C. H+由阳极向阴极迁移 D. 陶瓷可以隔离N2和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(4分)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6、⑥CH3CH=CH2中,一定互为同系物的是 ,一定互为同分异构体的是 。(填编号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com