
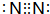 ��
������ A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ�A��B��ɵij����������ʹʪ��ĺ�ɫʯ����ֽ���������ΪNH3��AΪH��BΪNԪ�أ�A��C����ͬһ���壬���ԭ��������֪��CΪNa��C��D��E����ͬһ���ڣ�Ӧ�ô��ڵ������ڣ�Eԭ�ӵ�������������A��B��Cԭ������������֮�ͣ���Eԭ������������Ϊ��1+1+5=7����EΪCl��E�ĵ���������ף�NH3����Ӧ������B�ĵ��ʣ�ͬʱ������������ˮ�������ԵĻ������Һͱ���Ӧ��Ϊ�Ȼ�狀��Ȼ��⣬����0.1mol/L������ҺpH��1������ΪNH4Cl����ΪHCl��D�ĵ��ʼ�����C��Na��Ԫ������������ˮ�������Һ������������Һ����Ӧ�����ζ���Ҳ�������HCl����ˮ��Һ��Ӧ�������죬��D����������Ϊ�������������DΪAlԪ�أ��ʶ�ΪNaAlO2����Ϊ�Ȼ�����
��� �⣺A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ�A��B��ɵij����������ʹʪ��ĺ�ɫʯ����ֽ���������ΪNH3��AΪH��BΪNԪ�أ�A��C����ͬһ���壬���ԭ��������֪��CΪNa��C��D��E����ͬһ���ڣ�Ӧ�ô��ڵ������ڣ�Eԭ�ӵ�������������A��B��Cԭ������������֮�ͣ���Eԭ������������Ϊ��1+1+5=7����EΪCl��E�ĵ���������ף�NH3����Ӧ������B�ĵ��ʣ�ͬʱ������������ˮ�������ԵĻ������Һͱ���Ӧ��Ϊ�Ȼ�狀��Ȼ��⣬����0.1mol/L������ҺpH��1������ΪNH4Cl����ΪHCl��D�ĵ��ʼ�����C��Na��Ԫ������������ˮ�������Һ������������Һ����Ӧ�����ζ���Ҳ�������HCl����ˮ��Һ��Ӧ�������죬��D����������Ϊ�������������DΪAlԪ�أ��ʶ�ΪNaAlO2����Ϊ�Ȼ�����
��1����������������֪���Ļ�ѧʽΪNH3��B����ΪN2������ʽΪ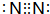 ��
��
�ʴ�Ϊ��NH3��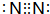 ��
��
��2��DԪ�ص������������ʴ�Ϊ������
��3��NaAlO2��Һ��ͨ�����������̼����Ӧ��������������̼�����ƣ����ӷ���ʽΪ��AlO2-+2H2O+CO2�THCO3-+Al��OH��3����
�ʴ�Ϊ��AlO2-+2H2O+CO2�THCO3-+Al��OH��3����
��4��N2+3H2 2NH3
2NH3
��ʼ��mol����2 1.6 0
��Ӧ��mol����0.4 1.2 0.8
ƽ�⣨mol����1.6 0.4 0.4mol/L��2L
ƽ�ⳣ��K=$\frac{{{{��\frac{0.8mol}{2L}��}^2}}}{{\frac{1.6mol}{2L}��{{��\frac{0.4mol}{2L}��}^3}}}$=25��
�ʴ�Ϊ��25��
��5�������백����Ӧ����NH4Cl��HCl���������ʵ���֮��Ϊ2��4����÷�Ӧ����ʽΪ��3Cl2+4NH3=N2+2NH4Cl+4HCl���÷�Ӧ�б��������ǰ���������ԭ��Ϊ������������ȫ����ԭ����4mol��������2mol�����������Ը÷�Ӧ�б������������뱻��ԭ�����ʵ����ʵ���֮��Ϊ2��3��
�ʴ�Ϊ��2��3��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��漰Ԫ�ػ��������ʡ�����ʽ����ѧƽ�ⳣ����������ԭ��Ӧ����ȣ��Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
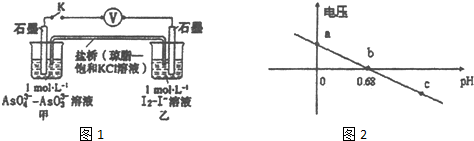
| A�� | pH=5 ʱ�������缫��ӦʽΪ2I--2e-�TI2 | |
| B�� | b��ʱ����Ӧ���ڻ�ѧƽ��״̬ | |
| C�� | a��ʱ��������K+�����ƶ� | |
| D�� | pH��0.68ʱ��������I2��AsO43- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鲽�� | Ԥ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH | B�� | Na2O | C�� | Na | D�� | CaO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų����������ش��������⣺
��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
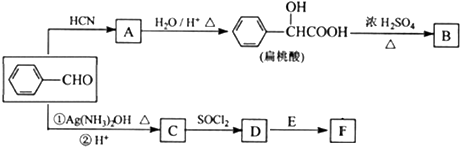

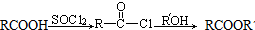 ��R��R�@����������
��R��R�@����������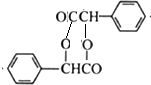 ��������C�еĺ��������ŵ��������Ȼ���
��������C�еĺ��������ŵ��������Ȼ��� ��
��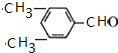 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
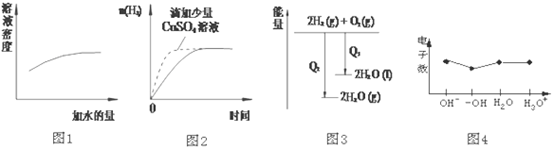
| A�� | ͼ1��ʾŨ�����ϡ�� | |
| B�� | ͼ2��ʾ�����������������п�۷�Ӧ | |
| C�� | ͼ3��ʾ������������Ӧ�е������仯 | |
| D�� | ͼ4��ʾ�������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com