
【题目】下列物品或设备:①水泥路桥、②门窗玻璃、③水晶镜片、④石英钟表、⑤玛瑙手镯、⑥硅太阳能电池、⑦光导纤维、⑧计算机芯片所用材料为SiO2或要用到SiO2的是 ( )
A.①②③④⑤⑦B.全部C.⑥⑧D.①②⑦⑧
科目:高中化学 来源: 题型:
【题目】瓷器(英文名为________)成了中华民族文化的象征之一;作为陶瓷的故乡,我国陶都________的陶器和瓷都________的瓷器,在世界上都享有盛誉.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期主族元素,分布在三个不同周期。X、Y、Z、W为这些元素形成的化合物,X为二元化合物且为强电解质,W的水溶液呈碱性,物质的转化关系如图所示。下列说法中正确的是
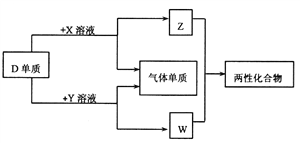
A. 离子半径:C+>D3+>B2-
B. C的单质的熔点低于D的单质的熔点
C. 电解C、E形成的化合物水溶液可生成C、E对应的单质
D. 由A、B、E形成的化合物都含有共价键,溶液都呈强酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如下图所示。A为地壳中含量仅次于氧的非金属元素的单质。
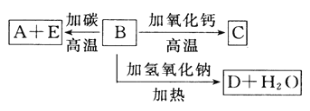
请填空:
(1)形成单质A的原子的结构示意图为______,它的最高化合价为______。
(2)B的化学式(分子式)为______,B和碳反应生成A和E的化学方程式是____________。
(3)C的化学式(分子式)为___________,D的化学式(分子式)为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜阳极泥是有色金属冶炼过程中重要的“二次资源”。其合理处理对于实现资源的综合利用具有重要意义。一种从铜阳极泥中分离提取多种金属元素的工艺流程如下:
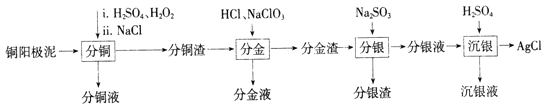
已知:分金液的主要成分为[AuCl4]-;分金渣的主要成分为AgCl和PbSO4;分银液中主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3-![]() Ag++2SO32-。
Ag++2SO32-。
(1)①“分铜”时,单质铜发生反应的化学方程式为________;反应过程中需控制适当温度,温度不宜过高或过低的原因为_______。
②已知“分铜”时 各元素的浸出率如下表所示。
Cu | Au | Ag | |
浸出率/% | 85.7 | 0 | 4.5 |
“分铜”时加入足量的NaCl的主要作用为__________
(2)“分金”时,单质金发生反应的离子方程式为___________。
(3)“沉银”时,需加入硫酸调节溶液的pH=4。已知: ![]() ,其中X表示SO32-、HSO3-或H2SO3,δ(x)与PH的关系如图所示。
,其中X表示SO32-、HSO3-或H2SO3,δ(x)与PH的关系如图所示。
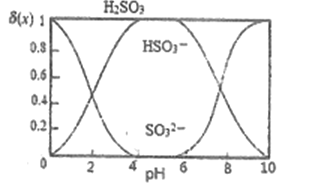
①分析能够析出AgCl的原因为_________
②调节溶液的PH不能过低,理由为__________
(4)“沉银液”加碱调至pH=8.0,Na2SO3可再生并循环利用,其再生原理为____(用离子方程式表示)。
(5)已知离子浓度≤10-5mol/L时,认为该离子沉淀完全;Ksp[Pb(OH)2]=2.5×10-16.
Ksp[Sb(OH)3])=10-41. 浸取“分银渣”可得到含0.025mol/L Pb2+的溶液( 含少量Sb3+杂质)。欲获得较纯净的Pb2+溶液,调节PH的范围为________。 (忽略溶液体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵是一种常见的强氧化剂,常用作火箭发射的推进剂。根据下列信息回答问题:
已知:①高氯酸铵受热分解为N2、Cl2、O2和H2O;②Mg3N2易水解;③Cu与N2在酒精灯加热条件下不反应。
(1)写出高氯酸铵受热分解的化学反应方程式: _____________,Mg3N2的电子式为________。
(2)现有23.5g NH4ClO4分解,用下列装置设计实验,验证其分解产物并计算分解率。(注:①装置中空气已除尽;②装置可重复使用;③B~F装置中的试剂均过量且能与相应物质反应完全。)
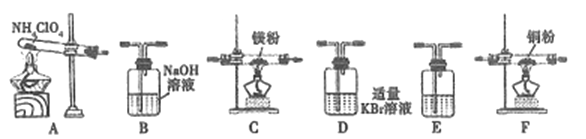
①用E装置质量的增加来验证生成的气体产物之一,则E中盛放的试剂是:_______。
②请按气流由左至右的方向连接装置:A →E→D →B→______→_____→_______→E (选择B~F装置,并用B~F字母填空)。
③证明产物中有Cl2的实验现象:________。
④反应结束后,若C装置质量增加了2.38g,则NH4ClO4的分解率是:________%。
(3)样品中NH4ClO4的含量(杂质中不含NH4+)还可用蒸馏法测定(如图所示,加热和夹持装置已略去),实验步骤如下:

步骤1:组装仪器,检查气密性;准确称取样品a g(不超过0.5g)于蒸馏烧瓶中,加入约150mL水溶解。
步骤2:准确量取40.00mL 约0.1mol/L H2SO4于锥形瓶中。
步骤3:向蒸馏烧瓶中加入20mL 3mol/L NaOH溶液;加热蒸馏使NH3全部挥发。
步骤4:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤5:向锥形瓶中加2~3滴甲基橙,用c mol/L NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1 mL。
步骤6:重复实验2~3次。
回答下列问题:
①步骤2中,准确量取40.00ml H2SO4 溶液的玻璃仪器是: __________。
②为获得样品中NH4ClO4的含量,还需补充的实验是:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A,B,C,D均含有同一种元素,A为单质,根据下图所示的物质之间的转化关系,回答下列有关问题。
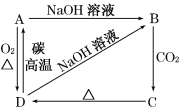
①写出A、B、C、D各物质的名称:A________,B________,C________,D_______;
②写出A→D的化学方程式:_______________。
③写出下列变化的离子方程式:
B→C______________________________;
D→B______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。回答下列问题:
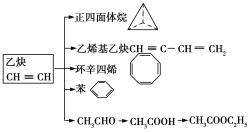
(1)正四面体烷的二氯取代产物有_____种。
A.1种 B.2种 C.3种 D.4种
(2)关于乙烯基乙炔分子的说法错误的是____(填字母符号)。
A.能使酸性KMnO4溶液褪色
B.1 mol乙烯基乙炔最多能与3 mol Br2发生加成反应
C.乙烯基乙炔分子内含有两种官能团
D.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
E.乙烯基乙炔分子中的所有原子一定都共平面
(3)环辛四烯的分子式为____,写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:_______
(4)下列属于苯的同系物的是____(填字母符号)。
A.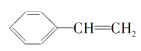 B.
B.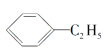
C.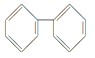 D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(N2H4)又称肼,是一种良好的火箭燃料,与适量氧化剂混合可组成液体推进剂,无水N2H4液体有微弱氨气的气味。
(1)N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7 kJ/mol,N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH2=-622 kJ/mol,试计算1 mol气态肼与二氧化氮完全反应时放出的热量为_______。
(2)在加热条件下,液态肼可还原新制的Cu(OH)2制备纳米级Cu2O,并产生无污染气体,试写出该反应的化学反应方程式_______________________________。
(3)以气态肼为原料的碱性燃料电池的总反应为N2H4+O2=N2+2H2O,放电时负极的反应方程式为______________________________
(4)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程 N2H4+H2O![]() N2H5++OH-,试写出第二步电离过程____________________________。常温下,某浓度N2H6Cl2溶液的pH为4,则该溶液中水电离出的c(H+)=_______________。
N2H5++OH-,试写出第二步电离过程____________________________。常温下,某浓度N2H6Cl2溶液的pH为4,则该溶液中水电离出的c(H+)=_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com