
【题目】在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象和结论一致且正确的是( )
A. 加入盐酸酸化的![]()
![]() 溶液产生白色沉淀,说明有
溶液产生白色沉淀,说明有![]()
![]() 存在
存在
B. 溶液呈黄绿色,且有刺激性气味,说明有![]()
![]() 分子存在
分子存在
C. 加入有色布条,一会儿有色布条褪色,说明溶液中有![]()
![]() 存在
存在
D. 加入![]()
![]() 溶液,氯水黄绿色消失,说明有
溶液,氯水黄绿色消失,说明有![]()
![]() 分子存在
分子存在
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】硫化钠在染料工业有着重要的用途。工业中常用煤粉(主要成分为碳)还原芒硝(Na2SO4)制备硫化钠。
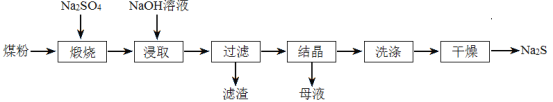
(1)①煅烧时煤粉把Na2SO4还原为Na2S,反应方程式为 。煤粉的作用是a.作为还原剂生成CO2、b. 。
②煅烧时常有副反应发生:Na2S+4CO2![]() Na2CO3+SO2+3CO
Na2CO3+SO2+3CO
4Na2S+O2![]() 2Na2S2+2Na2O
2Na2S2+2Na2O
为了控制杂质的生成可采取的措施是 。
(2)浸取用NaOH溶液而不用水的原因是 。
(3)滤渣需要用水洗涤回收,其目的是 。
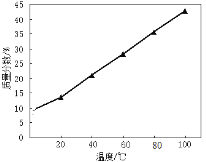
(4)随温度升高溶液中Na2S最高含量如图所示,工业上加热滤液到100 ℃以上但只蒸发到含Na2S 38%—39%,然后冷却结晶,其原因是 。
(5)干燥需要在真空中操作,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】
D是一种催眠药,F是一种香料,它们的合成路线如下:

(1)A的化学名称是______,C中含氧官能团的名称为______。
(2)F的结构简式为______,A和E生成F的反应类型为______。
(3)A生成B的化学方程式为_______________。
(4)B与乙炔钠合成C的反应类型(酸化前)是_________;写出由C合成D的第二个反应的化学方程式___________________________________。
(5)同时满足下列条件的E的同分异构体有_____种(不含立体异构)。
①遇FeCl3溶液发生显色反应; ②能发生银镜反应
(6)以乙炔和甲醛为起始原料,选用必要的无机试剂合成1,3-丁二烯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活处处有化学。下列说法不正确的是
A. 过多食用糖类(如淀粉)容易使人发胖
B. 维生素D可以促进人体对钙的吸收
C. 蛋白质仅含有碳、氢、氧三种元素
D. 硒是人体必需的微量元素,但不宜摄入过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把m mol的乙烯跟n mol H2混合于一密闭容器中,在适当条件下反应并生成p mol C2H6。若将所得的混合气体燃烧,并全部生成CO2和H2O,需要氧气的物质的量为(单位/mol) ( )
A. 3m+3p+![]()
![]() B. 3m+
B. 3m+![]()
![]() C. 3m+n D. 3m+
C. 3m+n D. 3m+![]()
![]() -2p
-2p
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)3-甲基-2-戊烯的结构简式是___________________;
(2)![]() 的系统命名为______________________;
的系统命名为______________________;
(3)键线式![]() 表示的分子式为_________________;
表示的分子式为_________________;
(4)2-溴丙烷的消去反应(化学方程式)______________________;
(5)在澄清的苯酚钠溶液中通入CO2气体,溶液浑浊,其反应方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1 mol共价键所需要吸收的能量分别为H—H:436 kJ,I—I:151 kJ,H—I:299 kJ,下列对H2(g)+I2(g) ![]() 2HI(g)的反应类型判断错误的是( )
2HI(g)的反应类型判断错误的是( )
A. 吸收能量的反应 B. 放出能量的反应
C. 氧化还原反应 D. 可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用 0.100 mol·L-1 的 NaOH 溶液滴定 10.00 mL 浓度均为 0.100 mol·L-1 的盐酸和 CH3COOH 溶液。利用传感器测得滴定过程中溶液的电导 率如图所示。下列说法正确的是( )

A. 曲线①代表滴定 HCl 溶液的曲线
B. A 点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1
C. 在相同温度下,A、B、C 三点溶液中水的电离程度:C<B=A
D. D 点溶液中:c(Cl-)=2c(OH-)-2c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com