
【题目】下列物质的电子式书写正确的是( )
A.Na2O Na ![]() [
[ ![]()
![]()
![]() ]2﹣
]2﹣
B.H2S H+[ ![]()
![]()
![]() ]2﹣H+
]2﹣H+
C.H2O2 H ![]()
![]()
![]()
![]()
![]() H
H
D.N2 N:::N
【答案】C
【解析】解:A.氧化钠为离子化合物,钠离子直接用离子符号表示,阳离子需要标出最外层电子及所带的电荷,氧化钠的电子式为: ![]() ,故A错误; B.H2S为共价化合物,硫原子中最外层有8个电子达到稳定结构,分子中存在两个H﹣S键,电子式为:
,故A错误; B.H2S为共价化合物,硫原子中最外层有8个电子达到稳定结构,分子中存在两个H﹣S键,电子式为: ![]() ,故B错误;
,故B错误;
C.双氧水为共价化合物,分子中存在两个氧氢键和一个O﹣O键,双氧水的电子式为: ![]() ,故C正确;
,故C正确;
D.氮气中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气的电子式为 ![]() ,故D错误.
,故D错误.
故选C.
A.钠离子不能合并;
B.H2S为共价化合物,硫原子中最外层有8个电子达到稳定结构;
C.双氧水中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合;
D.氮气中存在3对共用电子对,氮原子最外层达到8个电子.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】三氟化氮(NF3)是一种无色无味的气体,它是氨和氟(F2)在一定条件下直接反应得到:4NH3+3F2=NF3+3NH4F,下列有关NF3的叙述正确的是( )
A.NF3是共价化合物B.NF3的还原性比NH3强
C.NF3的氧化性比F2强D.NF3中的N呈+3价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.HClO溶于水能电离,破坏了H—O键和O—Cl键
B.CaCl2晶体中存在共价键
C.SiO2属于原子晶体,熔化破坏共价键和分子间作用力
D.NH4Cl受热分解既破坏了离子键,也破坏了共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X,Y,Z,W原子序数依次增大,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种耐高温材料,它们的关系如图所示.下列说法正确的是( ) 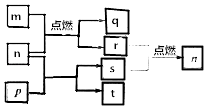
A.Y,Z,W的简单离子的电子层结构相同
B.原子半径:r(X)<r(Y)<r(Z)<r(W)
C.简单氢化物的稳定性:X>Y
D.Y与Z两种元素形成的化合物一定只含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钡(BaI22H2O)是一种白色粉末,常用于制取其他含碘化合物.一种制备流程如图1: 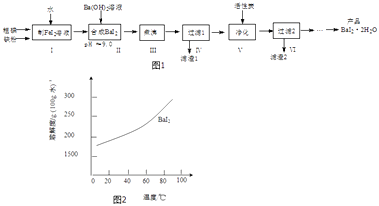
(1)步骤Ⅰ制FeI2溶液时,提高反应速率的可行措施有(填序号).
a.铁粉和碘粉用球磨机磨成细粉
b.增大n(铁粉):n(碘)的配料比
c.适当升高反应温度和搅拌速度
d.向反应器中加水至I2全部溶解
(2)步骤Ⅱ发生反应的化学方程式为;用pH试纸测定溶液pH的方法是
(3)步骤Ⅲ小心“煮沸”约20分钟,可使Fe(OH)2颗粒长大,其目的是;步骤V加入活性炭的目的是 .
(4)从过滤2所得滤液中获得BaI22H2O(溶解度曲线如图2所示)的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属的说法正确的是
A.金属原子只有还原性,金属阳离子只有氧化性 B.金属单质在常温下都是固体
C.金属阳离子被还原不一定得到金属单质 D.含金属元素的离子都是阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从含铜废料(如:覆铜板、印刷线路板及铅冰铜等)中提取铜,既可提高资源的利用率又可减少重金属污染.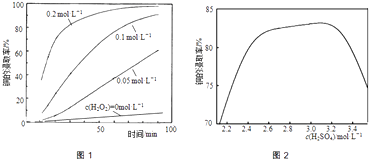
(1)废覆铜板(Cu和Sn组成)可用CuSO4和H2SO4混合溶液作电解质溶液,直接电解回收精铜,阳极上发生的电极反应为 .
(2)废印刷线路板中的铜常用含盐酸的FeCl3溶液或H2O2﹣HCl﹣NaCl混合溶液浸取回收.
①用FeCl3溶液浸取铜时发生反应的离子方程式为;若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀,产生红褐色沉淀的原因是 .
②将粉碎后的废印刷线路板放入三口烧瓶中,分别加入由0.3molL﹣1盐酸、0.5molL﹣1NaCl及不同浓度的H2O2组成的混合溶液,在温度、搅拌速率及固液比等均相同时,铜的浸取率随H2O2的浓度和时间的变化如图1所示.当c(H2O2)=0molL﹣1时,也有少量的铜被浸出,其原因是 .
③用H2O2﹣HCl﹣NaCl混合溶液浸取时,其浸取过程包括:
(Ⅰ) Cu+H2O2+2H+=Cu2++2H2O
(Ⅱ) Cu2++Cu2Cu+
(Ⅲ) Cu++nCl﹣CuCln(n﹣1)﹣
(Ⅳ) 2CuCln(n﹣1)﹣+2H++H2O2=2Cu2++2H2O+2nCl﹣
其他条件相同时,增大下列离子浓度可以加速Cu从废电路板中浸出的是(填序号).
a.Na+ b.Cu2+ c.Cl﹣d.OH﹣
(3)铅冰铜(PbS、Cu2S及FeS的混合物)可用HCl﹣H2O2混合溶液浸取.
①Cu2S被HCl﹣H2O2混合溶液浸取得到硫酸铜和氯化铜溶液的化学方程式为 .
②若由H2SO4代替HCl﹣H2O2中的HCl,其他条件相同,铜的浸取率随硫酸浓度的变化如图2所示.当H2SO4浓度大于3.1molL﹣1时,硫酸浓度越大,铜的浸取率反而越小,其原因可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的熔、沸点高低只与范德华力有关的是( )
A.Li、Na、K、PbB.HF、HCl、HBr、HI
C.LiCl、NaCl、KCl、RbClD.F2、Cl2、Br2、I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com