
【题目】下列说法不正确的是
A.Fe2O3 可用作红色颜料B.合金材料中可能含有非金属元素
C.SiO2 可用作半导体D.硅胶能吸水常用作干燥剂
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液]和FeCl3·6H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3=Cu(NH3)4Cl2]、固液分离,用盐酸溶解沉淀并制备FeCl3·6H2O。下列实验原理和装置不能达到实验目的的是
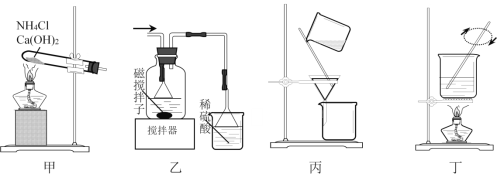
A. 用装置甲制备NH3
B. 用装置乙制备Cu(NH3)4Cl2并沉铁
C. 用装置丙分离Cu(NH3)4Cl2溶液和Fe(OH)3
D. 用装置丁将FeCl3溶液蒸干制备FeCl3·6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1) O2和O3是氧元素的两种单质。根据分子式回答。
等质量的O2和O3的物质的量之比为________,所含分子数之比为________,原子个数比为____________。
(2) NO2和N2O4是氮元素的两种常见氧化物,常温下都是气体,它们之间在常温下就能相互转化,因而经常见到的是两种气体的混合物。现取46 g该气体,所含氮原子的物质的量为________,所含氧原子个数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为: Ni(s)+4CO(g) ![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断不正确的是
A. 该反应达到平衡时,v分解[Ni(CO)4]=4v消耗(CO)
B. 第一阶段应选择稍高于42.2℃的反应温度
C. 第二阶段,230℃时Ni(CO)4分解率较高
D. 其他条件不变,增加c(CO),平衡向正向移动,反应的平衡常数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素a、b、c、d、e在周期表中的相对位置如图所示。已知a元素形成的物质种类最多。
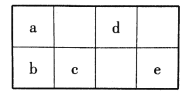
回答下列问题:
(1)在周期表中,b在元素周期表中的位置为______。
(2)b、c、e的气态氢化物热稳定性由强到弱的顺序为_____(用化学式表示)。
(3)在d的氢化物中,既含极性键又含非极性键的分子的电子式为____。
(4)a的单质在过量的d的单质气体中燃烧生成气态产物,转移1mol电子时放出的热量为98.75kJ。写出反应的热化学方程式:_______。
(5)请写出e单质与石灰乳制成漂白粉的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101kPa时,8gCH4完全燃烧生成液态水时放出的热量是445.15kJ,则CH4燃烧的热化学方程式_____________。
(2)已知:
C(s)+O2(g) = CO2(g) △H=-437.3kJ·mol -1
H2(g)+1/2O2(g) = H2O(g) △H=-285.8kJ·mol-1
CO(g)+1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1
则煤气化反应C(s)+H2O(g) = CO(g)+H2(g)的焓变△H=___ kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子中,在溶液中能大量共存的是( )
A. CO32-、S2-、NO3-、Ca2+B. Al3+、Na+、S2-、SO42-
C. Al3+、NH4+、K+、SO42-D. Fe2+、Ca2+、H+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,处理烟气中SO2常采用两种方法:液吸法和还原法。
Ⅰ.碱液吸收法
25 ℃时,Kb(NH3·H2O)=1.8×10-5;H2SO3:Ka1=1.5×10-2,Ka2=1.0×10-7;Ksp(CaSO4)=7.1×10-5。第1步:用过量的浓氨水吸收SO2,并在空气中氧化;第2步:加入石灰水,发生反应Ca2++2OH-+2NH4+ +SO42-![]() CaSO4↓+2NH3·H2O K。
CaSO4↓+2NH3·H2O K。
(1)25 ℃时,0.1 mol/L(NH4)2SO3溶液的pH____(填“>”“<”或“=”)7。
(2)计算第2步中反应的K=___________。
Ⅱ.水煤气还原法
已知:①2CO(g)+SO2(g)![]() S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1,②2H2(g)+SO2(g)
S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1,②2H2(g)+SO2(g)![]() S(l)+2H2O(g) ΔH2=+45.4 kJ/mol,③CO的燃烧热ΔH3=-283 kJ/mol。
S(l)+2H2O(g) ΔH2=+45.4 kJ/mol,③CO的燃烧热ΔH3=-283 kJ/mol。
(3)表示液态硫(S)的燃烧热的热化学方程式为_____________。
(4)反应②中,正反应活化能E1____(填“>”“<”或“=”)ΔH2。
(5)在一定压强下,发生反应①。平衡时SO2的转化率α(SO2)与投料比的比值[![]() =y]、温度T的关系如图所示。
=y]、温度T的关系如图所示。

比较平衡时CO的转化率α(CO):N____(填“>”“<”或“=”,下同)M。逆反应速率:N___P。
(6)某温度下,向10 L恒容密闭容器中充入2 mol H2、2 mol CO和2 mol SO2发生反应①、②,第5 min时达到平衡,测得混合气体中CO2、H2O(g)的物质的量分别为1.6 mol、1.8 mol。
①该温度下,反应②的平衡常数K为________。
②其他条件不变,在第7 min时缩小容器体积,α(SO2)______(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是粗盐提纯实验操作步骤,其名称为_____________(填“溶解”、“过滤”或“蒸发”),该步骤用到的玻璃仪器有:烧杯、玻璃棒和__________。实验结束后,取精盐配制成0.05L含NaCl 0.05mol 的食盐水,其浓度为___________________; 氯化钠中钠原子和氯原子之间形成的化学键属于__________(填“离子键”或“共价键”);实验室常用AgNO3来检验Cl-的存在,写出其离子方程式_____________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com