
����Ŀ����ͼ��ij�о���ѧϰС�������ȡ������������Ϊ��Ӧ������ض���Ӧ��װ�á�
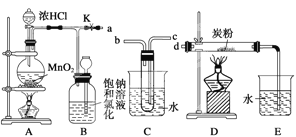
(1)Ҫ��Cװ�ý���B��D֮�䣬��ȷ�Ľӷ��ǣ�a��___��____��d��
(2)ʵ�鿪ʼ�ȵ�ȼA���ľƾ��ƣ�������K����Cl2��������װ�ã��ٵ�ȼD���ľƾ��ơ�Cl2ͨ��Cװ�ú����D��Dװ����ʢ��̿�ۣ�����������ԭ��Ӧ������CO2��HCl(g)��������Ӧ�Ļ�ѧ����ʽΪ______________________��
Ϊ��ʹCװ�÷��Ӹ��õ����ã������ձ��м���Ũ���ᣬ����Ũ�����������_____________________________________________��
(3)D����Ӧ��Ϻر�����K����ȥ�����ƾ��ƣ��������ȵ����ã�A����������Cl2 ��������ʱB�е�������____��B��������______________________��
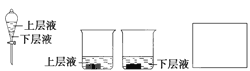
(4)����Ͳ��ȡ20 mL E����Һ�������Ѽ����ķ�Һ©���У�Ȼ����ע��10 mL CCl4���Ǻò�����(��ͼ)��������������̨�ϣ��ȷֲ��ȡ�ϲ�Һ���²�Һ���ʻ���ɫ����____(�����ϲ�Һ�������²�Һ��)����װ����ͼ��ʾ���ձ��У���ʹ��ɫ������ɫ����____(�����ϲ�Һ�������²�Һ��)��
(5)��A��B��C��D��Eװ������һ����Ҫ�Ľ���˵����Ҫ�Ľ�������______________________________,���ڷ����л����Ľ����װ��ͼ��
���𰸡�c b 2Cl2��C��2H2O![]() 4HCl��CO2 �����Ũ��������ˮ�ų��������ȣ��������Թ��е�ˮ��Ϊˮ�������Ӷ��ṩ������ˮ������D�з�Ӧ��Ҫ ƿ��Һ���½�������©����Һ������ ��������Cl2������Cl2�Ի��������Ⱦ �²�Һ �ϲ�Һ D�з�Ӧ���ɵ�HCl���弫������ˮ�������������Ľ����װ����ͼ��ʾ
4HCl��CO2 �����Ũ��������ˮ�ų��������ȣ��������Թ��е�ˮ��Ϊˮ�������Ӷ��ṩ������ˮ������D�з�Ӧ��Ҫ ƿ��Һ���½�������©����Һ������ ��������Cl2������Cl2�Ի��������Ⱦ �²�Һ �ϲ�Һ D�з�Ӧ���ɵ�HCl���弫������ˮ�������������Ľ����װ����ͼ��ʾ![]()
��������
��1������װ��D�з�Ӧ����Ӧ����C��Cl2����������CO2��HCl����Ȼ��Ӧ����ȱ��O��H����Ԫ�أ�C�����õ��ṩˮ���������ӷ�ʽӦѡ������Cl2���߸���ˮ�����ķ�ʽ������ͨ��ʢ��ˮ���Թ�ʱӦ�����̳���
��2�����ݷ�Ӧ����������������غ㶨����д��ѧ����ʽ������Ũ��������ˮ���ȵ����ʷ�����
��3���ر�����K��B�е����������࣬ѹǿ����B���������壻
��4��CCl4�ܶȴ���ˮ��������ˮ��Ӧ���ɴ��������Ư���ԣ�
��5��HCl��������ˮ���ײ�����������
��1����װ��ͼ�ж��жϣ�������B����C���뵽D�з�Ӧ������ͨ��ʢ��ˮ���Թ�ʱӦ�����̳���������ͨ��Cװ�ã��ʴ�Ϊ��c��b��
��2��������֪��ӦΪCl2��C��H2O��������ΪHCl��CO2����Ӧ�Ļ�ѧ����ʽΪ2Cl2��C��2H2O![]() 4HCl��CO2��CΪ�ṩˮ������װ�ã������Ũ��������ˮ�ų��������ȣ��������Թ��е�ˮ��Ϊˮ������
4HCl��CO2��CΪ�ṩˮ������װ�ã������Ũ��������ˮ�ų��������ȣ��������Թ��е�ˮ��Ϊˮ������
�ʴ�Ϊ��2Cl2��C��2H2O![]() 4HCl��CO2�������Ũ��������ˮ�ų��������ȣ��������Թ��е�ˮ��Ϊˮ�������Ӷ��ṩ������ˮ������D�з�Ӧ��Ҫ��
4HCl��CO2�������Ũ��������ˮ�ų��������ȣ��������Թ��е�ˮ��Ϊˮ�������Ӷ��ṩ������ˮ������D�з�Ӧ��Ҫ��
��3���ر�����K����ȥ�����ƾ��ƣ��������ȵ����ã�A����������Cl2������B�е����������࣬ѹǿ��������ƿ��Һ���½�������©����Һ�������������ж�������ֱ���ŷŵ������У�B���������������������ܷ�ֹ������Ⱦ��
�ʴ�Ϊ��ƿ��Һ���½�������©����Һ����������������Cl2������Cl2�Ի��������Ⱦ��
��4������Ͳ��ȡ20mLE����Һ�������Ѽ�������������õķ�Һ©���У�Ȼ����ע��10mLCCl4���Ǻò�������������������̨�ϣ��ȷֲ��ȡ�ϲ�Һ���²�Һ�����Ȼ�̼��ˮ�أ����������Ȼ�̼�е��ܽ��Դ���ˮ�У����Գʻ���ɫ�����²�Һ���ϲ�Ҳ�к���������ˮ��Ӧ���ɵĴ��������Ư���ԣ���ʹ��ɫ������ɫ��
�ʴ�Ϊ���²�Һ���ϲ�Һ��
��5��HCl��������ˮ���ײ�����������Ӧ�õ��õ�©�����Ľ����װ����ͼ��ʾ![]() ��
��
��D�з�Ӧ���ɵ�HCl���弫������ˮ������������![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:
![]()
��A��������ͼʾ�е�һϵ�з�Ӧ������B��C��1:2��Ӧ����Z��F��E��1:2��Ӧ����W��F�ĺ˴Ź�������ֻ�����ַ壬W��Z��Ϊͬ���칹�塣
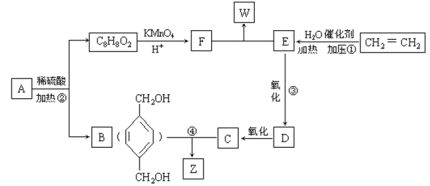
�ش��������⣺
��1��д����Ӧ����:��_____________________����______________________________��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ:
��_____________________________________________________��
��_____________________________________________________��
��3����B��Ϊͬ���칹�壬���ڷ����ұ�����ֻ������ȡ�����Ļ�������___�֣���������ӳ�칹�壩��
��4��A�Ľṹ��ʽ����Ϊ_________________________________��
��5����֪���봼�����·�Ӧ��
RCOOR����R��OH![]() RCOOR����R��OH(R��R����R����������)
RCOOR����R��OH(R��R����R����������)
B��W�����������¿��γɸ߷��ӻ�����Q����д��B��W����Q�Ļ�ѧ����ʽ________��
��6��ͬһ̼ԭ�����������ǻ�ʱ�ṹ���ȶ�������ˮ����ȩ��ͪ��
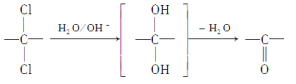
��������֪ʶ����������Ϣ��д���ԶԶ��ױ�Ϊԭ��(�������Լ���ѡ)�Ʊ�![]() �ĺϳ�·�ߡ�__________________
�ĺϳ�·�ߡ�__________________
�ϳ�·��ʾ��ͼ���磺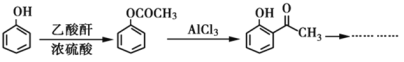
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ���У���Һ�������Ϊ250mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.10mol/L������һ��ʱ���õ����Ͼ�ͨ��0.02mol���ӣ�����������Һ����ı仯��������������ȷ���ǣ� ��
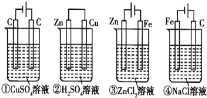
A. ����һ��ʱ�����Һ��Ũ�ȣ���=��=��=��
B. ����һ��ʱ�����Һ��pH���ܣ��ۣ��٣���
C. �����������������ܣ��ۣ��٣���
D. �缫������������������٣��ڣ��ۣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܽ�����п�̻���ȡ�ߴ�п�Ĺ���������ͼ��ʾ���ܽ�������п�̻���п��ͭ���ӡ���Ԫ�طֱ���Zn(NH3)42+��Cu(NH3)42+��Cd(NH3)42+��AsCl52������ʽ���ڡ�
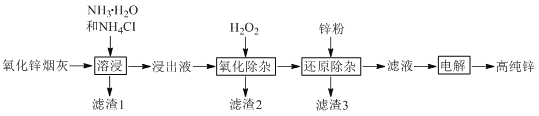
ע�����������ӡ��У�AsCl52��ת��ΪAs2O5���������۳���ȥ����Һʼ�սӽ����ԡ�
�ش��������⣺
��1��Zn(NH3)42+��Zn�Ļ��ϼ�Ϊ________�����ܽ�����ZnO������Ӧ�����ӷ���ʽΪ________��
��2��п���������¶ȵĹ�ϵ��ͼ��ʾ������30 ��ʱп��������ߵ�ԭ��Ϊ________��
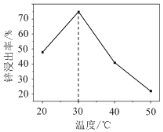
��3��������3������Ҫ�ɷ�Ϊ________��
��4������⡱ʱZn(NH3)42+�������ŵ�ĵ缫��ӦʽΪ_______���������ų�һ����ɫ��ζ�����壬����ͨ�����KSCN��FeCl2��Һ�У�����������������________��д��ѧʽ��������ĵ��Һ������________��дһ�����ʵĻ�ѧʽ����ɷ��ء��ܽ����������ʹ�á�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��17.4g MnO2��240 mL 10 mol/L(�ܶ�Ϊ1.10g/mL)������(����)��ϼ���(����������ӷ�)��ʹ���ַ�Ӧ��������Һ�м���������AgNO3��Һ������֪��MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
����(1)10 mol/L���������������____________
(2)�����������ڱ�״���µ����______________��
(3)��������������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)1 mol CO2�к���________mol C��________mol O��
(2)1.80 mol CO2�к���________��CO2���ӣ�________��Cԭ�ӣ�________��Oԭ�ӣ�
(3)3.60 mol CO2������CO2��������________��H2O������Ŀ��ȣ�8.40��1026��O3���ӵ����ʵ�����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(BN)�����ж�����ṹ�������൪������ͨ�����ڵ��ȶ��࣬��ʯī���ƣ����в�״�ṹ�������������������൪�����dz�Ӳ���ϣ����������ĥ�ԡ����ǵľ���ṹ��ͼ��ʾ�����������־����˵������ȷ����
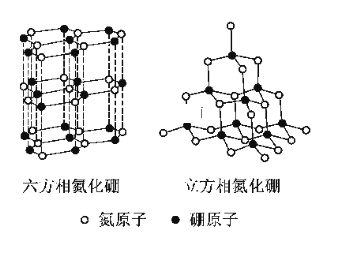
A. �����൪����������������������Ӳ�ȴ�
B. �����൪������������С�������ʵ���
C. ���־����е�Bԭ�ӵ��ӻ�������ͬ
D. ���־����Ϊ���Ӿ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ڣ�100 ��ĵ����ºϳ�һ����X���˷��ӵĽṹ��ͼ��ʾ��ͼ�е����߱�ʾ��ѧ����������˵����ȷ����
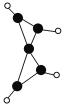
A. X����ʹ������Ȼ�̼��Һ��ɫ������ʹ����KMnO4��Һ��ɫ
B. X��һ�ֳ��������ȶ����ڵ�Һ̬��
C. X���������ƣ�������ȡ����Ӧ
D. ���ȼ�յ�������X�ͼ��飬�������������϶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������˵����ȷ����
A. 2.3gNa�������������г��ȼ�գ�ת�Ƶĵ�����Ϊ0.2NA
B. ��״���£�22.4 Lˮ�к��е���ԭ����ΪNA
C. 1L 0.5molL��1��AlCl3��Һ������Cl��ĿΪ3NA
D. 0.1 mol ���������е�ԭ����Ϊ0.2NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com