
| A、硫化钠 | B、硫酸 |
| C、过氧化钠 | D、氢氧化钠 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
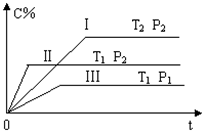 在一固定容积的密闭容器中充入气体A和B,发生如下可逆反应:
在一固定容积的密闭容器中充入气体A和B,发生如下可逆反应:| A、T1>T2,Q<0 |
| B、T1<T2,Q>0 |
| C、P1>P2,x=1 |
| D、P1<P2,x≠1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2C1- |
| B、金属钠投入水中Na+H2O=Na++OH-+H2↑ |
| C、氢氧化亚铁溶于稀硝酸Fe(OH)2+2H+=Fe2++2H2O |
| D、氯化铁溶液中加过量氨水3NH3?H2O+Fe3+=3NH4++Fe(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熔点、沸点:F2>Cl2>Br2>I2 |
| B、离子半径:F->Na+>Mg2+>Al3+ |
| C、碱性:LiOH>NaOH>KOH>RbOH |
| D、Na2CO3水溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com