
【题目】根据题目填空:
(1)间甲基苯乙烯的结构简式;
(2)提纯粗苯甲酸,常用的方法是;
(3)相同质量的乙醇、乙烯、乙炔完全燃烧后,生成CO2最多的是 .
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
【题目】铜锌原电池的装置如图所示,下列叙述不正确的是( ) 
A.锌片为负极,稀硫酸是电解质溶液
B.电池工作时电子由锌片经导线流向铜片
C.电池工作时铜片逐渐溶解而质量减轻
D.电池工作时实现了化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 甲同学设计实验探究碳、硅元素的非金属性的相对强弱,实验装置如图。根据要求完成下列各题。
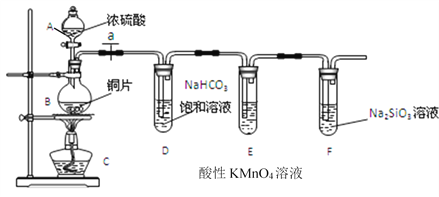
(1)填写所示仪器名称:A__________。
(2)实验步骤:连接仪器、______________、加药品后,打开 a、滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是________________________________;
装置E中酸性KMnO4溶液的作用是_____________________________;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是__________________。
③依据试管 D 中的反应,能否证明S的非金属性强于C的非金属性___(填 “能”或“否”)。
Ⅱ.将等质量的锌片和铜片用导线相连并插入500 mL CuSO4溶液中构成如图所示的装置。

(1)该装置中能量主要的转化形式是__________,铜片周围溶液会出现________的现象。
(2)若锌2 min后的质量减少1.3 g,则导线中流过的电子为_______mol。
(3)若将装置的锌片换为石墨棒,电解质溶液换为FeCl3溶液,其正极反应为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=l.1×10-12以及Ksp[Cu(OH)2] =2×10-20。下列说法错误的是
A. 常温下AgCl饱和溶液和Ag2CrO4饱和溶液的物质的量浓度比较:c(AgCl)<c(Ag2CrO4)
B. 常温下,在0.010molL-1的AgNO3溶液中,AgCl与Ag2CrO4分别能达到的最大物质的量浓度比较:c(AgCl)<c(Ag2CrO4)
C. 某CuSO4溶液里c(Cu2+)=0.02 molL-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于5
D. 要使0.2molL-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液PH为6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号内试剂除去下列各物质中的少量杂质,不正确的是
A.乙烷中的乙烯(Br2水)B.溴苯中的溴(KI溶液)
C.乙醇中的水(CaO)D.乙酸乙酯中的乙酸(饱和Na2CO3溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于生物体内有机化合物所含元素的叙述,错误的是( )
A. 叶绿素含有镁元素,血红蛋白含有铁元素
B. 脱氧核糖和ATP均含有磷元素
C. 甲状腺激素含有碘元素,不能为细胞供能
D. 胰岛素含有氮元素,能调节生命活动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应的描述正确的是
A. NaHSO4溶液与Ba(OH)2溶液混合后显中性:Ba2++2OH-+2H++SO![]() ===BaSO4↓+2H2O
===BaSO4↓+2H2O
B. 向Fe2(SO4)3溶液中通入足量Na2S溶液:2Fe3++S2-===2Fe2++S↓
C. 强碱溶液中,用次氯酸钠与Fe(OH)2反应是湿法制备高铁酸钠的最主要过程,可表示为:2ClO-+Fe(OH)2===FeO42—+2Cl-+2H+
D. 将少量二氧化碳通入次氯酸钠溶液中:CO2+H2O+2ClO-===CO32—+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:
下列说法不正确的是
A. 滤液A中的阳离子为Fe2+、H+
B. 样品中铁元素的质量为2.24 g
C. 样品中CuO的质量为4.0 g
D. V=448 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述正确的是( ) 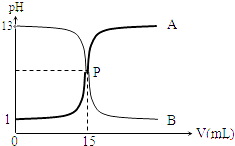
A.盐酸的物质的量浓度为1molL
B.P点时反应恰好完全,溶液呈中性
C.曲线a是盐酸滴定氢氧化钠的滴定曲线
D.酚酞不能用作本实验的指示剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com