
【题目】芳香族化合物A(C9H12O)可用于医药及香料的合成,A有如下转化关系:

已知信息:
①A不能使酸性高锰酸钾溶液褪色;
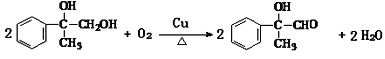
② ;
;
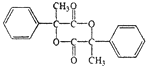
③![]()
回答下列向题:
(1)B→D与H→I的反应类型分别为:_________、_________。
(2)K所含官能闭的名称为___________,B的结构简式为____________。
(3)由E生成F的反应方程式为___________________________。
(4)J为一种具有3个六元环的酯,则其结构简式为_________________。
(5)F的同分异构体中,能与NaHCO3反应生成CO2,且核磁共振氢谱为4组峰,且峰面积比为6:2:1:1的结构有_________种。
(6)糖叉丙酮(![]() )是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁基氯[(CH3)3CCl]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁基氯[(CH3)3CCl]和糠醛(  )为原料制备糖叉丙酮的合成路线(无机试剂任用) _______。合成流程图示例如下:
)为原料制备糖叉丙酮的合成路线(无机试剂任用) _______。合成流程图示例如下:
【答案】 加成反应 缩聚反应 羰基、碳碳双键 ![]()
 2
2 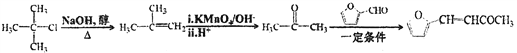
【解析】由题中信息可知,A为芳香醇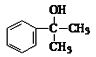 ,A发生消去反应后生成B,B为
,A发生消去反应后生成B,B为![]() ,B与溴发生加成反应生成二溴代烃D,D发生水解生成E,E为
,B与溴发生加成反应生成二溴代烃D,D发生水解生成E,E为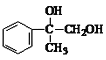 ,E发生催化氧化生成F,F为
,E发生催化氧化生成F,F为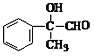 ,F发生银镜反应、酸化后得到H,H为
,F发生银镜反应、酸化后得到H,H为 ,H发生缩聚反应生成聚酯I,H发生酯化反应生成环酯J,J为
,H发生缩聚反应生成聚酯I,H发生酯化反应生成环酯J,J为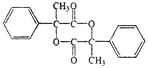 。由题中信息②和③可知,C为
。由题中信息②和③可知,C为![]() 、K为
、K为![]() 。
。
(1)B→D与H→I的反应类型分别为加成反应和缩聚反应。
(2)K所含官能闭的名称为羰基、碳碳双键,B的结构简式为![]() 。
。
(3)由E生成F的反应方程式为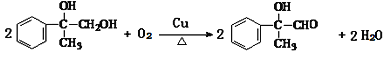 。
。
(4)J为一种具有3个六元环的酯,则其结构简式为 。
。
(5)F( )的同分异构体中,能与NaHCO3反应生成CO2,说明分子中有羧基,且核磁共振氢谱为4组峰、峰面积比为6:2:1:1的结构有2,6-二甲基苯甲酸和3,5-二甲基苯甲酸,共2种。
)的同分异构体中,能与NaHCO3反应生成CO2,说明分子中有羧基,且核磁共振氢谱为4组峰、峰面积比为6:2:1:1的结构有2,6-二甲基苯甲酸和3,5-二甲基苯甲酸,共2种。
(6)参考上述合成路线,由叔丁基氯[(CH3)3CCl]和糠醛( 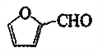 )为原料制备糖叉丙酮,可以先由叔丁基氯水解制备甲基丙烯,然后根据信息②的反应,甲基丙烯经酸性高锰酸钾溶液氧化、酸化后得到丙酮,最后再根据信息③的反应,丙酮与糠醛发生反应得到目标产品。具体合成路线如下 :
)为原料制备糖叉丙酮,可以先由叔丁基氯水解制备甲基丙烯,然后根据信息②的反应,甲基丙烯经酸性高锰酸钾溶液氧化、酸化后得到丙酮,最后再根据信息③的反应,丙酮与糠醛发生反应得到目标产品。具体合成路线如下 :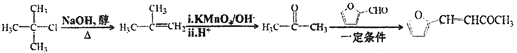 。
。


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说祛正确的是
A. 24gMg与足量N2反应生成Mg3N2,转移的电子数为6NA
B. lmolNa218O2中所含的中子数为42NA
C. 9.8g由H2SO4和H3PO4组成的混合物中含有的氧原子数为0.4NA
D. 1mol环已烷中含有的共价键数为12NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,H3AsO4溶液中各含砷粒子分布分数(平衡时该粒子的浓度与各含砷粒子浓度之和的比)与pH的关系如右图所示。下列说法正确的是
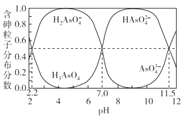
A. H3AsO4的第一步电离常数Ka1>0.01
B. pH=7.0时.溶液中c(AsO43-)=c(H3AsO4)=0
C. 0.1mol·L-1H3AsO4溶液的pH<2
D. pH=12时,c(H+)=3c(AsO43-)+2c(HAsO42-)+c(H2AsO4-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组对一种废旧合金(含有Cu、Fe、Si等元素)进行分离、回收再利用,所设计工艺流程如下。
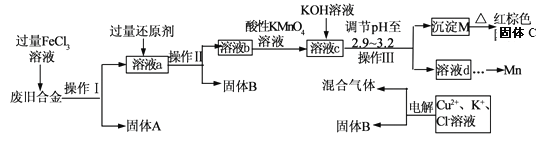
已知:298K时,Ksp[Fe(OH)3]=4.0×10—38,Ksp[Cu(OH)2]=2.2×10一20,
Ksp[Mn(OH)2]=1.9×10—13
回答下列问题:
(1)操作I、Ⅱ、Ⅲ为________,固体B为_________ (填化学式)。
(2)加人过量FeCl3溶液过程中与较不活泼的金属反应的离子方程式__________________。
(3)调节pH至2.9~3.2的目的是分离_________ (填离子符号)
(4)①向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为_________________。
②若用 a mol/LKMnO4溶液处理溶液b,当恰好反应时消耗KMnO4溶液V mL,所得红棕色固体C的物质的量为_________(用含a、v的代数式表示)
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,最后生成的沉淀为_________ (填化学式)。
(6)用惰性电极电解时阳极产生标准状况下的气体6.72L,阴极得到的电子数为0.8NA,则生成氧气的物质的量为________ mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是

A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是
A. 2 mol水的摩尔质量和1 mol水的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 标准状况下,22.4 L一氧化碳中氧原子数和16 g二氧化硫中氧原子数
D. 2 mol·L-1H2SO4溶液中的H+个数与1 mol·L-1HCl溶液中的H+个数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl = NaCl + H2O, B.2FeCl3 + Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A.__________B.____________。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是_________(填“锌”或“铜”);
②正极的电极反应式为__________________________________;
③产生这些气体共需转移电子_________________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com