
【题目】某同学用某化合物X(两种短周期元素组成的纯净物)进行了如下实验:

实验步骤②中还观测到生成黑色固体和无色无味气体,生成的溶液可作为建筑行业的一种黏合剂。
请回答:
(1)X的化学式是____,步骤①的离子方程式是___。
(2)步骤②的化学方程式是_____。
【答案】Mg2Si Mg2Si +4H+=SiH4↑+2Mg2+ SiH4 +2KMnO4=2MnO2↓+Na2SiO3+H2↑+H2O
【解析】
短周期元素形成的化合物中,与过量烧碱溶液生成白色沉淀,则灼烧后得到白色固体的为MgO,4.0g白色固体可得X中0.1molMg原子,无色气体A与高锰酸钾可生成黏合剂硅酸钾溶液,可知无色气体A具有还原性且含有Si元素,据此分析作答。
(1)根据化合物X 7.20g计算得到Mg原子与Si原子个数之比为2:1,则X的化学式为Mg2Si,在盐酸作用下会生成硅烷气体与氯化镁,故其离子方程式为:Mg2Si +4H+=SiH4↑+2Mg2+,故答案为:Mg2Si;Mg2Si +4H+=SiH4↑+2Mg2+;
(2)在强氧化剂高锰酸钠的作用下,硅烷被氧化为硅酸钠与氢气,同时生成黑色固体二氧化锰,根据氧化还原反应得失电子守恒与元素守恒可得,其化学方程式为:SiH4 +2KMnO4=2MnO2↓+K2SiO3+H2↑+H2O。


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述正确的是
A. 通常状况下,NA个Cl2分子的质量是71g
B. 通常状况下,NA个C02分子的体积约是22.4L
C. 0.1 mol/L的H2S04溶液中H+的个数是0.2NA
D. 若lg N2含有m个分子,则NA=m/28
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知75mL2mol∕L NaOH溶液的质量为80g,计算溶液中NaOH的质量分数。___
(2)乙酸是实验室常用的一种化学试剂,某乙酸试剂瓶上标签的部分内容如图所示。利用标签提供的信息,回答下列问题:
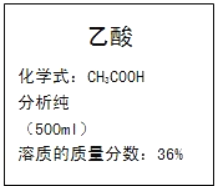
①乙酸的摩尔质量为___。
②若该乙酸溶液的密度为1.02g/cm3,求此乙酸溶液的物质的量浓度。___
③某实验中要用2mol·L-1的乙酸溶液306ml,需要取用上述乙酸溶液多少毫升?___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用质量分数为36.5%的盐酸(密度为1.20g/㎝3)配制480mL1.0mol/LHCl。回答下列问题:
(1)此浓盐酸的物质的量浓度是________________
(2)配制时,必要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、____________________。该试验中两次用到玻璃棒,其作用分别是 ___________________,________________________。
(3)若实验遇下列情况,溶液的浓度偏高的是 __________________________________________
A.量取浓盐酸时仰视量筒刻度
B.摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C.定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
E.未冷却到室温就定容
(4)若取50.0mL上述已配好的溶液,与另一150mL0.2mol/L的HCl溶液混合,最后得到的溶液的物质的量浓度为_________________(设溶液的体积变化可忽略)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性,高效催化性等优良的性质。资料显示:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570℃时生成FeO,高于570℃时生成Fe3O4。如下两个装置可在不同温度下进行该反应并验证产物。
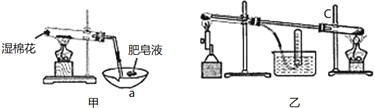
(1)甲装置中仪器a的名称为_____。
(2)装置甲验证气体产物的操作是____。装置C的作用是____。
(3)A同学取出少量乙装置中实验结束后的固体物质于另一试管中,加入少量盐酸,微热,观察到黑色粉末逐渐溶解,溶液呈浅绿色,有少量气泡产生。再向溶液中滴加几滴KSCN溶液,震荡,溶液没有出现红色,推断该条件下生成FeO,B同学却不同意该结论,他的理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水蒸气通过的灼热的焦炭后,流出气体的主要成分是 CO 和 H2,还有 CO2和水蒸气等。现利用下图中提供实验装置,证明上述混合气体中有CO 和 H2。(A中加热装置在图中略去)回答下列问题:
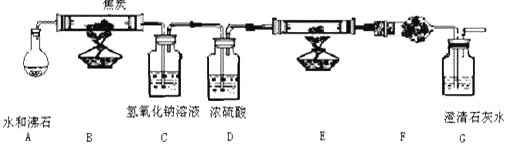
(1) C装置的用途是____________
(2)仪器 E 中需加入的试剂是_____________
(3)仪器 F 中需加入的试剂是:______,其目的是_________________
(4)装置F和G的位置能否颠倒_____,(填“能”或“否”)理由是____________________
(5)能证明混合气中含有 CO 的实验现象是________________________
(6)有人认为该实验装置存在一个缺陷,你认为这个缺陷是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃以某种比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L。下列各组混合烃中不符合此条件的是
A. CH4、C2H4 B. CH4、C3H6 C. C2H4、C3H4 D. C2H2、C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝诺酯是一种新型抗炎、解热、镇痛药,其结构如下所示。下列对该化合物叙述正确的是

A. 贝诺酯分子式为![]()
B. 贝诺酯属于芳香烃
C. 贝诺酯属于高分子化合物
D. 已知贝诺酯的水解产物之一为对氨基乙酰酚( ),在核磁共振氢谱中,对氨基乙酰酚有5种峰
),在核磁共振氢谱中,对氨基乙酰酚有5种峰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)在标准状况下,V L H2 中含有 N 个氢分子,则阿伏加德罗常数为_____mol-1
(2)8.5 g氢氧根离子含有的电子数目为________。
(3)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D;现将16 g A与70 g B混合,充分反应后,生成2 mol D和一定量的C,则D的相对分子质量为_________。
(4)标准状况下,8.96L的CH4和CO的混合气体,该混合气体对氢气的相对密度是9.5,则混合气体平均摩尔质量为____________,混合气体中CH4与CO的体积比为____。
(5)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为________mol/L。(用带字母的表达式回答)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com