
����Ŀ������������ݻ���Ϊ1L�ĺ��������У��ֱ����2moLA��2molB��1molA��1molB����ͬ�����£��������з�Ӧ��A��g����B��g��![]() xC��g����H��0�������������c��A����ʱ��t�ı仯��ͼ��ʾ������˵����ȷ����
xC��g����H��0�������������c��A����ʱ��t�ı仯��ͼ��ʾ������˵����ȷ����
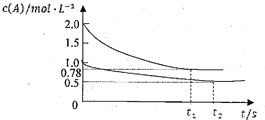
A.x���ܵ���2Ҳ���ܵ���3
B.��ƽ�����������г��뺤����ʹc��A������
C.����������ٳ���2molA��2molB����ƽ��ʱ��������0.78mol��L��1��c��A����1.56mol��L��1
D.���������������¿�ʹ�������ڸ����ʵ����������������ڵ���ͬ
���𰸡�C
��������
A.��ͼ���֪ƽ��ʱ��������ƽ��ʱ��A��ת����Ϊ![]() =61%����������A��ת����Ϊ
=61%����������A��ת����Ϊ![]() =50%����������ѹǿ���������ڴ�����ѹǿƽ�����������С�ķ����ƶ����ʣ�1+1��x������x=1��������������֪x=1����x=2����Ӧǰ������������䣬�ס���Ϊ��Чƽ�⣬ת������ȣ���A����
=50%����������ѹǿ���������ڴ�����ѹǿƽ�����������С�ķ����ƶ����ʣ�1+1��x������x=1��������������֪x=1����x=2����Ӧǰ������������䣬�ס���Ϊ��Чƽ�⣬ת������ȣ���A����
B.��ƽ�����������г��뺤����������ѹǿ��Ȼ����ƽ�ⲻ�ƶ�����Ӧ��������ֵ�Ũ�Ȳ��䣬��B����
C.����������ٳ���2molA��2molB�����Ե�ЧΪԭƽ��״̬��ѹǿ����һ����ƽ��������Ӧ�����ƶ���Aת������������ƽ��ʱ��������c(A)С��2��ԭƽ���е�c(A)��ƽ���ƶ�Ŀ���ǽ���Ũ���������ƣ���������ȫ����Ũ�������Ӱ�죬����ƽ��ʱŨ�ȱ�ԭƽ�������ƽ��ʱ��������0.78mol/L��c(A)��1.56mol/L����C��ȷ��
D.�÷�ӦΪ���ȷ�Ӧ�����������������£�ƽ�������ȷ�Ӧ�����ƶ��������淴Ӧ�����ƶ���A��ת���ʱȼ�������ת���ʵͣ�������ʹ�������ڸ����ʵ����������������ڵ���ͬ����D����
��ѡC��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH=11��X��Y���ּ���Һ��10mL���ֱ�ϡ����1000mL����pH����Һ�����V���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��

A. X��Y���ּ�����ʵ���Ũ��һ�����
B. ϡ�ͺ�X��Һ���Ա�Y��Һ����ǿ
C. ��9��a��11����X��Y��������
D. ��ȫ�к�X��Y����Һʱ������ͬŨ����������VX��VY
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2CO(g)��O2(g)=2CO2(g)����H����566 kJ/mol��Na2O2(s)��CO2(g)=Na2CO3(s)��![]() O2(g)����H����226 kJ/mol�����������Ȼ�ѧ����ʽ�ж�����˵����ȷ����( ��)
O2(g)����H����226 kJ/mol�����������Ȼ�ѧ����ʽ�ж�����˵����ȷ����( ��)

A.CO��ȼ����Ϊ283 kJ
B.��ͼ��ʾΪCO����CO2�ķ�Ӧ���̺������Ĺ�ϵ
C.2Na2O2(s)��2CO2(s) =2Na2CO3(s)��O2(g)��H>��452 kJ/mol
D.CO(g)��Na2O2(s)��Ӧ�ų�509 kJ����ʱ��ת�Ƶ�����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(s)+3B(g)![]() 2C(g)+2D(g)�������ֲ�ͬ������ò�ͬ���ʱ�ʾ�ķ�Ӧ���ʷֱ����£����з�Ӧ����������( )
2C(g)+2D(g)�������ֲ�ͬ������ò�ͬ���ʱ�ʾ�ķ�Ӧ���ʷֱ����£����з�Ӧ����������( )
A.v(C)=0.02mol��(L��s)-1B.v(B)=0.06mol��(L��min)-1
C.v(A)=1.5mol��(L��min)-1D.v(D)=0.01mol��(L��s)-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ǵ�ͳ�в�ҩ���˵���Ч�ɷ�֮һ��������ϸ����ɱ���ж������á������йغ������ص�������ȷ���ǣ� ��
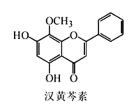
A.�������صķ���ʽΪC16H13O5
B.����������Na2CO3��Һ��Ӧ����FeCl3��Һ��ɫ
C.1mol����������ˮ��Ӧ������2molBr2�����ӳɷ�Ӧ
D.������H2�����ӳɷ�Ӧ�÷����й����ŵ��������1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��6��6�գ����Ų���ʽ���Ĵ���Ӫ�̰䷢��5G�������գ���ʾ���ҹ�5GԪ�����㡣ͨ����������﮵���������С�������ᡢ��������ͻ�����ɸ߱��ʳ�ŵ硢��ɫ�������ڶ��ŵ㡣������﮵�������������Ϊ�������ϵ�һ������Ӷ��ε�أ��ŵ�ʱ��������ӦʽΪM1��xFexPO4+e-+Li��=LiM1��x FexPO4����ԭ����ͼ��ʾ������˵����ȷ���ǣ� ��
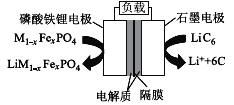
A.�ŵ�ʱ��������ʯī�缫����������﮵缫
B.����ܷ�ӦΪM1��xFexPO4+LiC6![]() Li M1��xFexPO4+6C
Li M1��xFexPO4+6C
C.�ŵ�ʱ��������ӦʽΪLiC6-e-=Li��+6C
D.���ʱ��Li������������﮵缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�����������еĽ��Ͳ��������ǣ� ��
ѡ�� | �������ʵ | ���� |
A | ��ϩͨ��������Ȼ�̼��Һ��������Ȼ�̼��Һ�Ⱥ�ɫ��ɫ | ��ϩ�����Ȼ�̼��Һ�е��巢���ӳɷ�Ӧ��������ɫ��1,2-�������� |
B | ���ִ�����ຸ�Ӵ���п�飬����Ч�������������ں�ˮ�еĸ�ʴ���� | п�����ں�ˮ�й���ԭ��أ�п�������ṩ���ӣ��Ӷ������˸��� |
C | ������ʯ�������������У���Ӧ����������������ӿ������ | ��ʼ�η�Ӧ���ȣ���Һ�¶����ߣ����ڷ�Ӧ���ȣ���Һ�¶��½� |
D | ��AgNO3��Һ�м������NaCl��Һ�����ú����ϲ���Һ���Լ�Ag+ | Ag+��Cl-�ij�����ӦΪ���淴Ӧ���ܷ�Ӧ����Լ��Ag+������ȫ���� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����⣨PH3����һ�־綾���壬�dz��õĸ�ЧѬ��ɱ�����Ҳ��һ�ֵ��ӹ�ҵԭ�ϣ�
��1�����ܱ����ַ��õ�������AIP��Ƭ������ˮ�����ų�PH3���壬��ѧ����ʽΪ ______
��2�����÷�ӦPH3+3HgCl2=P(HgCl)3��+3HCl��ͨ���ⶨ��Һ ______ �仯����ȷ�ⶨ����������PH3������HgCl2����ˮ��������Һ���������磬��HgCl2���� ______ �����������������������������
��3����ҵ�Ʊ�PH3��������ͼ1��ʾ��

������������ ______ Ԫ�
������ӦI���ɵ�n��NaH2PO2����n��Na2HPO3��=3��1ʱ���μӷ�Ӧ��n��P4����n��NaOH��= ______ ��
��4����Ư�ۿɽ�PH3����ΪH3PO4����ѧ����ʽΪ ______ ������ˮ����ʱ�ɼӿ�PH3���������̣������ӷ���ʽ��ʾԭ�� ______ ��
��5���ӣ�4���еķ�Ӧ�����л���������ƣ�CaHPO4���ķ�����ͼ2��

���Լ�XΪ ______ ���ѧʽ����
����֪25��ʱ��H3PO4��Ka1=7.5��10-3��Ka2=6.3��10-8��Ka3=4.4��10-13��
CaHPO4����ҺpH ______ 7��������������=��������������ͨ������˵������ ______ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���仯����㷺��������Ȼ�硣��ش��������⣺
��1����Ӧ��Fe(s)+CO2(g)![]() FeO(s)+CO(g) ��H1 ƽ�ⳣ��ΪK1
FeO(s)+CO(g) ��H1 ƽ�ⳣ��ΪK1
��Ӧ��Fe(s)+H2O(g)![]() FeO(s)+H2(g) ��H1 ƽ�ⳣ��ΪK2
FeO(s)+H2(g) ��H1 ƽ�ⳣ��ΪK2
��ͬ�¶��£�K1��K2��ֵ���±���

���з�Ӧ��H2(g)+CO2(g)![]() CO(g)+H2O(g)������ϱ����ݣ���Ӧ����___(����ȡ������ȡ�����Ӧ��Ϊ���CO2��ת���ʿɲ��ô�ʩ��___��д��������������
CO(g)+H2O(g)������ϱ����ݣ���Ӧ����___(����ȡ������ȡ�����Ӧ��Ϊ���CO2��ת���ʿɲ��ô�ʩ��___��д��������������
(2)��֪CO2������ϳ��Ҵ��ķ�Ӧԭ��Ϊ��2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) H<0����mΪ��ʼʱ��Ͷ�ϱȣ���m= n(H2)/ n(CO2)��
C2H5OH(g)+3H2O(g) H<0����mΪ��ʼʱ��Ͷ�ϱȣ���m= n(H2)/ n(CO2)��

��ͼ1��Ͷ�ϱ���ͬ���¶ȴӸߵ��͵�˳��Ϊ______��
��ͼ2��m1��m2��m3�Ӵ�С��˳��Ϊ____��
��ͼ3��ʾ����ѹΪ5MPa�ĺ�ѹ�����£���m=3ʱ��ƽ��״̬ʱ�����ʵ����ʵ����������¶ȵĹ�ϵ��������d���������ʻ�ѧ����Ϊ____��T4�¶�ʱ���÷�Ӧƽ�ⳣ��KP�ļ���ʽΪ____��
��3����ҵ�ϳ��ø�Ũ�ȵ� K2CO3��Һ����CO2������ҺX�������õ�ⷨʹK2CO3��Һ��������װ��ʾ��ͼ��ͼ��

���������������ķ�Ӧ����____��H++HCO3- ==CO2��+H2O
�ڼ���CO32-��������������ԭ����____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com