
����Ŀ��һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M(g)��N(g)�����ʵ����淴Ӧʱ��仯��������ͼ����ͼ��ʾ��
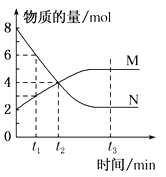
��1����ͼ���������ķ�Ӧ�Ļ�ѧ����ʽ��______________��
��2����ͼ����ʾ������ʱ���У�_______����t1��t2��t3��ʱ�̴���ƽ��״̬����ʱv��____v������>��<��=����
��3��������������˵��������Ӧ�ﵽƽ��״̬����_______��
A.������M��N�����ʵ���֮��Ϊ1��l
B�����������ܶȲ���ʱ��ı仯���仯
C���������������ʵ�������ʱ��ı仯���仯
D����λʱ��������2molN��ͬʱ����ImolM
��4�����д�ʩ������Ӧ���ʵ���_______��ѡ����ĸ��
A�������¶� B������ѹǿ C����СM��Ũ�� D������Ӧ���������С
���𰸡� 2N(g)![]() M(g) t3 = C AD
M(g) t3 = C AD
����������1����ͼ��֪��Ӧ���� t2ʱ��N����8mol-4mol=4mol��M����4mol-2mol=2mol��NΪ��Ӧ�MΪ������ұ仯��֮��Ϊ2��1������ѧ������֮��Ϊ2��1����˷���ʽΪ2N(g)![]() M(g)����2�������ʵ�����ʱ��ı仯���������仯ʱΪƽ��״̬����ͼ��֪��t3Ϊƽ��״̬����ƽ��ʱ���淴Ӧ������ȣ���3��A����ͼ��֪t2ʱM��N�����ʵ���֮��Ϊ1��1������ʱ��ı仯�����ǵ����ʵ����ڱ仯������ƽ��״̬��A����B�������������������һֱ���䣬���ܶ�ʼ�ղ��䣬������Ϊ�ж�ƽ������ݣ�B����C����÷�Ӧ�����ʵ����ڼ��ٵĻ�ѧ��Ӧ����������������ʵ�������ʱ��ı仯���仯���ﵽƽ��״̬��C��ȷ��D����λʱ��������2molN��ͬʱ����1molM��ֻ��˵��������N��M�Ĺ�ϵ������˵�����淴Ӧ���ʵĹ�ϵ��D����ѡC����4��A�������¶�������Ӧ���ʣ�A��ȷ��B������ѹǿ�ܼ�С��ѧ��Ӧ���ʣ�B����C����СM��Ũ�ȣ���ѧ��Ӧ������Ӧ�����ƶ�������Ӧ���ʼ�С��C����D������Ӧ���������С������ڼ�ѹ����������Ӧ���ʣ�D��ȷ����ѡAD��
M(g)����2�������ʵ�����ʱ��ı仯���������仯ʱΪƽ��״̬����ͼ��֪��t3Ϊƽ��״̬����ƽ��ʱ���淴Ӧ������ȣ���3��A����ͼ��֪t2ʱM��N�����ʵ���֮��Ϊ1��1������ʱ��ı仯�����ǵ����ʵ����ڱ仯������ƽ��״̬��A����B�������������������һֱ���䣬���ܶ�ʼ�ղ��䣬������Ϊ�ж�ƽ������ݣ�B����C����÷�Ӧ�����ʵ����ڼ��ٵĻ�ѧ��Ӧ����������������ʵ�������ʱ��ı仯���仯���ﵽƽ��״̬��C��ȷ��D����λʱ��������2molN��ͬʱ����1molM��ֻ��˵��������N��M�Ĺ�ϵ������˵�����淴Ӧ���ʵĹ�ϵ��D����ѡC����4��A�������¶�������Ӧ���ʣ�A��ȷ��B������ѹǿ�ܼ�С��ѧ��Ӧ���ʣ�B����C����СM��Ũ�ȣ���ѧ��Ӧ������Ӧ�����ƶ�������Ӧ���ʼ�С��C����D������Ӧ���������С������ڼ�ѹ����������Ӧ���ʣ�D��ȷ����ѡAD��


 ����5��2���ϵ�д�
����5��2���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯī�缫���50mLCuSO4����Һ�������Ͼ��ռ���4.48L����(��״��)����ԭ���Һ��Cu2�����ʵ���Ũ��Ϊ
A. 1mol��L��1 B. 2 mol��L��1 C. 3mol��L��1 D. 4 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����������±�ػ����϶��ɵ�±�ػ�����仯ѧ������Cl2���ƣ���������ͷǽ�����Ӧ����±�������ˮ��Ӧ��BrCl+H2O = HCl+HBrO�������й�BrCl�����ʵ������в���ȷ���ǣ� ��
A. BrCl��NaOH��Һ��Ӧ����NaCl��NaBrO������
B. BrCl���н�ǿ��������
C. ��ʹ��ʪ�ĵ��۵⻯����ֽ����
D. BrCl��ˮ��Ӧ�У�BrCl�������������ǻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ�1,2-���������ԭ����
CH3CH2OH![]() CH2=CH2��+H2O
CH2=CH2��+H2O
CH2=CH2+Br2��BrCH2CH2Br
���ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������l40����ˮ�������ѣ�������������������Ҵ��Ʊ�1��2-���������װ����ͼ��ʾ���й������б����£�
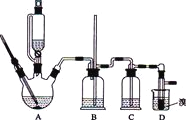
�й������б����£�
�Ҵ� | 1��2-�������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/gcm-3 | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | -130 | 9 | -116 |
(1)�ڷ�Ӧ�������Ⱥ���δ�ӷ�ʯ��Ӧ��ȡ����ȷ������________________���жϸ��Ʊ���Ӧ�Ѿ��������������_________________��
(2)װ��C��Ӧ����______________�����շ�Ӧ�в�����ijЩ��Ӱ�����������(��д��ȷѡ��ǰ����ĸ)
a.ˮ b.Ũ���� c.NaOH��Һ d.KMnO4��Һ
(3)װ��B����ֱ�ij�������ȫ�ܵ����ã���ԭ����_____________��
(4)��������������Br2�������_________ϴ�ӳ�ȥ(��д��ȷѡ��ǰ����ĸ)
a.ˮ b.�Ҵ� c.KI��Һ d.NaHSO3��Һ
������Ӧ�Ļ�ѧ����Ϊ____________________��
(5)�����������������������ѣ�����__________�ķ�����ȥ��
(6)��Ӧ������Ӧ����ˮ��ȴװ��D����ҪĿ����__________________�����ֲ��ܹ�����ȴ(���ñ�ˮ)����ԭ����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z����Ԫ�صĵ��Ӳ�����ͬ�����ǵ����������ֱ�Ϊ�����������������������������������Ԫ�ص�ԭ�������Ĵ�С˳���ǣ�����
A. X>Y>Z B. Y>Z>X
C. X>Z>Y D. Z>X>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ��(������Ϊ���Ե缫)������SO2�����������ų�����Һ����NO2�����й��ڸ�װ��������˵������ȷ�������

��.aΪֱ����Դ�ĸ���
��.�����ĵ缫��ӦʽΪ��2HSO3-+2H++2e-=S2O42-+2H2O
��.�����ĵ缫��ӦʽΪ��SO2+2H2O-2e-=SO42-+4H+
��.���ʱ��H+��������ͨ�������ӽ���Ĥ��������
A. ������ B. ������
C. �ں͢� D. �ۺ͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʵĽṹ�����ʶ����ڱ������о������������Ǹ��õ�����ͬ��֪ʶ��
(1)��̬��ԭ���У��۵���ռ��_________��ԭ�ӹ�����ƻƷ���ʽΪAs2S3�����ӽṹ��ͼ����Asԭ�ӵ��ӻ���ʽΪ_________ ��

(2)N2��CO��Ϊ�ȵ����壬��1molCO�����к��еĦм���Ŀ��_________����
(3)��CuSO4��Һ�м���������ˮ������ɫ�������������˹�����ˮ�����ܽ⣬�õ�����ɫ����Һ����������Һ�м���һ�����Ҵ�������[Cu(NH3)4]SO4 .H2O���壻�þ��������ķǽ���Ԫ���У�N��O��S��һ�������ɴ�С��˳����_________ (��Ԫ�ط�������SO42-�Ŀռ乹��Ϊ____________�������к��еĻ�ѧ����__________�������Ҵ�������[Cu(NH3)4]SO4 .H2O�����ԭ����____________��
(4)������PCl5��һ�ְ�ɫ���壬��������ϵ����ṹģ��������ͼ��ʾ����A��B���������ɡ� ���������148���ۻ����γ�һ���ܵ�������塣��֪A����CCl4������ͬ�Ŀռ乹�ͺ����ƵĻ�ѧ����������AΪ_________ �� BΪ_______________��
(5)������BP)��һ�ֳ�Ӳ��ĥͿ����ϣ�����ͼΪ��������������֪�������������ԭ�Ӻ���ԭ�Ӻ˼��Ϊx cm�������Ħ������Ϊbg.��mol-1�������ӵ�����ΪNA�����������ܶȵı���ʽ
Ϊ____________g.cm-3�����г�����ʽ����)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������������;�Ĺ�ϵ����ȷ����( )
A. �������ƣ������� B. �ռ ����θ������һ��ҩ��
C. С�մ� ���ͷ���Ҫ�ɷ� D. ������ ��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڶ����������������ȷ����
�� ����������������ά����Ҫԭ��
�� �衢̼ԭ������㶼��4�����ӣ���SiO2������������CO2����
�� SiO2���ܺ�����������Һ��ӦҲ�ܺ�����ᷴӦ��������������
�� ��CO2ͨ��Na2SiO3��Һ���н�״�������ɣ�˵��̼��ȹ�������ǿ
A. �ڢ� B. �ۢ� C. �ڢ� D. �٢�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com