
| △c |
| △t |
| 0.3mol/L |
| 10min |
| 0.15mol/L |
| 0.45mol/L |


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
| 实验编号 | NaOH溶液的浓度 (mol/L) | 消耗NaOH溶液的 体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 19.98 | 20.00 |
| 2 | 0.10 | 20.02 | 20.00 |
| 3 | 0.10 | 20.00 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
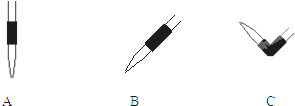
| A、实验室制备有毒气体应在通风橱中进行,且必须对尾气进行吸收或处理 |
| B、浓硝酸需用细口棕色试剂瓶密封保存 |
| C、氢气还原氧化铜,一般先预热氧化铜,然后通入氢气 |
| D、高锰酸钾等药品不能和易燃物同放,且远离火源 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+、Mg2+、NO3-、CO32+ |
| B、Na+、Al3+、Cl-、Mg2+ |
| C、K+、Ba2+、Cl-、HCO3- |
| D、NH4+、Ba2+、Fe3+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由前到后金属单质的还原性逐渐增强 |
| B、由前到后金属阳离子的氧化性逐渐增强 |
| C、氢以后的金属单质都很稳定,不能失电子 |
| D、金属K的活动性最强,它能将所有金属从盐溶液中置换出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解质一定能导电 |
| B、某物质不是电解质就是非电解质 |
| C、非电解质在水溶液中也可能会发生电离 |
| D、强电解质在水溶液中完全以离子形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
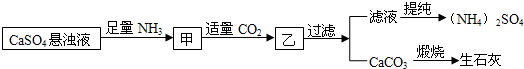
| A、生成1mol (NH4)2SO4至少消耗2mol NH3 |
| B、CO2可被循环使用 |
| C、先通二氧化碳,后通氨气,效果相同 |
| D、往甲中通CO2有利于制备(NH4)2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com