
【题目】(1)0.92g甲苯(分子式为C7H8,常温下为液态)在足量的O2中燃烧,生成CO2气体和液态水,放出39.43kJ的热量。该反应的热化学方程式为__________。
(2)将煤转化为水煤气(CO和H2的混合气体)是通过化学方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要化学反应为:C(s) + H2O(g)=CO(g) + H2(g);△H1。
已知:①2H2(g) + O2(g) = 2H2O(g);△H2=-483.6kJ·mol-1,
②2C(s) + O2(g) = 2 CO(g); △H3=-221.0kJ·mol-1,
结合上述热化学方程式,计算得出△H1= _______。
(3)反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

①该反应是___________反应(填“吸热”、“放热”)。
②在反应体系中加入催化剂,化学反应速率增大, E1、E2和ΔH的变化是:E1________,E2_______,ΔH _______(填“增大”、“减小”或“不变”)
③当反应达到平衡时,其他条件不变,升高温度,A的转化率______(填“增大”、“减小”或“不变”)。
【答案】C7H8(l)+9O2(g)=7CO2(g)+4H2O(l);H =- 3943 kJ·mol-1 +131.3 kJ·mol-1 放热 减小 减小 不变 减小
【解析】
(1)0.92g甲苯的物质的量为![]() =0.01mol,据此计算1mol甲苯在足量的O2中燃烧,生成CO2气体和液态水,放出的热量,再书写反应的热化学方程式;
=0.01mol,据此计算1mol甲苯在足量的O2中燃烧,生成CO2气体和液态水,放出的热量,再书写反应的热化学方程式;
(2)根据盖斯定律分析计算;
(3)由图象可知,反应物的能量高于生成物的能量;催化剂能够降低反应所需的活化能,但不改变反应物的总能量与生成物的总能量;结合温度对平衡的影响分析解答。
(1)0.92g甲苯的物质的量为![]() =0.01mol,0.01mol甲苯(分子式为C7H8,常温下为液态)在足量的O2中燃烧,生成CO2气体和液态水,放出39.43kJ的热量,则1mol甲苯(分子式为C7H8,常温下为液态)在足量的O2中燃烧,生成CO2气体和液态水,放出3943kJ的热量,则热化学方程式为:C7H8(l)+9O2(g)=7CO2(g)+4H2O(l)△H=-3943 kJ/mol,故答案为:C7H8(l)+9O2(g)=7CO2(g)+4H2O(l)△H=-3943 kJ/mol;
=0.01mol,0.01mol甲苯(分子式为C7H8,常温下为液态)在足量的O2中燃烧,生成CO2气体和液态水,放出39.43kJ的热量,则1mol甲苯(分子式为C7H8,常温下为液态)在足量的O2中燃烧,生成CO2气体和液态水,放出3943kJ的热量,则热化学方程式为:C7H8(l)+9O2(g)=7CO2(g)+4H2O(l)△H=-3943 kJ/mol,故答案为:C7H8(l)+9O2(g)=7CO2(g)+4H2O(l)△H=-3943 kJ/mol;
(2)①2H2(g)+O2(g)=2H2O(g) △H2=-483.6kJmol-1,②2C(s)+O2(g)=2CO(g) △H3=-221.0kJmol-1,为求C(s)+H2O(g)=CO(g)+H2(g)的△H1,可用盖斯定律将![]() 可得:△H1=
可得:△H1=![]() =+131.3 kJ·mol-1,故答案为:+131.3 kJ·mol-1;
=+131.3 kJ·mol-1,故答案为:+131.3 kJ·mol-1;
(3)①由图象可知,反应物的能量高于生成物的能量,该反应是一个能量降低的反应,所以属于放热反应,故答案为:放热;
②加入催化剂改变了反应的途径,降低反应所需的活化能,则 E1和E2都减小,但是催化剂不改变反应物的总能量与生成物的总能量,即反应热不变,所以催化剂对该反应的反应热无影响,则ΔH不变,故答案为:减小;减小;不变;
③该反应为放热反应,升高温度,平衡逆向移动,A的转化率减小,故答案为:减小。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。
(1)请写出Fe的基态原子核外电子排布式____________。
(2)金属A的原子只有3个电子层,其第一至第四电离能如下:
电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15 390 | 21 771 |
则A原子的价电子排布式为______________。
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(Ⅰ)溶液来吸收原料气体中的CO(Ac—代表CH3COO—),其反应是:[Cu(NH3)2]Ac+CO+NH3![]() [Cu(NH3)3CO]Ac[醋酸羰基三氨合铜(Ⅰ)] ΔH<0。
[Cu(NH3)3CO]Ac[醋酸羰基三氨合铜(Ⅰ)] ΔH<0。
①C、N、O三种元素的第一电离能由小到大的顺序为____________。
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为____________。
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子和N原子轨道的杂化类型分别为________;1 mol尿素分子中,σ键的数目为________。
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3 ℃,MgO的熔点高达2800 ℃。造成两种晶体熔点差距的主要原因是____________________________________。
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾。其中NH4+的空间构型是____________(用文字描述),与NO互为等电子体的分子是____________(填化学式)。
(6)铜的化合物种类很多,如图是氯化亚铜的晶胞结构(黑色球表示Cu+,白色球表示Cl-),已知晶胞的棱长为a cm,则氯化亚铜密度的计算式为ρ=________g·cm-3(用NA表示阿伏加德罗常数)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应。下列分析正确的是
容器编号 | 实验条件 | 平衡时反应中的能量变化 |
I | 恒温恒容 | 放热Q1kJ |
II | 恒温恒压 | 放热Q2kJ |
A.放出热量:Q1<Q2B.N2的转化率:II>I
C.平衡常数:II>ID.平衡时氨气的体积分数:I>II
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀。根据上述实验事实,下列说法中,不正确的是
A.溶解度 MnS<PbS
B.MnS存在沉淀溶解平衡 MnS(s)![]() Mn2+(aq) + S2-(aq)
Mn2+(aq) + S2-(aq)
C.Cu2+转化为沉淀的原理为 MnS(s) + Cu2+(aq)=CuS(s) + Mn2+(aq)
D.沉淀转化能用于除去溶液中的某些杂质离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在中性、室温下,催化剂FeQ或FeCuQ催化![]() 解离产生的
解离产生的![]() 来降解浓度为
来降解浓度为![]() 的苯酚,降解率
的苯酚,降解率 随
随![]() 浓度、反应时间的关系如图所示
浓度、反应时间的关系如图所示![]() 保持其他条件相同
保持其他条件相同![]() 。
。
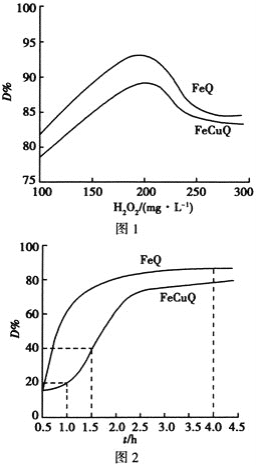
下列说法不正确的是 ![]()
![]()
A.在FeCuQ催化下,![]() 内,苯酚降解速率为
内,苯酚降解速率为![]() mol/(L·h)
mol/(L·h)
B.其他条件不变时,随![]() 浓度的增大,降解率
浓度的增大,降解率![]() 不一定增大
不一定增大
C.FeQ催化![]() 后,降解率
后,降解率![]() 不变,可能是反应达到了平衡状态
不变,可能是反应达到了平衡状态
D.随![]() 浓度的增大降解率
浓度的增大降解率![]() 减小的原因可能是过量
减小的原因可能是过量![]() 导致
导致![]() 浓度减小
浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。其中X与Y可形成一种淡黄色物质P,常温下将0.05 mol P溶于水,配成1 L溶液,其中![]() ;Z为金属元素,且Z可在W的一种氧化物中燃烧,生成一种白色的物质和一种黑色的物质。下列说法错误的是()
;Z为金属元素,且Z可在W的一种氧化物中燃烧,生成一种白色的物质和一种黑色的物质。下列说法错误的是()
A. 氢化物的沸点:W<X
B. 简单离子半径:X>Y>Z
C. 化合物P中既含有离子键又含有共价键
D. W、X、Y三种元素形成的物质的水溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常稳下,某绝热容器中盛有50mLc(H+)=10-3mol·L-1的HX溶液,向该容器中滴加c(OH-)=10-2mol·L-1的NaOH溶液,滴加过程中混合溶波的温度(T)与所加溶液体积(V)的关系如图所示。下列叙述不正确的是
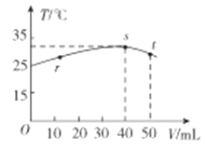
A.s点时:c(Na+)>c(X-)>c(OH-)>c(H+)
B.r→s的过程中,混合溶液中可能存在c(X-)=c(Na+)
C.pH=10的NaX溶液,用蒸馏水稀释10倍后,溶液的pH>9
D.已知某温度下CaX2的Ksp=5.3×10-9mol·L-3,在该温度下c(X-)=0.1mol·L-1的溶液中Ca2+可能的最高浓度是5.3×10-8mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝、铁是三种重要金属,它们的单质和化合物应用十分广泛。回答下列问题:
(1)镁、铝第一电离能大小的关系是I1(Mg)_________I1(Al),金属镁、铝熔点大小关系是Mg_________Al。(填“大于”、“等于”或“小于”)
(2)氯化铝加热时易升华,实验测得铝元素与氯元素形成化合物的实际组成为Al2Cl6,其结构简式如图所示。其中处于中间的Al原子杂化轨道类型为_________杂化,分子中所有原子_________(能、不能)在同一平面上。
![]()
(3)硝酸铁和尿素在乙醇中生成[Fe(H2NCONH2)6](NO3)3三硝酸六尿素合铁![]() 。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为____________。尿素分子中
。产物是一种重要的配合物,用作有机铁肥,简称铁氮肥。基态Fe3+的核外电子排布式为____________。尿素分子中![]() 键与
键与![]() 键的数目之比为_______。NO3-的空间构型为_________,经测定N2O5晶体中存在NO2+和NO3-,NO2+中氮原子为_________杂化。
键的数目之比为_______。NO3-的空间构型为_________,经测定N2O5晶体中存在NO2+和NO3-,NO2+中氮原子为_________杂化。
(4)碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如图所示。晶体中与相邻铁原子距离相等且最近的铁原子有________个,该物质的化学式为_________。若晶体密度为dg/cm3,则晶胞中最近的两个碳原子的距离为___________pm(阿伏加德罗常数的值为NA表示,写出简化后的计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp[Mg(OH)2]=1.8×10-11 mol3·L-3,Ksp[Cu(OH)2]=2.2×10-20 mol3·L-3。向浓度为0.01 mol·L-1的Cu2+和Mg2+的混合溶液中逐滴加入NaOH溶液至过量,下列说法正确的是( )
A.较先出现的沉淀是Mg(OH)2
B.两种离子开始沉淀时,Cu2+所需溶液的pH较大
C.当两种沉淀共存时,说明溶液中完全不存在Cu2+、Mg2+
D.当两种沉淀共存时,溶液中![]() ≈8.2×108
≈8.2×108
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com