
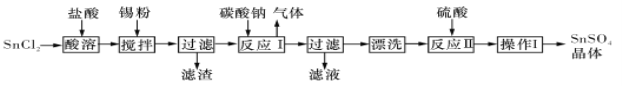
【题目】I.硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:
查阅资料:
A.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
B.SnC12易水解生成碱式氯化亚锡
回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请结合必要的化学方程式用平衡移动原理解释原因:___________。
(2)加入Sn粉的作用有两个:①调节溶液pH;②__________。
(3)反应I得到沉淀SnO,得到该沉淀的离子反应方程式是____________。
(4)操作I是____________。
II.已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8 mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5 mol/L。若在10 mL含有KCl和KI各为0.01 mol/L的溶液中,加入16 mL 0.01 mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
c(K+)>c(NO![]() )>c(Cl-)>c(Ag+)>c(I-)
)>c(Cl-)>c(Ag+)>c(I-)
B .c(K+)>c(NO![]() )>c(Ag+)>c(Cl-)>c(I-)
)>c(Ag+)>c(Cl-)>c(I-)
C.c(K+)>c(NO![]() )>c(Ag+)=c(Cl-)+c(I-)
)>c(Ag+)=c(Cl-)+c(I-)
D.c(NO![]() )>c(K+)>c(Ag+)>c(Cl-)>c(I-)
)>c(K+)>c(Ag+)>c(Cl-)>c(I-)
【答案】(10分每空2分)
I.(1)SnCl2+H2O![]() Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解
Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解
(2)防止Sn2+被氧化; (3)Sn2++CO32-=SnO↓+CO2↑
(4)加热浓缩、冷却结晶、过滤、洗涤; II.A
【解析】
试题分析:I.(1)由信息可知,SnCl2易水解生成碱式氯化亚锡,存在平衡Sn Cl2+H2O![]() Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解;
Sn(OH)Cl+HCl,加入盐酸,使该平衡向左移动,抑制Sn2+水解;
(2)由信息可知,Sn2+易被氧化,加入Sn粉除调节溶液pH外,还防止Sn2+被氧化;
(3)反应Ⅰ得到沉淀是SnO,Sn元素化合价为变化,属于非氧化还原反应,同时生成气体,该气体为二氧化碳,离子方程式为:Sn2++CO32-═SnO↓+CO2↑;
(4)由流程图可知,操作Ⅰ是从溶液中得到含结晶水的晶体,只能采取蒸发浓缩、冷却结晶、过滤、洗涤得到;
II.若在10mL含有KCl和KI各为0.01mol/L的溶液中,加入16mL0.01mol/L AgNO3溶液,首先生成AgI沉淀,
反应后剩余n(Ag+)=0.006L×0.01mol/L=6×10-5mol,继续生成AgCl沉淀,
反应后剩余n(Cl-)=0.01×0.01mol/L-6×10-5mol=4×10-5mol,
c(Cl-)=![]() =1.53×10-3mol/L,
=1.53×10-3mol/L,
浊液中c(Ag+)═![]() =1.02×10-7mol/L,
=1.02×10-7mol/L,
c(I-)═![]() =1.48×10-9mol/L,混合溶液中n(K+)=2×10-4mol,
=1.48×10-9mol/L,混合溶液中n(K+)=2×10-4mol,
n(NO3-)=0.016L×0.01mol/L=1.6×10-4mol,则c(K+)>c(NO3-),
故c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-),故选A。


科目:高中化学 来源: 题型:
【题目】25℃时,0.1molNa2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关溶液中离子浓度关系叙述正确的是
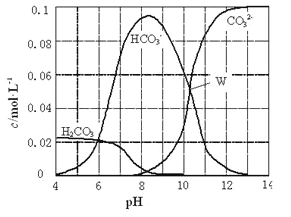
A. W点所示的溶液中:c (Na+)+c (H+)=2c(CO32-)+c (OH-)+c (Cl-)
B. pH=8的溶液中:c (H+)+c (H2CO3)+c (HCO3-)= c (OH-)+c (Cl-)
C. pH= 4的溶液中:c (H2CO3)+c (HCO3-)+c (CO32-)<0.1mol·L-1
D. pH=11的溶液中:c (Na+)>c (Cl-)>c (CO32-)>c (HCO3-)>c (H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,NO跟NH3可以发生反应:6NO+4NH3=5N2+6H2O,该反应中被还原和被氧化的氮元素的质量比是( )
A. 3:2 B. 2:1 C. 1:1 D. 2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于组成生物体化学元素的论述,正确的是
A. 组成生物体的化学元素中,碳元素含量最多
B. 动物和植物所含的化学元素的种类差异很大
C. 无机自然界中的元素都可以参与组成生物体
D. 微量元素是维持正常生命活动不可缺少的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素,D单质燃烧时呈现黄色火焰,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
(1)元素名称:C________、D________、F________。
(2)E在元素周期表中的位置:______________________________。
(3)A、B组成的最简单化合物的结构式是_________________。
(4)C、D按原子个数比1∶1组成的一种化合物与A、E按原子个数比2∶1组成的一种化合物发生反应的化学方程式为_________________________。
(5)能说明E的非金属性比F的非金属性_______(填“强”或“弱”)的事实是:________(举一例)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由NO和CO组成的混合气体与同温同压下空气的密度相等(空气的平均相对分子质量为29),下列关系正确的是( )
A. 混合气体中,CO与NO质量比15:14
B. 混合气体中,CO与NO分子个数比1:2
C. 混合气体中CO占有的体积大于NO占有的体积
D. 混合气体中,CO与NO密度比14:15
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED系列产品是被看好的一类节能新产品,如图是一种氢氧燃料电池驱动LED发光的装置.下列有关叙述正确的是( )
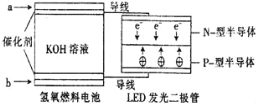
A.a处通入氢气,发生了还原反应:H2﹣2e﹣+2OH﹣=2H2O
B.该装置中只涉及两种形式的能量转化,电池中的KOH溶液也可用稀硫酸溶液代替
C.b处通入氧气,为电池的正极
D.P﹣型半导体连接的是电池负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2014·四川理综,6,6分)下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 NaHCO3溶液与0.1 mol·L -1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO![]() )>c(HCO
)>c(HCO![]() )>c(OH-)
)>c(OH-)
B.20 mL 0.1 mol·L-1 CH3COONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH![]() )+c(OH-)
)+c(OH-)
D.0.1 mol·L-1 CH3COOH溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com