
【题目】国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”。
(1)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式:____________。
(2)除去Na2CO3粉末中混入的NaHCO3杂质最佳方法是_________,化学方程式为_________。
科目:高中化学 来源: 题型:
【题目】铂(Pt)及其化合物用途广泛。
(1)在元素周期表中,Pt与Fe相隔一个纵行、一个横行,但与铁元素同处_____族。基态铂原子有2个未成对电子,且在能量不同的原子轨道上运动,其价电子排布式为____________。
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
①吡啶分子是大体积平面配体,其结构简式如图所示。每个吡啶分子中含有的σ键数目为________。
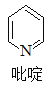
②二氯二吡啶合铂中存在的微粒间作用力有________(填序号)。
a.离子键 b.氢键 c.范德华力 d.金属键 e.非极性键
③反式二氯二吡啶合铂分子是非极性分子,画出其结构式:_____。
(3)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
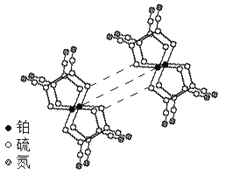
① 硫和氮中,第一电离能较大的是______。
②“分子金属”可以导电,是因为______能沿着其中的金属原子链流动。
③“分子金属”中,铂原子是否以sp3的方式杂化?简述理由:______。
(4)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示。若金属铂的密度为d g·cm-3,则晶胞参数a=_________________nm(列计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是

A. 该化合物的名称为乙酸乙酯
B. 1mol该化合物与2 mol Br2发生加成反应
C. 该化合物既能发生水解反应,又能发生氧化反应
D. 该化合物的同分异构体中,能与NaHCO3反应放出CO2的只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C60具有完美的球形结构。之后Si60、N60等球形分子被不断制备出来。回答下列问题:
(1)Si 的核外电子排布式为____________,C和N元素中第一电离能较大的是________________。
(2)富勒烯衍生物具有良好的光电性能,富勒烯(C60)的结构如图所示,C60属于________晶体;C60中C原子的杂化类型为__________________。

(3)N60的晶体中存在的作用力有____________(填字母)。
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键 F.金属键
(4)立方氮化硼(BN)可做磨料,其结构与金刚石相似,二者具有相似性结构的原因是______________________________________________。
(5)金属M(相对原子质量为m)与N60形成的化合物晶体结构如图所示(其中白球代表N60,黑球代表金属M),其晶胞边长为k pm,NA代表阿伏加德罗常数的值,则其密度为_______g·cm-3,该化合物中N60的配位数为__________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为_____,物质的量之比为_____,质量之比为_____。
(2)等质量的 SO2 和 SO3 物质的量之比是_____,氧原子数之比为_____。
(3)19 g 某二价金属的氯化物 ACl2 中含有 0.4mol Cl-,则 A 的摩尔质量为_____。
(4)密度为 1.84 g/cm3,质量分数为 98%的浓硫酸浓度为_____mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. 无色透明的溶液中:Fe3+、NH、I—、CO![]()
B. 0.1 mol·L-1 KNO3溶液中:Na+、Fe2+、Cl—、SO![]()
C. 使甲基橙变红的溶液中:Na+、Mg2+、SO![]() 、AlO
、AlO
D. 水电离产生的c(H+) =10-13mol·L-1的溶液中:K+、Ca2+、NO、HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.32 g Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1 mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如下图所示,下列说法中错误的是( )
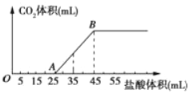
A. OA段发生反应的离子方程式为:H++OH-=H2O、CO32-+H+=HCO3-
B. A点溶液中的溶质为NaCl、NaHCO3
C. 当加入45 mL盐酸时,产生CO2的体积为336mL
D. 混合物中NaOH的质量0.20 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】β—紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是( )
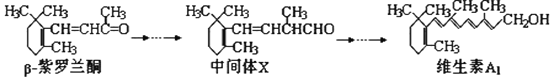
A. β—紫罗兰酮与中间体X互为同分异构体
B. β—紫罗兰酮不可使酸性KMnO4溶液褪色
C. 维生素A1易溶于NaOH溶液
D. 1mol维生素A1最多能与5molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是
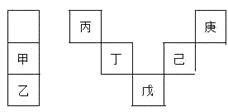
A. 丙与戊的原子序数相差28
B. 气态氢化物的稳定性:庚<己<戊
C. 常温下,甲和乙的单质均能与水剧烈反应
D. 丁的最高价氧化物可用于制造光导纤维
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com