
【题目】已知甲、乙、丙、丁都是含碳物质。其中丁是一种有机物,甲、乙、丁都能发生燃烧生成丙,同时放出大量的热,甲与丙反应时需要吸收热量。则甲、乙、丙、丁分别是 ( )
A.CO,C,CO2,CH4B.C,CO2,CH4,CO
C.C,CO,CO2,CH4D.C,O2,CO2,CH4
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列物质中属于有机物的是( )
①乙醇 ②蛋白质 ③石墨 ④甲烷 ⑤蔗糖 ⑥碳酸 ⑦一氧化碳 ⑧碳酸钙 ⑨乙酸
A.①④⑤⑦⑧⑨B.①④⑤⑨C.①②④⑤⑨D.①②④ ⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列说法正确的是
A.化学反应的实质就是旧化学键的断裂,新化学键的形成,在化学反应中,反应物转化为生成物的同时,必然伴随着能量的变化
B.钢铁生锈腐蚀时,铁被氧化
C.放热反应发生时,不一定要加热。但吸热反应必须要加热才能发生
(2)在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ 热量,氢气燃烧的热化学方程式表示为 。
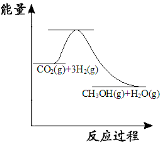
(3)目前工业上有一种方法是用CO2来生产甲醇:CO2(g)+3H2(g)![]() CH3OH(g) +H2O(g);如图表示该反应进行过程中能量的变化。(单位为:kJ·mol1)该反应是 (填“吸热”或“放热”)反应,ΔH 0(填“>”或“<”)。
CH3OH(g) +H2O(g);如图表示该反应进行过程中能量的变化。(单位为:kJ·mol1)该反应是 (填“吸热”或“放热”)反应,ΔH 0(填“>”或“<”)。
(4)比较下面各组热化学方程式,ΔH1<ΔH2的是 。
A.2H2(g) + O2(g) ![]() 2H2O(g) ΔH1 2H2(g) + O2(g)
2H2O(g) ΔH1 2H2(g) + O2(g) ![]() 2H2O(1) ΔH2
2H2O(1) ΔH2
B.S(g) + O2(g) ![]() SO2(g ) ΔH1 S(s) + O2(g)
SO2(g ) ΔH1 S(s) + O2(g) ![]() SO2(g ) ΔH2
SO2(g ) ΔH2
C.C(s) +![]() O2(g)
O2(g) ![]() CO (g ) ΔH1 C(s) +O2(g)
CO (g ) ΔH1 C(s) +O2(g) ![]() CO2 (g ) ΔH2
CO2 (g ) ΔH2
D.H2(g) + Cl2(g) ![]() 2HCl(g ) ΔH1
2HCl(g ) ΔH1 ![]() H2(g) +
H2(g) +![]() Cl2(g)
Cl2(g) ![]() HCl(g) ΔH2
HCl(g) ΔH2
(5)101 kPa条件下,14 g N2和3 g H2反应生成NH3的能量变化如图示意:
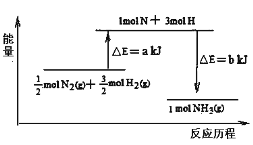
又已知:①已知b=1173;②25℃、101 kPa下N2(g)+3H2 (g) ![]() 2 NH3 (g) ΔH =-92 kJ·mol1,则a = 。
2 NH3 (g) ΔH =-92 kJ·mol1,则a = 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某电动汽车使用的是高铁电池,其总反应为3Zn(OH)2+2Fe(OH)3+4KOH ![]() 3Zn+2K2FeO4+8H2O,下列说法正确的是( )
3Zn+2K2FeO4+8H2O,下列说法正确的是( )
A.放电时,若有6mol电子发生转移,则有2mol K2FeO4被氧化
B.放电时,正极反应为:FeO42﹣+4H2O+3e﹣═Fe(OH)3+5OH﹣
C.充电时,电池的负极与外接电源的正极相连
D.充电时,阴极附近溶液的pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】比较下列各组热化学方程式中ΔH的大小关系。
(1)S(s)+O2(g)===SO2(g) ΔH1
S(g)+O2(g)===SO2(g) ΔH2
ΔH1__________ΔH2
(2)CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH2
ΔH1__________ΔH2
(3)4Al(s)+3O2(g)===2Al2O3(s) ΔH1
4Fe(s)+3O2(g)===2Fe2O3(s) ΔH2
ΔH1__________ΔH2
(4)煤作为燃料有2种途径:
途径1——直接燃烧:
C(s)+O2(g)===CO2(g) ΔH1<0
途径2——先制水煤气:
C(s)+H2O(g)===CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
2CO(g)+O2(g)===2CO2(g) ΔH3<0
2H2(g)+O2(g)===2H2O(g) ΔH4<0
ΔH1、ΔH2、ΔH3、ΔH4的关系式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业的核心反应:N2(g)+3H2(g)![]() 2NH3(g)的反应过程中能量变化如图所示,回答下列问题:
2NH3(g)的反应过程中能量变化如图所示,回答下列问题:
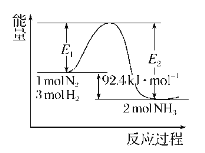
(1)ΔH=______;在反应体系中加入催化剂,反应速率增大,E2的变化是______(填“增大”“减小”或“不变”);△H (填“增大”“减小”或“不变”)。
(2)在500℃、2×107 Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量_______(填“<”“>”或“=”)46.2 kJ,理由__________________________________。
(3)已知在25℃、101 kPa时,14克CO气体完全燃烧放出热量为Q kJ。
请写出CO燃烧热的热化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业中电解饱和食盐水的原理示意图如图所示: 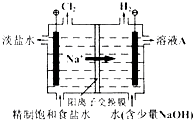
(1)溶液A的溶质是;
(2)电解饱和食盐水的离子方程式是;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用平衡移动移动原理解释盐酸的作用:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100g碳燃烧所得气体中,CO占![]() ,CO2占
,CO2占![]() 体积,且C(s)+
体积,且C(s)+![]() O2(g)===CO(g);ΔH(298K)=-110.35kJ·mol-1,CO(g)+
O2(g)===CO(g);ΔH(298K)=-110.35kJ·mol-1,CO(g)+![]() O2(g)===CO2(g);ΔH(298K)=-282.57kJ·mol-1。与这些碳完全燃烧相比较,损失的热量是( )
O2(g)===CO2(g);ΔH(298K)=-282.57kJ·mol-1。与这些碳完全燃烧相比较,损失的热量是( )
A.392.92kJ B.2489.44kJ
C.784.92kJ D.3274.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12 000~20 000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
化学键 | N≡N | F-F | N-F |
键能/kJ·mol-1 | 941.7 | 154.8 | 283.0 |
下列说法中正确的是
A.过程N2(g)![]() 2N(g)放出能量
2N(g)放出能量
B.过程N(g)+3F(g)![]() NF3(g)放出能量
NF3(g)放出能量
C.反应N2(g)+3F2(g)![]() 2NF3(g)吸收热量
2NF3(g)吸收热量
D.NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com