
【题目】氯碱工业中电解饱和食盐水的原理示意图如图所示: 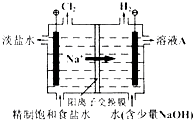
(1)溶液A的溶质是;
(2)电解饱和食盐水的离子方程式是;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用平衡移动移动原理解释盐酸的作用:
【答案】
(1)NaOH
(2)2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑
2OH﹣+H2↑+Cl2↑
(3)Cl2与水的反应为Cl2+H2O?HCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出
【解析】解:(1)装置图中氯气和氢气生成的位置判断,生成氯气的电极为阳极,左边电极为正极,右边电极为负极,连接电极为阴极,溶液中氢离子在阴极得到电子生成氢气,氢氧根离子浓度增大,溶液A为氢氧化钠溶液,所以答案是:NaOH;(2)电解饱和食盐水,溶液中的氯离子在阳极失电子生成氯气,氢离子在阴极得到电子生成氢气,阴极附近氢氧根离子浓度增大生成氢氧化钠,反应的离子方程式:2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑,所以答案是:2Cl﹣+2H2O
2OH﹣+H2↑+Cl2↑,所以答案是:2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑;(3)电解时用盐酸控制阳极区溶液的pH在2~3的作用是促使化学平衡Cl2+H2OHCl+HClO向左移动,减少Cl2在水中的溶解,有利于Cl2的逸出,
2OH﹣+H2↑+Cl2↑;(3)电解时用盐酸控制阳极区溶液的pH在2~3的作用是促使化学平衡Cl2+H2OHCl+HClO向左移动,减少Cl2在水中的溶解,有利于Cl2的逸出,
所以答案是:Cl2与水的反应为Cl2+H2OHCl+HClO,增大HCl的浓度使平衡逆向移动.减少Cl2在水中的溶解,有利于Cl2的逸出.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。
已知:①P4(白磷,s)+5O2(g)![]() P4O10(s) ΔH=2 983.2 kJ·mol1
P4O10(s) ΔH=2 983.2 kJ·mol1
②P(红磷,s)+![]() O2(g)
O2(g)![]()
![]() P4O10(s) ΔH=738.5 kJ·mol1
P4O10(s) ΔH=738.5 kJ·mol1
则白磷转化为红磷的热化学方程式为
A.P4(白磷,s)![]() 4P(红磷,s) ΔH=29.2 kJ·mol1
4P(红磷,s) ΔH=29.2 kJ·mol1
B.P4(白磷,s)![]() 4P(红磷,s) ΔH=+29.2 kJ·mol1
4P(红磷,s) ΔH=+29.2 kJ·mol1
C.P4(白磷,s)![]() 4P(红磷,s) ΔH=2 244.7 kJ·mol1
4P(红磷,s) ΔH=2 244.7 kJ·mol1
D.P4(白磷,s)![]() 4P(红磷,s) ΔH=+2244.7 kJ·mol1
4P(红磷,s) ΔH=+2244.7 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙、丁都是含碳物质。其中丁是一种有机物,甲、乙、丁都能发生燃烧生成丙,同时放出大量的热,甲与丙反应时需要吸收热量。则甲、乙、丙、丁分别是 ( )
A.CO,C,CO2,CH4B.C,CO2,CH4,CO
C.C,CO,CO2,CH4D.C,O2,CO2,CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. NaCl的摩尔质量是58.5g/mol B. 1mol NaOH的质量是40g
C. 1mol氮的质量是14g D. 摩尔不是物理量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在指定溶液中能大量共存的是( )
A.强酸溶液中:K+、Fe2+、MnO4﹣、SO42﹣
B.![]() =0.1mol/L的溶液:Na+、K+、SiO32﹣、NO3﹣
=0.1mol/L的溶液:Na+、K+、SiO32﹣、NO3﹣
C.既能溶解Al(OH)3又能溶解 H2SiO3的溶液中:Na +、CO32﹣、SO32﹣、NO3﹣
D.在含有大量HCO3﹣的溶液中:K+、Na+、AlO2﹣、Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列物质所含粒子数为0.2NA的是( )
①标准状况下,2.24L Cl2中含有的共价键数
②常温下,2L pH=13的Na2CO3溶液中含有的OH﹣离子数
③100mL 1.0mo1L﹣1的NaAlO2溶液中含有的氧原子数
④标准状况下,2.24L Cl2与足量的NaOH溶液反应时转移的电子数
⑤3.2gO2和O3的混合气体中含有的氧原子数
⑥3.9g Na2O2晶体中所含的离子总数.
A.②③⑥
B.②⑤
C.③⑤⑥
D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验,能成功的是
A.苯和溴水、铁屑混合制溴苯
B.用溴水除乙烷中混有的乙烯
C.苯与浓硝酸和浓硫酸的混合物共热至70℃~80℃制硝基苯
D.用酒精和浓盐酸通过加热来制取乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com