
【题目】2020年以来,新型冠状病毒肺炎席卷全世界,中国传统中药“连花清瘟胶囊”助力世界抗疫。连花清瘟胶囊配方中含传统中药金银花,绿原酸是金银花主要抗菌、抗病毒有效药理成分之一,结构简式如下图所示。关于绿原酸的下列推测不合理的是
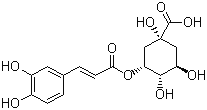
A.分子中有4个手性碳原子B.可溶于水也可溶于乙醇
C.1mol最多可和3mol NaOH反应D.可通过缩聚反应形成高分子
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】每次取20 g海水,严格按照过滤、蒸发、冷却、称量、计算的实验步骤规范操作,连续实验三次,平均得固态盐a g。该海水中含氯化钠的质量分数是( )
A.大于5a%
B.小于5a%
C.等于5a%
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱土金属(ⅡA族)元素单质及其相关化合物的性质、合成一直以来是化学界研究的重点。回答下列问题:
(1)对于碱土金属元素Be、Mg、Ca、Sr、Ba,随着原子序数的增加,以下性质呈单调递减变化的是___。
A.原子半径 B.单质的硬度 C.第一电离能
(2)①铍与相邻主族的___ 元素性质相似。下列有关铍和该元素的叙述正确的有___填标号。
A.都属于p区主族元素
B.电负性都比镁大
C.第一电离能都比镁大
D.氯化物的水溶液pH均小于7
②(NH4)2BeF4是工业制备金属铍过程中的重要中间产物,其阳离子含有的化学键类型为__,阴离子中心原子杂化方式为___。
(3)Sr是人体必需的微量元素,SrCO3是其重要的化合物之一。Sr2+的电子排布式为___判断SrCO3的热分解温度___(填“大于”/“小于”)CaCO3的热分解温度,理由是____。
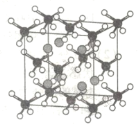
(4)MgH2和金属Ni在一定条件下用球磨机研磨,可制得化学式为Mg2NiH4的储氢化合物,其立方晶胞结构如图所示:
①Mg原子周围距离最近且相等的Ni原子有___个,若晶胞边长为646pm,则Mg—Ni核间距为___pm(结果保留小数点后两位,![]() 取1.73)。
取1.73)。
②若以晶胞中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则该化合物的储氢能力为___(列出计算式即可。假定该化合物中所有的H可以全部放出,液氢密度为dg/cm3;设NA代表阿伏伽德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香天竺葵醇具有温和、香甜的玫瑰花气息,其结构式如图所示。下列有关香天竺葵醇的说法错误的是
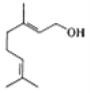
A.分子中含有两种官能团
B.该物质中的碳原子一定全部共面
C.使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色的原理不同
D.香天竺葵醇能发生加聚反应和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:浓硫酸易使有机物脱水,如图是用实验室制得的乙烯(C2H5OH![]() CH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是
CH2=CH2↑+H2O)与溴水作用制取1,2-二溴乙烷的部分装置图,根据图示判断下列说法正确的是

A. 装置①和装置③中都盛有水,其作用相同
B. 装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同
C. 产物可用分液的方法进行分离,1,2-二溴乙烷应从分液漏斗的上口倒出
D. 制备乙烯时温度计水银球位置应在反应液的液面下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应CH3COOH(l) + C2H5OH(l) ![]() CH3COOC2H5(l) + H2O(l) ΔH=-2.7kJ·mol-1,下列说法正确的是
CH3COOC2H5(l) + H2O(l) ΔH=-2.7kJ·mol-1,下列说法正确的是
A.由于水为液态,移走生成的水平衡不会移动。
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的ΔS等于零
C.因为反应的△H 接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀___________。
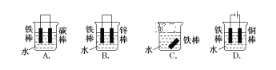
(2)实际生产可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:

①A电极对应的金属是________(写元素名称),B电极的电极反应式是_________。
②镀层破损后,镀铜铁和镀锌铁中更容易被腐蚀的是___________。
A 镀铜铁 B 镀锌铁。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是_______(填字母)。
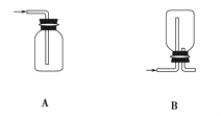

漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为_________________________。漂白粉与浓盐酸发生氧化还原反应,化学方程式为____________________________________。
(2)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
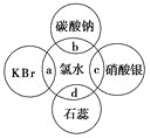
①能证明氯水具有漂白性的是______(填“a”“b”“c”或“d”)。
②c过程中的现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。W、X、Y、Z均为短周期元素,原子序数依次增加,其中W、X、Z组成的化合物M、N、R之间存在如图所示的反应。下列叙述正确的是
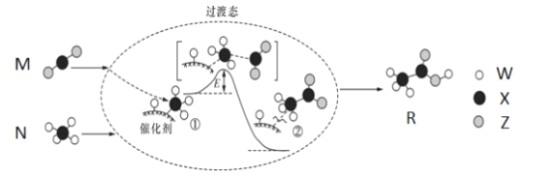
A.元素非金属性的顺序为X>Y>Z>W
B.M、N、R三种分子中,所有原子均满足8电子稳定结构
C.M、N、R三种分子均含有极性键和非极性键
D.W、X、Y、Z四种元素既可形成离子化合物,又可形成共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com