
【题目】我国科研人员提出了由CO2 和 CH4 转化为高附加值产品CH3COOH 的催化反应历程如图所示:
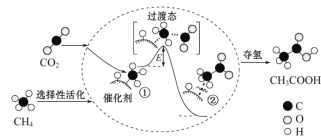
下列说法正确的是
A. 该反应证明任何非自发反应只要条件合适都能进行
B. 反应过程中,只有C—H 键发生断裂
C. 状态①、②之间的能量差即该反应的焓变
D. 合适的催化剂可有效降低活化能
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】把![]() L含硫酸铵、硝酸铵的混合溶液分成两等份,一份用
L含硫酸铵、硝酸铵的混合溶液分成两等份,一份用![]() mol烧碱刚好把NH3全部赶出,另一份与氯化钡溶液完全反应消耗
mol烧碱刚好把NH3全部赶出,另一份与氯化钡溶液完全反应消耗![]() molBaCl2,则原溶液中
molBaCl2,则原溶液中![]() (NO
(NO![]() )为( )
)为( )
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·1-1
mol·1-1
C. ![]() mol·L-1 D.
mol·L-1 D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯酚为原料合成防腐剂尼泊金丁酯(对羟基苯甲酸丁酯)、香料G (结构简式为![]() )的路线如下:
)的路线如下:

已知:
①
② ![]()
注:R、R′为烃基或H原子,R″为烃基
请回答:
(1)下列说法正确的是_________。
A.反应②F→G,既属于加成反应,又属于还原反应
B.若A→B属于加成反应,则物质X为CO
C.甲物质常温下是一种气体,难溶于水
D.上述合成路线中,只有3种物质能与FeCl3溶液发生显色反应
(2)上述方法制取的尼泊金酯中混有属于高聚物的杂质,生成该物质的化学方程式为_________。
(3)E的结构简式为_____________。
(4)写出同时符合下列条件并与化合物B互为同分异构体的有机物的结构简式____________。
①分子中含有苯环,无其它环状结构;
②1H-NMR谱表明分子中有4种氢原子:
③能与NaOH溶液反应。
(5)设计以乙烯为原料制备1-丁醇的合成路线(用流程图表示,无机试剂任选)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图能量关系示意图,下列说法正确的是

A. 1 mol C(s)与1 mol O2(g)的能量之和为393.5 kJ
B. 反应2CO(g)+O2(g)= 2CO2(g)中,生成物的总能量大于反应物的总能量
C. 由C(s)→CO(g)的热化学方程式为:2C(s)+O2(g)= 2CO(g) ΔH=-221.2 kJ·mol-1
D. 热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH=-10.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关节炎首次发作一般在寒冷季节,原因是关节滑液中形成了尿酸钠晶体(NaUr),易诱发关节疼痛,其化学机理是:①HUr(aq)+H2O(1)![]() Ur-(aq)+H3O+(aq)
Ur-(aq)+H3O+(aq)
② Ur-(aq)+Na+(aq)![]() NaUr(s) △H
NaUr(s) △H
下列叙述错误的是
A. 降低温度,反应②平衡正向移动
B. 反应②正方向是吸热反应
C. 降低关节滑液中HUr及Na+含量是治疗方法之一
D. 关节保暖可以缓解疼痛,原理是平衡②逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
请回答下列问题:
(1)请列举海水淡化的一种方法__________________________。
(2)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是______(填字母)。
A.①②③④ B.②③④① C.②④③① D.③④②①
(3)在实验室中可以用萃取的方法提取溴,可选用的试剂是________________,所用主要仪器的名称是____________________。
(4)步骤I已经获得Br2,步骤II又将Br2还原为Br—,其目的是_____________________
(5)写出步骤III反应的离子方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产钡盐的主要原料是重晶石(BaSO4)。在高温下,重晶石与石墨存在如下反应:
①: BaSO4(s)+4C(s,石墨) ![]() 4CO(g)+BaS(s) ΔH1=+571.2 kJ/mol
4CO(g)+BaS(s) ΔH1=+571.2 kJ/mol
②: BaSO4(s)+4CO(g) ![]() 4CO2(g)+BaS(s) ΔH2 =-118.8 kJ/mol
4CO2(g)+BaS(s) ΔH2 =-118.8 kJ/mol
回答下列问题:
(1)反应①在一定条件下能够自发的原因:_______________;
(2)已知:C(s,石墨)+O2(g) = CO2(g) ΔH3 =-393.5 kJ/mol;
求 CO 的标准燃烧热ΔH4 = _______kJ/mol;
(3)图 1 为 1200K下, 恒容密闭容器中重晶石与石墨反应时, c(CO)随时间变化曲线图。 请分析图 1 曲线 c(CO)在 0-t2 区间变化的原因:_________________;
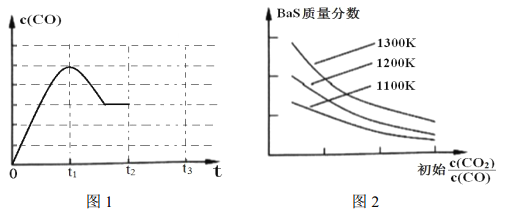
(4)图2为实验测得不同温度下, 反应体系中初始浓度比![]() 与固体中BaS质量分数的关系曲线。 分析图2 曲线, 下列说法正确的有________;
与固体中BaS质量分数的关系曲线。 分析图2 曲线, 下列说法正确的有________;
A.提高 BaSO4 的投料量,可提高 BaS 的产率
B.恒温恒容时, 当混合气体的密度不变, 反应①、②均达到化学平衡状态
C.减小初始浓度比![]() ,有利于增大 BaSO4 的转化率
,有利于增大 BaSO4 的转化率
D.适当升高温度,反应②的平衡左移,对生成 BaS不利
(5)图1 中, t2 时刻将容器体积减小为一半, t3 时刻达到新的平衡, 请在图 1 中画出 t2-t3 区间 c(CO)的变化曲线。________________
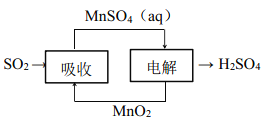
(6)工业生产中产生的 SO2 废气可用如图方法获得H2SO4。写出电解的阳极反应式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】针对如图所示的实验室制取氨气,下列说法正确的是

A.发生装置与用 KClO3 制取O2 的装置相同
B.可以用碱石灰或无水氯化钙干燥制得的氨气
C.可用单孔橡皮塞代替棉花
D.所用的铵盐不能是 NH4NO3,所用的碱可以是 NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把22.4g铁粉完全溶解于某浓度的硝酸中,如反应只收集到0.3 mol NO2和0.2 mol NO,下列说法正确的是
A. 反应后生成的盐只为Fe(NO3)3
B. 反应后生成的盐只为Fe(NO3)2
C. 反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为1∶3
D. 反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为3∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com