
【题目】下列关系正确的是
A. 沸点:新戊烷>2,2-二甲基戊烷>丙烷
B. 密度:CCl4>H2O>甲苯
C. 等质量的物质燃烧耗O2量:乙烷>乙烯>乙炔>甲烷
D. 等物质的量物质燃烧耗O2量:环己烷>苯>苯甲醇
【答案】B
【解析】
A.烷烃中,碳原子个数越多其熔沸点越高,碳原子个数相等时,支链越多其熔沸点越低,所以沸点大小为:2,2﹣二甲基戊烷>新戊烷>丙烷,故A错误;B.水的密度大于甲苯,所以密度大小为:CCl4>H2O>甲苯,故B正确;C.甲烷、乙烷、乙烯、乙炔、最简式分别是CH4、CH3、CH2、CH,这几种最简式中碳原子个数相等、H原子个数不等,H原子个数越多,则H元素含量越高,耗氧量越多,等质量的物质燃烧耗O2量:甲烷>乙烷>乙烯>乙炔,故C错误;D.环己烷(C6H12)、苯(C6H6)、苯甲醇(C7H8O),等物质的量的有机物其耗氧量比为:(6+![]() ):(6+
):(6+![]() ):(7+
):(7+![]() ﹣
﹣![]() )=18:15:17,燃烧耗O2量大小顺序为:环已烷>苯甲醇>苯,故D错误;故答案为B。
)=18:15:17,燃烧耗O2量大小顺序为:环已烷>苯甲醇>苯,故D错误;故答案为B。


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
【题目】酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐或与冰醋酸加热来制取,苯胺与乙酸酐的反应速率远大于与冰醋酸反应的速率,现选用苯胺与乙酸酐为原料制取和提纯乙酰苯胺,该放热反应的原理:
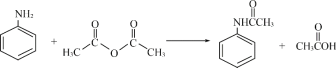
密度(g/mL) | 相对分子质量 | 颜色、状态 | 溶解性 | |
苯胺 | 1.04 | 93 | 无色油状液体 | 微溶于水, 易溶于乙醇、乙醚 |
乙酸酐 | 1.08 | 102 | 无色透明液体 | 遇水缓慢反应生成乙酸 |
乙酰苯胺 | 135 | 无色片状晶体, 熔点 114℃ | 不溶于冷水,可溶于热 水、乙醇、乙醚 |
实验步骤
①取 5.00mL 苯胺,倒入 100mL 锥形瓶中,加入 20mL 水,在旋摇下分批加入 6.00mL 乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至 150mL 烧杯中,加入适量水配制成 80℃的饱和溶液,再加入过量 20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸 3~5min,趁热过滤,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品。
请回答:
(1)苯胺与冰醋酸反应制备乙酰苯胺的化学反应方程式____________________________________。
(2)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是____________。
A.反应快结束时的充分搅拌 B.旋摇下分批加入 6.0mL 乙酸酐
C.玻璃棒将块状物研碎 D.加 20mL 水
(3)在步骤②中对粗产品进行洗涤可能需要用到以下操作:a.加入洗涤剂至浸没固体;b. 洗涤剂缓慢通过;c.洗涤剂快速通过;d.关小水龙头;e.开大水龙头;f.重复 2~3 次。请选出正确的操作并排序_____。(操作可重复使用)
(4)加入过量 20%的水的目的是_____。
(5)下列关于步骤③说法不正确的是__________________________。
A. 活性炭吸附有色物质,可以提高产率
B. 冷却时,冰水浴冷却比室温冷却更易得到大颗粒晶体便于抽滤
C. 抽滤用如图装置,为防止倒吸,结束时可先关闭抽气泵,后打开活塞 a
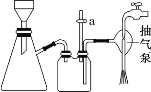
D. 洗涤完成后应将布氏漏斗从吸滤瓶上取下,左手握布氏漏斗,倒转,用右手“拍击”左手, 使固体连同滤纸一起落入洁净的表面皿上,揭去滤纸,再对固体做晾干处理
(6)最后测得纯乙酰苯胺固体 5.40g,该实验的产率为_____(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族;E元素原子L层电子数是K层和M层电子数之和。
(1)写出元素符号:A______ , B______ ,C______ ,D______ ,E__________。
(2)画出E的阴离子的结构示意图:_____________;
(3)A单质和C单质在一定条件下反应生成化合物X,该反应的化学方程式为_______________。向X的水溶液中滴入酚酞溶液,会观察到________________________________________。
(4)将9g B单质在足量的D单质中燃烧,所得气体通入1L 1moL-1 NaOH溶液中,完全吸收后,溶液中大量存在的离子是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种短周期元素,原子序数依次增大,B、C同周期,A、D同主族且A为非金属性最强的元素,C的原子结构示意图为![]() ,A、B可形成BA2型化合物。据此填空:
,A、B可形成BA2型化合物。据此填空:
(1)C的元素名称为____,其气态氢化物的化学式为_____。
(2)A、B、C、D四种元素的原子半径由大到小的顺序为___(用元素符号表示)。
(3)B和D的最高价氧化物对应的水化物反应的离子方程式是_____。
(4)某同学根据元素周期律推知:A元素和D元素最高价氧化物对应的水化物酸性前者强。该同学的推断是否正确?____,请说明理由:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
元素 | 相关信息 |
X | X的价电子排布式为nsnnpn |
Y | Y的负一价离子的电子层结构都与氩相同 |
Z | 常温常压下,Z单质是淡黄色固体,常在火山口附近沉积 |
W | W原子共有6个价电子,其中五个价电子位于第三能层d轨道 |
(1)Z在元素周期表中的位置 _______________________,Z的氢化物空间构型是________
(2)在H—Y、H—Z两种共价键中,键的极性较强的是____________(用相应的元素符号表示该共价键)。
(3)XZ2分子中X以________方式杂化。
(4)写出W元素的原子核外电子排布式___________________________________。
(5)Y元素和Na形成晶体的部分结构可用下图中的_________来表示(填序号)。
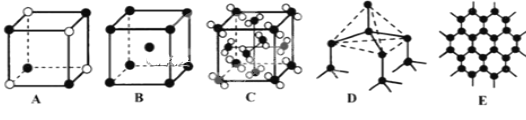
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图回答有关问题。
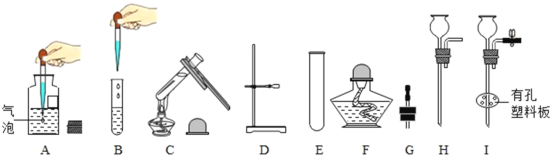
(1)仪器E的名称为___________。
(2)图A~C是常见实验基本操作。其中正确的是___________(填序号);请选择一个有错误的操作写出改正方法:_________________________________________________________________________。
(3)选择仪器D~I完成下列实验操作:
①用KMnO4制备O2,应选仪器________(填序号),其化学反应方程式为_________________________________;
②用大理石与稀盐酸反应制备CO2并使反应随时发生或停止,应选仪器___________,其反应方程式为______________________。
(4)如图是以锌粒和稀硫酸反应制备H2,并用排水法收集。请把图补画完整____________。
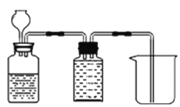
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应使用催化剂后,其反应过程中能量变化如图所示。下列说法错误的是
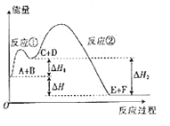
A. △H=△H1-△H2
B. 该反应的总反应为放热反应
C. 使用催化剂,不能改变反应进行的方向
D. 反应①是吸热反应,反应②是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用电子式表示H2O和MgBr2的形成过程:
H2O_________
MgBr2__________
(2)写出CO2、Na2O2、H2O2的电子式:
CO2___________Na2O2________ H2O2________
(3)A+、B+、C-、D、E 5种离子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:
A.A++ C- → D + E b.B++ C- → 2D 。据此回答下列问题:
①写出A反应的离子方程式________;
②写出A+、C-离子的电子式:A+________ C-__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法标出电子转移的方向和数目
①Cl2+SO2 +2H2O=H2SO4 +2HCl ____________________
②2Na2O2+2H2O=4NaOH+O2↑____________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com