
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用.其工作流程如下:
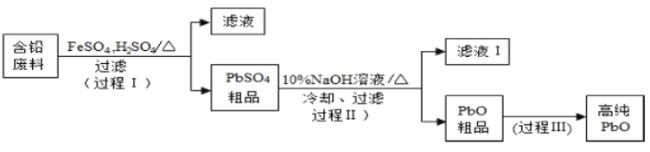
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是_______________。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++PbO2+4H++![]() ═2Fe3++PbSO4+2H2O
═2Fe3++PbSO4+2H2O
ii:…
①写出ii的离子方程式:_______________。
②下列实验方案可证实上述催化过程,将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红;
b._______________。
(3)过程Ⅱ的目的是脱硫.滤液Ⅰ经处理后可在过程Ⅱ中重复使用,其目的是_______________(选填序号)。
A.减小Pb的损失,提高产品的产率
B.重复利用NaOH,提高原料的利用率
C.增加Na2SO4浓度,提高脱硫效率
【答案】Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O 2Fe3++Pb+
2PbSO4+2H2O 2Fe3++Pb+![]() ═PbSO4+2Fe2+ 取a中红色溶液少量,加入过量Pb,充分反应后,红色褪去 AB
═PbSO4+2Fe2+ 取a中红色溶液少量,加入过量Pb,充分反应后,红色褪去 AB
【解析】
根据工艺流程分析可知,过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4和水,过滤后得到PbSO4的粗品,向粗品中加入10%的NaOH溶液,发生反应PSO4+2NaOH=PbO+Na2SO4+H2O,冷却过滤后得到PbO的粗品,经过程Ⅲ得到高纯度的PbO,据此分析解答问题。
(1)结合工艺流程图,过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4和水,化学方程式为:Pb+PbO2+2H2SO4=Fe2+=![]() 2PbSO4+2H2O;
2PbSO4+2H2O;
(2)①催化剂参加反应,改变反应历程,降低反应活化能,加快反应速率,而本身的质量和化学性质在反应前后保持不变,i中Fe2+被氧化为Fe3+,ii中Fe3+被还原成Fe2+,离子方程式:2Fe3++Pb+![]() ═PbSO4+2Fe2+;
═PbSO4+2Fe2+;
②取a中红色溶液少量,溶液中存在平衡,Fe3++SCN―=Fe(SCN)3加入过量Pb,Fe3+ 被还原成Fe2+,平衡逆向移动,充分反应后,红色褪去;
(3)过程Ⅱ脱硫过程中发生的反应为PSO4+2NaOH=PbO+Na2SO4+H2O,由于PbO能溶解于NaOH溶液,因此滤液I中含有Pb元素,重复使用滤液I可减少PbO的损失,且滤液I中过量的NaOH可以重新利用,提高原料的利用率,故选AB。


科目:高中化学 来源: 题型:
【题目】25℃时,用NaOH调节0.1molL-1 H2C2O4溶液的pH,假设不同pH下均有![]() ,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是( )
,使用数字传感器测得溶液中各含碳微粒的物质的量浓度随pH的变化曲线如图。下列有关分析正确的是( )
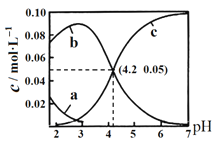
A.曲线b代表H2C2O4浓度随pH的变化
B.HC2O4- ![]() C2O42-+ H+ K = 1×10-4.2
C2O42-+ H+ K = 1×10-4.2
C.pH从4到6时主要发生反应的离子方程式为2OH- + H2C2O4 = 2H2O + C2O42-
D.当溶液pH = 7 时:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知AX3的熔点和沸点分别为-93.6℃和76℃。在常温常压条件下,AX3与X2气体反应生成1molAX5固体,放出热量123.8kJ。该反应的热化学方程式为_______________。
(2)在25℃、101kPa下,一定质量的无水乙醇(C2H5OH)完全燃烧时放出热量QkJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为_______________。
(3)NaBH4(s)与H2O(l)反应生成NaBO2(s)和氢气,在25℃、101kPa下,已知每消耗3.8gNaBH4(s)放热21.6kJ,该反应的热化学方程式是_______________。
(4)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。已知:E(H—H)=436kJmol-1,E(Cl—Cl)=243kJmol-1,E(H—Cl)=432kJmol-1。则H2(g)+Cl2(g) =2HCl(g) ΔH=_______________。
(5)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化的示意图,请计算每生成1molNH3(g)放出热量为_______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中一定能大量共存的有几组( )
①pH=0的溶液:Na+、I-、NO3-、SO42-
②pH=12的溶液中:CO32-、Na+、NO3-、S2-、SO32-
③水电离的H+浓度10-12molL-1的溶液中:Cl-、CO32-、NO3-、NH4+、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-
A.1组B.2组C.3组D.4组
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有物质的量浓度均为0.1molL-1的①NH4Cl溶液,②NaCl溶液,③HCl溶液各20mL,下列说法错误的是( )
A.三种溶液中c(Cl-)的关系是①=②=③
B.若将三种溶液稀释相同的倍数,pH变化最小的是②
C.三种溶液中由水电离出的c(H+)的关系是①<②<③
D.若向三种溶液中分别加入20mL0.1molL-1的NaOH溶液后,pH最小的是③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是![]() ,铝、炭黑及其他杂质,回收利用的流程如图1:
,铝、炭黑及其他杂质,回收利用的流程如图1:
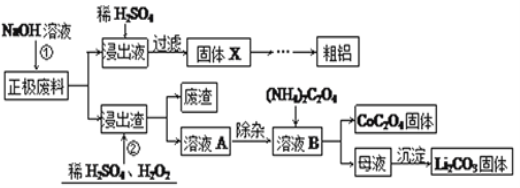
图1
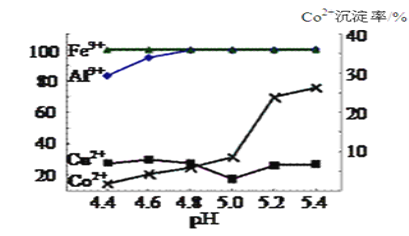
图2
已知A溶液主要的金属离子是![]() 、
、![]() ,还含有少量
,还含有少量![]() 、
、![]() 、
、![]() .
.
![]() 步骤
步骤![]() 中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
![]() 步骤
步骤![]() 中
中![]() 固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
![]() 实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
![]() 母液中含量最大三种离子是 ______ ;
母液中含量最大三种离子是 ______ ;
![]() 从1000g锂离子电池正极材料
从1000g锂离子电池正极材料![]() 元素含量为
元素含量为![]() 中可回收
中可回收![]() 质量为 ______
质量为 ______ ![]() 已知回收率为
已知回收率为![]() ,
,![]() 的化学式量为74).
的化学式量为74).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH-ΔΗ>0,下列叙述正确的是( )
H++OH-ΔΗ>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体NaOH,平衡逆向移动,c(OH-)降低
D.向水中加入少量固体NaCl,pH变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下有H2RO4=H++HRO4-、HRO4-H++RO42-,现有物质的量浓度都为0.1molL-1的三种溶液:①NaHRO4溶液;②H2RO4溶液;③Na2RO4溶液。下列说法中正确的是( )
A.②和③等体积混合后的溶液中:c(Na+)=c(HRO4-)+c(H2RO4)+c(RO42-)
B.100mL①溶液中:n(HRO4-)+n(RO42-)+n(OH-) -n(H+)=0.01mol
C.①和②等体积混合后的溶液中离子浓度大小顺序为c(H+)>c(HRO4-)>c(Na+)
D.若①和③等体积混合后,会抑制水的电离,则HRO4-的电离程度肯定大于RO42-的水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是

A. 反应①为取代反应,有机产物与水混合浮在上层
B. 反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C. 反应③为取代反应,有机产物是一种烃
D. 反应④中1 mol苯最多与3 mol H2发生加成反应,因为每个苯分子含有三个碳碳双键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com