
【题目】碳及其化合物在能源、材料等方面具有广泛的用途。回答下列问题:
(1)碳酸和草酸均为二元弱酸,其电离分为两步进行,已知其电离常数的有关数据如下表:向Na2CO3溶液中滴加草酸溶液,开始时所发生反应的离子方程式为 。
H2CO3 | H2C2O4 | |
K1 | 4.2×10-7 | 5.4×10-2 |
K2 | 5.6×10-11 | 5.4×10-5 |
(2)常温时,C和CO的燃烧热△H分别为-394.0 kJ·mol-1、-283.0 kJ·mol-1,该条件下C转化为CO的热化学方程式为 。
(3)氢气和一氧化碳在一定条件下可合成甲醇,反应如下
2H2(g)+CO(g)![]() CH3OH(g) △H=Q kJ·mol-1。
CH3OH(g) △H=Q kJ·mol-1。
①该反应在不同温度下的化学平衡常数(K)如下表:
温度(℃) | 250 | 300 | 350 |
K(L2·mol-1) | 2.041 | 0.270 | 0.012 |
由此可判断Q 0(填“>”、“=”或“<”)
②一定温度下,将6 mol H2和2mol CO充入到体积为2 L的密闭容器中,10 min时反应达到平衡状态,此时测得c(CO)=0.2 mol·L-1,该温度下的平衡常数K= 。0~10 min内,反应速率v(CH3OH)= 。
③在两个密闭容器中分别都充入20 mol H2和10 mol CO,测得一氧化碳的平衡转化率随温度(T)、压强(p)的变化如下图所示:
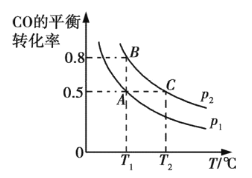
A、B两点压强大小关系:p1 p2(填“>”、“=”或“<”)。若A点对应容器的容积为20 L,则B点对应的容器的容积为 L。
【答案】(1)H2C2O4+2CO32-=2HCO3-+C2O42-(2分)
(2)2C(g)+O2(g)=2CO(g) △H=-222.0kJ·mol-1(2分)
(3)①<(1分) ②2.041L2·mol-2(2分) 0.08mol·L-1·min-1(2分)③<(1分)4(2分)
【解析】
试题分析:(1)由图表可知草酸的一级电离、二级电离均大于碳酸的一级、二级电离,即HC2O4-的酸性比H2CO3强,则向Na2CO3溶液中滴加草酸溶液,开始时所发生反应的离子方程式为H2C2O4+2CO32-=2HCO3-+C2O42-;
(2)①C(s)+O2(g)═CO2(g);△H=-394kJ/mol
②CO(g)+1/2O2(g)=CO2(g)△H=-283.0kJ/mol
依据盖斯定律,①-②得可得:C燃烧生成CO的热化学方程式为:
C(s)+1/2O2(g)=CO (g)△H=-111.kJ/mol,
即:2C(g)+O2(g)—2CO(g) △H=-222.0kJ·mol-1;
(3)①温度升高,平衡常数减小,可知反应逆向进行,说明正反应为放热反应,即Q<0;②10 min时反应达到平衡状态,此时测得c(CO)=0.2 mol·L-1,则CO的变化浓度为2mol/2L-0.2 mol·L-1=0.8mol/L,可知H2的变化浓度为1.6mol/L,CH3OH的变化浓度为0.8mol/L,平衡时H2的浓度为6mol/2L-1.6mol/L=1.4mol/L,则该温度下的平衡常数K=c(CH3OH)÷[c(CO)×c2(H2)]=0.8÷(0.2×1.42)=2.041,0~10 min内,反应速率v(CH3OH)=c(CH3OH)÷10min=0.08mol·L-1·min-1;
③正反应方向为气体体积减小的方向,T1℃时比较CO的转化率,转化率越大,则压强越大,图象中PB转化率大于PA,可知PA<PB;
③A、B两容器温度相同,即化学平衡常数相等,且B点时CO的转化率为0.8,
则 CO(g)+2H2(g)CH3OH(g)
起始(mol):10 20 0
转化(mol):8 16 8
平衡(mol):2 4 8
设体积为VL,则有K=![]() =4,V=4L。
=4,V=4L。


科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为1.0 L的恒容密闭容器中发生反应:2CH3OH(g) ![]() CH3OCH3(g)+H2O(g),下列说法正确的是
CH3OCH3(g)+H2O(g),下列说法正确的是
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量 | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | ||
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A.该反应的正反应为吸热反应
B.达到平衡时,容器Ⅰ中的CH3OH体积分数比容器Ⅱ中的小
C.容器Ⅰ中反应到达平衡所需时间比容器Ⅲ中的长
D.若起始时向容器Ⅰ中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.NaHCO3溶液与盐酸:CO32+2H+![]() H2O+CO2↑
H2O+CO2↑
B.将少量的铜屑放入硝酸银溶液中:Cu+2Ag+![]() Cu2++2Ag
Cu2++2Ag
C.用醋酸溶液除水垢:2H++CaCO3![]() Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
D.Ca(HCO3)2溶液与过量NaOH溶液:Ca2++HCO3+OH![]() H2O+CaCO3↓
H2O+CaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积可变的恒压容器中,反应2NO2(g)N2O4(g)达到平衡后,再向容器内通入一定量NO2,再次达到平衡时,N2O4的体积分数( )
A.不变 B.增大 C.减小 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】9月15日22时04分09秒,长征二号FT2火箭托举着天宫二号空间实验室腾空而起,成功送上太空。该火箭所用的推进燃料偏二甲肼(化学式为C2H8N2),下列说法中正确的是
A.lmolC2H8N2中含有lmolN2
B.偏二甲肼的摩尔质量为60g
C.偏二甲肼是比液氢更环保的燃料
D.偏二甲肼燃烧时能放出大量的热和气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
I.2015年国产C919大型客机正式下线,标志着我国成为世界上少数几个具有自行研制大型飞机的国家之一,标志着我国航空工业进入了新的发展阶段。
(1)飞机的外壳通常采用镁-铝合金材料,铝的价电子排布图为 ,第一电离能:镁 (填“大于”或“小于”)铝。
(2)现代飞机为了减轻质量而不减轻外壳承压能力,通常采用复合材料--玻璃纤维增强塑料,其成分之一为环氧树脂,常见的E51型环氧树脂中部分结构如下图所示:
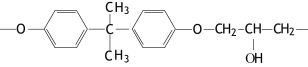

其中碳原子的杂化方式为 ,个数比为 。
II.大型飞机的发动机被誉为航空工业皇冠上的“宝石”。制造过程中通常采用碳化钨做关键部位的材料。
(3)钨元素位于周期表的第六周期第VIB族,请写出其外围电子排布式 ;
(4)下图为碳化钨晶体的一部分结构, 碳原子嵌入金属钨的晶格的间隙,并不破坏原有金属的晶格,形成填隙+固溶体,也称为填隙化合物。在此结构中,其中钨原子有 个,1个钨原子周围距离钨原子最近的碳原子有 个 ,下列金属元素的堆积方式与碳化钨晶胞中碳原子和钨原子所处位置类似的是 。
A. Fe Cu B.Ti Au C.Mg Zn D.Cu Ag
(5)假设该部分晶体的体积为Vcm3,碳化钨的摩尔质量为M g/mol,密度为b g/cm3,则阿伏加德罗常数NA用上述数据可以表示为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂试剂和方法不正确的是
编号 | 被提纯物质(杂质) | 除杂试剂 | 分离方法 |
A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
B | 乙烯(二氧化硫) | 氢氧化钠溶液 | 洗气 |
C | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
D | 苯(苯酚) | 氢氧化钠溶液 | 分液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式BaCO3+2H+=CO2↑+H2O+Ba2+中的H+能代表的物质是( )
①HCl ②H2SO4 ③HNO3 ④NaHSO4 ⑤CH3COOH
A. ②④⑤ B.①④⑤ C.①⑤ D.①③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com