
下列说法正确的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| B.pH=8.3的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C.常温下,pH=2的盐酸溶液中,由水电离出的c(H+)=1.0×10-12 mol/L |
| D.Na2CO3溶液中加水稀释后恢复至原温度,pH和Kw均减小 |
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:单选题
常温下向10 mL 0.1mol·L–1氨水中缓缓加蒸馏水稀释到1 L后,下列变化中正确的是
①电离程度增大;②c(H+)增大;③导电性增强;④ 不变;⑤OH–数目增大,H+数目减小;⑥pH增大;⑦ c(H+)与c(OH–)的乘积减小
不变;⑤OH–数目增大,H+数目减小;⑥pH增大;⑦ c(H+)与c(OH–)的乘积减小
| A.①②④ | B.①⑤⑥ | C.除②外都正确 | D.①④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
0.1mol·L-1Na2S溶液,下列关系正确的是
| A.c(Na+)=2c(S2-) |
| B.c(OH-)="c" (H+)+c (HS-)+2c (H2S) |
| C.c(Na+) >c(S2-) >c (HS-) >c (OH-) |
| D.c(Na+)+c (H+)="2c" (S2-)+c (HS-)+c (OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25℃时,水的电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C.向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱 |
| D.将水加热,KW增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液: c(NH4+)>c(SO42-)>c(Fe2+)>c(H+) |
| B.0.1 mol·L-1 Na2CO3溶液:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C.0.1 mol·L-1 NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(CO32-) |
| D.0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知NH4+与HCHO在水溶液中发生如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O。现有某一铵盐,为测定其氮的质量分数,称取铵盐样品m g,溶于水后,再加入足量HCHO溶液配成100 mL溶液。充分反应后,从中取出V1 mL溶液,用c mol·L-1的NaOH溶液进行中和滴定,恰好用去V2 mL。试求该铵盐中氮元素的质量分数为:
A. | B. | C.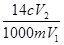 | D. |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中,正确的是
| A.某离子被沉淀完全是指该离子在溶液中的浓度变为0 |
| B.某物质的溶解性为难溶,则该物质的溶解度为0 |
| C.一般来说,溶解度小的难溶物容易转化为溶解度大的难溶物 |
| D.沉淀的生成、溶解和转化其实质都是沉淀发生了溶解平衡的移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,下列溶液中各微粒浓度关系不正确的是( )
| A.PH相等的①CH3COONa②C6H5ONa③NaHCO3溶液中,C(Na+)大小关系:①>③>② |
| B.向氨水中滴加稀硫酸至溶液呈中性:C(NH4+)>C(SO42-)>C(OH-)=C(H+) |
| C.向1L 0.1mol/L的NaOH溶液中通入6.6gCO2:2C(Na+)=3[C(CO32-)+C(HCO3-)+C(H2CO3)] |
| D.CH3COONa溶液中加入少量KNO3后的碱性溶液一定有:C(Na+)+C(H+)=C(CH3COO-)+C(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com