
 甲、乙、丙、丁、戊五种前四周期元素,其中甲乙丙都为非金属元素,在周期表中的位置关系如图1所示.丁、戊两种元素则位于同一周期同一族,而且戊的原子序数比丁大2.
甲、乙、丙、丁、戊五种前四周期元素,其中甲乙丙都为非金属元素,在周期表中的位置关系如图1所示.丁、戊两种元素则位于同一周期同一族,而且戊的原子序数比丁大2.| 1 |
| 8 |
| ||
| ρ |
| 3 |
| ||
| ||
| 4 |
| ||
| 4 |
| 3 |
| ||
| ||
| 4 |
| 3 |
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、等于50mL |
| B、大于50mL |
| C、等于100mL |
| D、大于100mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、KClO3在反应中得到电子 |
| B、1mol KClO3参加反应有2mol电子转移 |
| C、H2C2O4在反应中被氧化 |
| D、ClO2是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | ||
B、甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2
| ||
C、实验室用液溴和苯在催化剂作用下制溴苯: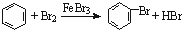 | ||
D、将CO2通入苯酚钠溶液: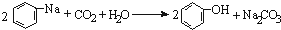 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 同学甲 | 同学乙 | |
| 实验方案 | 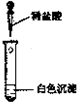 | 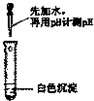 |
| 实验现象 | ||
| 实验结论 | 只有MgCO3 | 只有Mg(OH)2 |
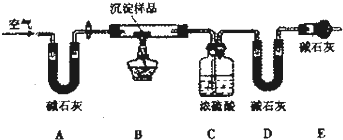
| 实验序号 | 沉淀样品质量 | CO2的物质质量/mol | H2O的物质的量/mol |
| 1 | 3.64 | 0.03 | 0.04 |
| 2 | 7.28 | 0.06 | 0.08 |
| 3 | 10.92 | 0.09 | 0.16 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2的水溶液能导电,所以CO2是电解质 |
| B、BaSO4不溶于水,其水溶液很难导电,所以BaSO4是非电解质 |
| C、液氯不导电,所以液氯是非电解质 |
| D、氯化氢的水溶液能导电,所以氯化氢是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
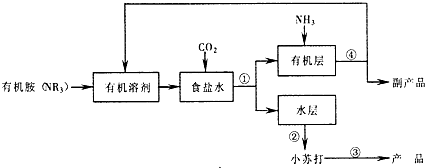
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com