
【题目】25 ℃时,用蒸馏水稀释1 mol/L醋酸,下列各项始终保持增大趋势的是( )
A.![]() B.
B.![]() C.
C.![]() D.c(H+)·c(CH3COO-)
D.c(H+)·c(CH3COO-)
【答案】A
【解析】
稀释过程中醋酸的电离程度增大,溶液中醋酸的物质的量减小、醋酸根离子的物质的量增大,由于在同一溶液中,浓度之比等于物质的量之比,则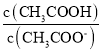 的比值逐渐减小;稀释过程中醋酸、氢离子、醋酸根离子浓度都减小,氢氧根离子浓度增大,则
的比值逐渐减小;稀释过程中醋酸、氢离子、醋酸根离子浓度都减小,氢氧根离子浓度增大,则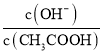 的比值逐渐增大,据此结合水的离子积、电离平衡常数进行判断。
的比值逐渐增大,据此结合水的离子积、电离平衡常数进行判断。
A、稀释过程中醋酸、氢离子、醋酸根离子浓度都减小,氢氧根离子浓度增大,则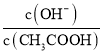 的比值逐渐增大,故A正确;
的比值逐渐增大,故A正确;
B、稀释到一定程度时,氢离子浓度基本不变,则醋酸根离子仍然减小,则![]() 的比值逐渐减小,故B错误;
的比值逐渐减小,故B错误;
C、在稀释过程中醋酸的电离程度增大,溶液中醋酸的物质的量减小、醋酸根离子的物质的量增大,由于在同一溶液中,则![]() 的比值逐渐减小,故C错误;
的比值逐渐减小,故C错误;
D、稀释过程中醋酸、氢离子浓度逐渐减小,则c(H+)·c(CH3COO-)的乘积逐渐减小,故D错误;
故选A。


科目:高中化学 来源: 题型:
【题目】已知NH3气体34 g,求:(注意书写单位)
(1)NH3的物质的量为__________________。
(2)NH3所含原子总数为__________________。
(3)这些NH3溶于150 mL水后形成溶液,密度为0.9281g/cm3,则其溶液的物质的量浓度为_______________。
(4)与___________gOH-有相同的电子数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,一密闭容器中有如下反应:4CO(g)+2NO2(g) ![]() N2(g)+4CO2(g),下列叙述中不能说明该反应一定达到了平衡状态的是
N2(g)+4CO2(g),下列叙述中不能说明该反应一定达到了平衡状态的是
A.单位时间内有amolCO参加反应,同时也有amolCO2参加反应
B.NO2的生成速率:N2的消耗速率=2:1
C.CO的消耗速率:NO2的生成速率=2:1
D.NO2的消耗速率:CO2的消耗速率=1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 在低温下比较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物,还原产物与溶液pH的关系如表:
在低温下比较稳定,酸性比醋酸略强,既有氧化性又有还原性,其氧化产物,还原产物与溶液pH的关系如表:
pH范围 |
|
|
产物 |
| NO、 |
下列有关说法错误的是![]()
A.碱性条件下,![]() 与NaClO反应的离子方程式为
与NaClO反应的离子方程式为![]()
B.向冷的![]() 溶液中通入
溶液中通入![]() 可得到
可得到![]()
C.向冷的![]() 溶液中加入稀硫酸可得到
溶液中加入稀硫酸可得到![]()
D.向冷的![]() 溶液中加入滴有淀粉的氢碘酸,溶液变蓝色
溶液中加入滴有淀粉的氢碘酸,溶液变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H=-746.8kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
2CO2(g)+N2(g) △H=-746.8kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
A. 降低温度 B. 增大压强
C. 升高温度同时充入N2 D. 及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素的原子序数依次增大,W的某种原子无中子,X、Y可形成原子个数比为1∶1的具有漂白性的物质,工业上常用电解饱和YZ溶液来获得Z的单质及其他产品。下列说法正确的是
A. W和X、Y、Z均能形成18电子的分子
B. 上述四种元素的原子半径大小顺序为r(Z)>r(Y)>r(X)>r(W)
C. X、Y之间形成的化合物可能同时含有离子键和非极性共价健
D. W、X、Z三种元素形成的化合物一定是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.01mol/L醋酸中存在下列平衡:CH3COOH![]() H++CH3COO-,若要使溶液的pH和c( CH3 COO-)均减小,可采取的措施是
H++CH3COO-,若要使溶液的pH和c( CH3 COO-)均减小,可采取的措施是
A.适当升高温度B.加入稀盐酸C.加入 CH3COONa固体D.加入少量水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | -33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)甲装置中仪器A的名称为___________。
(2)用甲装置制氯气,MnO4- 被还原为Mn2+,该反应的离子方程式为________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到__________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:
①促进氯气与锡反应;
②_______________________________。
(4)如果缺少乙装置,可能发生的副反应的化学方程式为___________________;己装置的作用是_________________:
A.除去未反应的氯气,防止污染空气
B.防止空气中CO2气体进入戊装置
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有_______________(填标号)。
A. H2O2溶液 B. FeCl3溶液(滴有KSCN) C. AgNO3溶液 D. 溴水
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl4,则SnCl4的产率为________。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示的转化关系,回答下列问题:

(1)写出反应①的离子方程式:______________________________________________;写出反应②的离子方程式:______________________。
(2)推出下列物质的化学式:E____________;I______________。
(3)在上述转化过程中,B、C、F、H的氧化能力由弱到强的顺序为______________________(写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com