
【题目】A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
![]()
![]()
![]()
![]()
![]()
试回答:
(1)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为________;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)________________,检验此C溶液中金属元素价态的操作方法是__________。
(2)若A、B、C为含有金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为________,X的化学式可能为(写出不同类物质)________或________,反应①的离子方程式为____________或_____________________。
【答案】FeCl3防止Fe2+被氧化 2Fe3++Fe=3Fe2+用试管取少量C溶液,滴加KSCN溶液,无颜色变化,再滴加氯水(或硝酸),溶液呈血红色,证明原溶液中有Fe2+存在(答出要点即可)Al(OH)3NaOH(或KOH)HCl(或其他强酸)Al3++3OH-=Al(OH)3↓AlO2-+H++H2O=Al(OH)3↓
【解析】
(1)若X是一种金属单质,X一定为变价金属,A为强氧化性物质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则C中含有氯离子,因此X为Fe,A为Cl2,符合转化关系,B为FeCl3,C为FeCl2。贮存氯化亚铁溶液时,亚铁离子易被氧气氧化生成铁离子,为防止亚铁离子被氧化且不引进新的杂质,应该向氯化亚铁溶液中加入铁粉,离子方程式为2Fe3++Fe=3Fe2+;亚铁离子和硫氰化钾溶液不反应,铁离子和硫氰化钾溶液混合溶液呈红色,此现象是铁离子的特征反应,所以检验氯化亚铁中亚铁离子方法是:用试管取少量C溶液,滴加KSCN溶液,无颜色变化,再滴加氯水(或硝酸),溶液呈血红色,证明原溶液中有Fe2+存在;
(2)若A、B、C为含有金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,可考虑Al的化合物的相互转化,若X是一种强碱例如NaOH(或KOH),A为铝盐,B为Al(OH)3,C为偏铝酸盐,若X是一种强酸例如HCl(或其他强酸),A为偏铝酸盐,B为Al(OH)3,C为铝盐,因此反应①的离子方程式可能为Al3++3OH-=Al(OH)3↓或AlO2-+H++H2O=Al(OH)3↓。


科目:高中化学 来源: 题型:
【题目】室温时,向20 mL 0.1 mol/L的醋酸溶液中不断滴入0.1 mol/L的NaOH溶液,溶液的pH变化曲线如图所示。在滴定过程中,关于溶液中离子浓度大小关系的描述正确的是
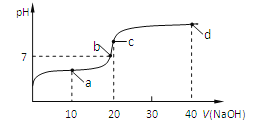
A.a点时:c(CH3COOH) c(CH3COO-) c(H+) c(Na+) c(OH-)
B.b点时:c(Na+)=c(CH3COO-)
C.c点时:c(H+)=c(CH3COOH)+c(OH-)
D.d点时:c(Na+) c(OH-) c(CH3COO-) c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.花生油的主要成分是高级脂肪酸甘油酯,属于高分子化合物
B.汽油和食用油都可以在碱性条件下水解
C.脱脂棉、滤纸的主要成分均为纤维素,完全水解能得到葡萄糖
D.钠与乙醇反应时钠浮在液面上,反应比钠与水反应更剧烈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10﹣8 mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10﹣5 mol/L。若在10mL含有KCl和KI各为0.01mol/L的溶液中,加入16mL 0.01mol/L AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是( )
A. c(K+)>c(NO3﹣)>c(Ag+)>c(Cl﹣)>c(I﹣)
B. c(K+)>c(NO3﹣)>c(Cl﹣)>c(Ag+)>c(I﹣)
C. c(K+)>c(NO3﹣)>c(Ag+)=c(Cl﹣)+c(I﹣)
D. c(NO3﹣)>c(K+)>c(Ag+)>c(Cl﹣)>c(I﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修5:有机化学基础]
甲苯在医药、农药,特别是香料合成中应用广泛,可合成以下物质:
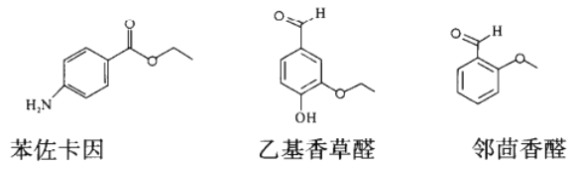
(1)苯佐卡因中含有的碱性官能团为____________(填名称)。
(2)乙基香草醛和邻茴香醛具有相同的亲水基团,该基团可用________(填物理方法)检测。
(3)写出符合下列条件的乙基香草醛的同分异构体的结构简式______(任写两种)。
a.苯环上连接两个互为对位的基团 b.有一个-CH3
c.与FeCl3溶液发生显色反应 d.能发生水解反应
(4)已知:
有机物M为含有两个互为邻位基团的芳香族化合物,且与本佐卡因互为同分异构,其合成路线如下:
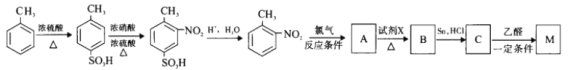
①生成A的“反应条件”为________;
②以上合成路线涉及的7个反应中,属于取代反应的有_________个;
③M的结构简式为___________;
④A→B反应的化学方程式为____________。
(5)参照上述合成路线,以甲苯和甲醇为原料(无机试剂任选),设计制备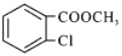 的合成路线___________。
的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用“银-Ferrozine”法检测室内甲醛含量的原理如下:

下列说法错误的是( )
A. 标准状况下,11.2LCO2中含碳氧双键的数目为6.02×1023
B. 30gHCHO被氧化时转移电子数目为4×6.02×1023
C. 反应①的化学方程式为2Ag2O+HCHO=4Ag+CO2+H2O
D. 理论上,吸收HCHO 与消耗Fe3+的物质的量之比为4∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组需要用 18 mol/L 的浓硫酸配制80mL 3.0 mol/L 稀硫酸的实验步骤如下: ① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 稀释 ④ 检漏、 转移、洗涤 ⑤ 定容、摇匀 回答下列问题:
(1)所需浓硫酸的体积是________mL, 量取浓硫酸所用的量筒的规格是_________(用下列编号填空) 。
A.10 mL B.25 mL C.50 mL D.100 mL
(2)第⑤步实验的操作是继续向容量瓶中注入蒸馏水至离刻度线__________, 改用___________向容量瓶中滴加蒸馏水至___________为止。塞紧瓶塞,倒转摇匀并装试剂瓶。
(3)下列情况对所配制的稀硫酸浓度有何影响? (填 “ 偏大 ”“ 偏小 ” 或 “ 无影响”)
①所用的浓硫酸长时间放置在密封不好的容器中 ______________;
②容量瓶用蒸馏水洗涤后残留有少量的水_________________;
③在转入容量瓶前烧杯中溶液未冷却至室温_________;
④取完浓硫酸后洗涤量筒,并把洗涤液倒入烧杯___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com