
【题目】闪锌矿(主要成分ZnS,含Cd、Fe、Cu等元素杂质)是冶炼锌单质的原料,有两种常见的冶炼方式:火法炼锌和湿法炼锌。两种方法均先将闪锌矿加热焙烧,得到以ZnO为主要成分的焙砂,再分别经过两条路线得到单质锌,同时得到副产品。
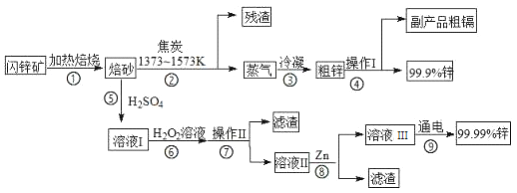
已知:
(I)相关金属单质的熔沸点
金属单质 | Zn | Fe | Cu | Cd |
熔点 (K) | 693 | 1812 | 1356 | 594 |
沸点 (K) | 1180 | 3023 | 2840 | 1040 |
(II)几种离子生成氢氧化物沉淀的pH
Fe3+ | Zn2+ | Cu2+ | Cd2+ | |
开始沉淀pH | l.l | 5.9 | 4.7 | 6.9 |
完全沉淀pH | 3.2 | 8.9 | 6.7 | 9.6 /span> |
请回答下列问题:
(1) 步骤②若焦炭与ZnO(s)反应生成1mol CO时吸收akJ的热量,请写出该反应的热化学方程式___________________________________________________。
(2)步骤④中操作I的分离方法为蒸馏,得到副产品粗镉需控制温度为____左右。
(3)步骤⑦需调节溶液pH为_______,目的是_____________________________。
(4)写出步骤⑧中反应的离子方程式___________________________(任写一个)
(5)步骤⑨以Pt为电极进行电解,阴极的电极反应方程式为________________。
(6)分别取闪锌矿200kg,通过火法炼锌得到Zn的质量为65kg,通过湿法炼锌得到Zn的质量为78kg,闪锌矿中ZnS的质量分数约为___________。
【答案】 ZnO(s) + C(s) ![]() Zn(g) + CO (g) △H = + a kJ/mol 1040 K 3.2 < pH < 5.9 除去溶液中的Fe3+ Zn+Cu2+
Zn(g) + CO (g) △H = + a kJ/mol 1040 K 3.2 < pH < 5.9 除去溶液中的Fe3+ Zn+Cu2+![]() Zn2++Cu Zn+Cd2+
Zn2++Cu Zn+Cd2+![]() Zn2++Cd Zn2++2e—
Zn2++Cd Zn2++2e—![]() Zn 48.5%
Zn 48.5%
【解析】闪锌矿(主要成分ZnS,含Cd、Fe、Cu等元素杂质)加热焙烧,得到以ZnO为主要成分的焙砂,其中还含有其他金属的氧化物。焙砂中的金属氧化物被焦炭还原生成金属单质和残渣,要得到金属蒸气,需要控制温度在1373K~1573K,得到的蒸气中含有锌和镉,通过蒸馏可以分离锌和镉;焙砂中加入硫酸将金属氧化物溶解,再加入双氧水将生成的亚铁盐氧化,调节溶液的酸碱性,使铁离子沉淀,得到的溶液Ⅱ中主要含有Zn2+、Cu2+、Cd2+,再加入锌,将Cu2+、Cd2+还原,得到的溶液Ⅲ中主要含有Zn2+,最后电解得到金属锌。
(1)步骤②若焦炭与ZnO(s)反应生成1molCO时吸收akJ的热量,反应的热化学方程式为
ZnO(s) + C(s) ![]() Zn(g) + CO (g) △H = + a kJ/mol,故答案为:ZnO(s) + C(s)
Zn(g) + CO (g) △H = + a kJ/mol,故答案为:ZnO(s) + C(s) ![]() Zn(g) + CO (g) △H = + a kJ/mol;
Zn(g) + CO (g) △H = + a kJ/mol;
(2)根据相关金属单质的熔沸点数据可知,步骤④中操作I的分离方法为蒸馏,得到副产品粗镉需控制温度为1040K左右,故答案为:1040K;
(3)根据几种离子生成氢氧化物沉淀的pH数据可知,步骤⑦需调节溶液pH除去溶液中的Fe3+,因此需要控制pH在3.2 < pH < 5.9,故答案为:3.2 < pH < 5.9;除去溶液中的Fe3+;
(4)根据上述分析,步骤⑧中反应的离子方程式有Zn+Cu2+=Zn2++Cu、Zn+Cd2+=Zn2++Cd,故答案为:Zn+Cu2+=Zn2++Cu、Zn+Cd2+=Zn2++Cd;
(5)步骤⑨以Pt为电极进行电解,阴极上锌离子发生还原反应生成锌,电极反应方程式为Zn2++2e—=Zn,故答案为:Zn2++2e—=Zn;
(6)根据流程图,闪锌矿中ZnS的质量分数只能通过火法炼锌计算,闪锌矿中ZnS的质量分数为![]() ×100%=48.5%,故答案为:48.5%。
×100%=48.5%,故答案为:48.5%。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】关于下列有机物,说法正确的是
A. CH3CH=CHCH3分子中的四个碳原子在同一直线上
B. 按系统命名法, 的名称为4, 4-二甲基-3-乙基己烷
的名称为4, 4-二甲基-3-乙基己烷
C. 满足分子式为C4H8ClBr的有机物有11种
D.  的结构中含有酯基
的结构中含有酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法不正确的是( )

A. 简单离子半径:M<R
B. 氢化物的稳定性:Y<Z
C. M的氢化物常温常压下为气体
D. X、R、Y、Z均存在两种及两种以上的氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际能源网报道:金属燃料可能成为新能源,可能带来结束化石能源时代的希望,是一种理想的储能方式。下列说法不正确的是( )
A.钠米金属燃料,更易点燃
B.铁作燃料时,可用磁性材料吸引生成物,便于产物分离
C.镁可以通过2Mg+CO2=2MgO+C,达到既节能减碳又释放能量的效果
D.可从海水中提取氯化镁,并使氯化镁分解获得镁并释放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素周期表的说法正确的是( )
A. 元素周期表有8个主族 B. 短周期是指第1、2、3周期
C. ⅠA族的元素全是金属元素 D. 0族原子的最外层电子数均为8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M(NO3)2热分解化学方程式为:2M(NO3)2 ![]() 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是( )
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11.2L的气体,那么M的摩尔质量是( )
A.148g/mol
B.24g/mol
C.74g/mol
D.40g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-=IO3-+5I-+3H2O,下列说法不正确的是( )

A. 右侧发生的电极方程式:2H++2e-=H2↑
B. 电解结束时,右侧溶液中含有IO3-
C. 电解槽内发生反应的总化学方程式KI+3H2O=KIO3+3H2↑
D. 如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种清洁、高效、具有优良的环保性能的可燃物,被称为21世纪的新型能。工业制备二甲醚的生产流程如下:
催化反应室中(压力2.0~10.0MPa,温度300℃)进行下列反应:
(Ⅰ)CO(g)+2H2(g) ![]() CH3OH(g) ΔH1=-90.7kJ·mol-1
CH3OH(g) ΔH1=-90.7kJ·mol-1
(Ⅱ)2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1
(Ⅲ)CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1
(1)催化反应室中的总反应:3CO(g)+3H2(g) ![]() CH3OCH3(g)+CO2(g)
CH3OCH3(g)+CO2(g)
①该反应的反应热△H=__________。
②催化反应室中采用300℃的反应温度,理由是______________________________。
(2)已知:反应(Ⅰ)在300℃时的化学平衡常数为0.27。该温度下将2molCO、3molH2和2molCH3OH充入容积为2L的密闭容器中,此时反应将__________(填“正向进行”、“逆向进行”或“处于平衡状态”)。
(3)上述流程中二甲醚精制的实验操作名称为____________________。
(4)如图为绿色电“二甲醚燃料电池”的工作原理示意图。
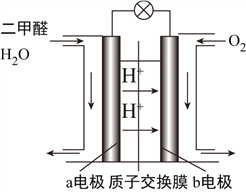
①该电池工作时,H+向__________极移动(填“正”或“负”);
②a电极的电极反应式为________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com