
【题目】完成下列问题
(1)硬脂酸甘油酯的结构简式____________
(2)用系统命名法命名 ![]() 为___________________
为___________________
(3)酸催化条件下制备酚醛树脂的化学方程式____________________________________________
(4)1,3-丁二烯与丙烯等物质的量发生加聚反应的化学方程式______________________________
(5)葡萄糖发生银镜反应的化学方程式_____________________________________
【答案】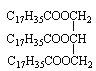 2-乙基-1-丁烯
2-乙基-1-丁烯 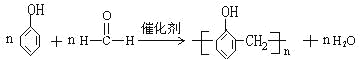 nCH2=CH-CH=CH2+nCH2=CH-CH3
nCH2=CH-CH=CH2+nCH2=CH-CH3![]() [CH2-CH=CH-CH2- CH2-CH(CH3)]n CH2OH(CHOH)4CHO+2Ag(NH3)2OH
[CH2-CH=CH-CH2- CH2-CH(CH3)]n CH2OH(CHOH)4CHO+2Ag(NH3)2OH![]() CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O
【解析】
(1)硬脂酸甘油酯的结构简式为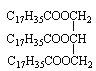 ,故答案为:
,故答案为: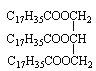 。
。
(2)该有机物为烯烃,含有碳碳双键的最长碳链含有4个碳原子,主链为丁烯;编号从距离双键最近的一端开始,在2号碳上有1个乙基,所以命名为:2-乙基-1-丁烯,
故答案为:2-乙基-1-丁烯。
(3)苯酚羟基邻位上的两个氢原子比较活泼,与甲醛醛基上的氧原子结合为水分子,其余部分连接起来成为高分子化合物即酚醛树脂,反应的方程式可以表示为: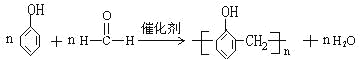 ,
,
故答案为: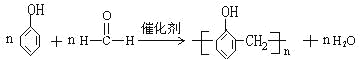 。
。
(4)1,3-丁二烯与丙烯等物质的量发生加聚反应的化学方程式:
nCH2=CH-CH=CH2+nCH2=CH-CH3![]() [CH2-CH=CH-CH2-CH2-CH(CH3)]n,故答案为:
[CH2-CH=CH-CH2-CH2-CH(CH3)]n,故答案为:
nCH2=CH-CH=CH2+nCH2=CH-CH3![]() [CH2-CH=CH-CH2-CH2-CH(CH3)]n。
[CH2-CH=CH-CH2-CH2-CH(CH3)]n。
(5)葡萄糖是多羟基醛,和银氨溶液发生银镜反应,其反应方程式:CH2OH(CHOH)4CHO+2Ag(NH3)2OH![]() CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,故答案为:CH2OH(CHOH)4CHO+2Ag(NH3)2OH
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,故答案为:CH2OH(CHOH)4CHO+2Ag(NH3)2OH![]() CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O。
CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O。


科目:高中化学 来源: 题型:
【题目】在实验室里,常用如图所示装置制取并收集氨气。请回答下列问题:
(1)原理与方法
①制取氨气的化学方程式为__________________________________;
②该收集氨气的方法为________。
A.向上排空气法 B.向下排空气法
(2)装置与操作
按下图组装仪器,进行实验。仪器a的名称为____________。

(3)思考与交流
①欲制取标准状况下4.48 L NH3,至少需要NH4Cl________g;
②实验室制取氨气,还可采用下图中的______(填“A”或“B”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答一下回答以下关于第三周期元素及其化合物的问题。
(1)Na原子核外共有___种不同运动状态的电子,Al的原子结构示意图___。
(2)相同压强下,部分元素氟化物的熔点见表:

试解释上表中氟化物熔点差异的原因:___。
(3)SiF4分子的空间构型为____,SiF4中Si-F键间的键角是____。
(4)在P、S、Cl三种元素形成的氢化物中,热稳定性最大的是____(填氢化物的化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g)![]() C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是( )
C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是( )
A.v(A)=0.2mol/(Ls)B.v(B)=0.6mol/(Ls)
C.v(C)=0.3mol/(Ls)D.v(D)=0.5mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用铝灰(主要成分为Al、Al2O3、AlN、FeO等)制备铝鞣剂[主要成分为Al(OH)2Cl]的一种工艺如下: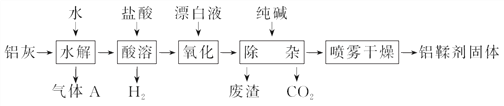
(1)气体A能使湿润的红色石蕊试纸变蓝。铝灰在90 ℃水解生成A的化学方程式为_________________________________________。“水解”采用90 ℃而不在室温下进行的原因是_________________________________________________;
(2)“酸溶”时,Al2O3发生反应的离子方程式为_____________________;
(3)“氧化”时,发生反应的离子方程式为________________________________;
(4)“废渣”成分为________(填化学式);
(5)采用喷雾干燥而不用蒸发的原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3·5H2O),俗称大苏打,是无色透明晶体,易溶于水,易被氧化。是一种重要的化工产品,临床上用于氰化物的解毒剂,工业上也用于纸浆漂白的脱氯剂。某兴趣小组在实验室用如下装置(夹持仪器略去)模拟硫代硫酸钠生产过程。

(1)仪器a的名称为_________。
(2)装置A中发生反应的化学方程式为_____________________________。
(3)为提高产品纯度,应使烧瓶C中Na2S和Na2CO3恰好完全反应,则烧瓶C中Na2S和Na2CO3物质的量之比为____________。
(4)装置B中盛有饱和NaHSO3溶液,装置B的作用是_________、__________。
(5)装置D用于处理尾气,可选用的最合理装置(夹持仪器已略去)为____(填序号)。

(6)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____________,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
已知:Na2S2O3稀溶液与BaCl2溶液混合无沉淀生成。
限选试剂:稀HNO3、稀H2SO4、稀HCl、蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12.某溶液中含有Cl-、Br-和CrO42-浓度均为0.010mol.L-1,向该溶液中逐滴加入0.010mol.L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为( )
A. Cl-、Br-、CrO42- B. CrO42-、Br-、Cl-
C. Br-、Cl-、CrO42- D. Br-、CrO42-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业是最基本的化学工业之一,离子膜电解法为目前普遍使用的生产方法,其生产流程如图1所示:
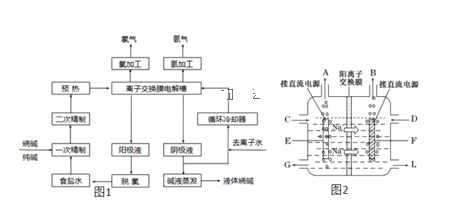
(1)该流程中可以循环的物质是____。
(2)电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有Ca2+、Mg2+、SO42﹣等无机杂质,所以在进入电解槽前需要进行两次精制,写出一次精制中发生的离子方程式___。
(3)图2是工业上电解饱和食盐水的离子交换膜电解槽示意图(阳极用金属钛网制成,阴极由碳钢网制成)。则B处产生的气体是___,E电极的名称是___。电解总反应的离子方程式为____。
(4)从阳极槽出来的淡盐水中,往往含有少量的溶解氯,需要加入8%~9%的亚硫酸钠溶液将其彻底除去,该反应的化学方程式为___。
(5)已知在电解槽中,每小时通过1安培的直流电可以产生1.492g的烧碱,某工厂用300个电解槽串联生产8小时,制得32%的烧碱溶液(密度为1.342吨/m3)113m3,电解槽的电流强度1.45×104A,该电解槽的电解效率为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com