
����Ŀ���о����֣�������ʯī�����������������������ڵ�CaF2��CaO������ʣ�����ͼʾװ�û�ý����ƣ����Ը�Ϊ��ԭ����ԭ���������Ʊ������ѡ�����˵���д������
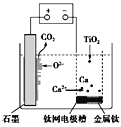
A. ���Ʊ�������ǰ������װ����CaO���������ֲ���
B. �����ĵ缫��ӦʽΪC��2O2����4e��===CO2��
C. ��TiO2�Ƶ�1 mol����Ti�����������·ͨ��2 mol ����
D. ����Ǧ�����������Դ��������������Ӧ����Pb�缫
���𰸡�C
��������
��ͼ��֪�����Դ����������ʯī�缫Ϊ������������Cʧȥ���ӷ���������Ӧ���ɶ�����̼���缫��ӦʽΪC+2O2--4e-�TCO2�������Դ��������������Ϊ������������Ca2+�õ��ӷ�����ԭ��Ӧ����Ca���缫��ӦʽΪ��Ca2++2e-�TCa����Ӧ���ɵĸƻ�ԭ���������Ƶ�Ti����Ӧ�Ļ�ѧ����ʽΪ��2Ca+TiO2=Ti+2CaO��
A�������Ca2+�õ��ӷ�����ԭ��Ӧ����Ca���缫��ӦʽΪ��Ca2++2e-�TCa����Ӧ���ɵĸƻ�ԭ���������Ƶ�Ti����Ӧ�Ļ�ѧ����ʽΪ��2Ca+TiO2=Ti+2CaO�����Ʊ�������ǰ������װ����CaO���������ֲ��䣬��A��ȷ��
B�������Cʧȥ���ӷ���������Ӧ���ɶ�����̼���缫��ӦʽΪC+2O2--4e-�TCO2������B��ȷ��
C�TiO2��TiԪ�صĻ��ϼ�Ϊ+4����TiO2�Ƶ�1 mol����Ti����Ӧת��4 mol ���ӣ������������·ͨ��4 mol ���ӣ���C����
D�PbΪǦ���صĸ�������������������Ӧ����Pb�缫����D��ȷ��
��ѡC��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������屽��ʵ���з����FeBr3��Һ���õ���ı���Һ����ˮFeCl3����������ܴﵽ��Ӧʵ��Ŀ�ĵ���

A.��װ�ü���ȡ������ͼʾͨ��װ��������ʹBr-ȫ��ת��Ϊ�嵥��
B.��װ�ñ���Һʱ�ȴ��¿ڷų�ˮ�㣬��һ�������Ͽڵ����л���
C.������Һ���Ƿ�������ȫ��ȡˮ�������μ���������Һ��������������
D.��װ�ö�����Һ���ˮ����Һ�������д�����������ʱ��ֹͣ���ȣ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����KOHΪ����ʵ�ѭ������п�������ε�طŵ�ʱ���ܷ�ӦΪ2Zn+O2=2ZnO������ʱ���ñý�п������Һ�γɵĽ����������ڲ�������Ӧ����Ӧ�����ɵIJ����潬��������غ���������ⲿ�ĵ����У�����ԭ�������������أ�ѭ������п-�������ε�ع�������ͼ��ͼ��ʾ������˵��������ǣ� ��

A.�ŵ�ʱ�����������ӦΪO2+4e-+2H2O=4OH-
B.�ŵ�ʱ��������л���������̼����
C.���ֹͣ����ʱ��п����������Һ����Ӧ
D.���ʱ������������ӦΪZnO+2e-+H2O=Zn+2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڸ���ʱ�����õĵ��壬Ҳ����;�㷺�Ļ���ԭ�ϡ�þ���ʿ���������������Ͻ���ī�����ȡ���þ�����Ҫ�ɷ�ΪMg2B2O5��H2O��������ȡ�������þ����ȡ����������ͼ��ʾ����֪��ɰ�Ļ�ѧʽΪNa2B4O7��10H2O����þ������þ������ɰ�����в����ķ���������Ҫ�ɷ���MgCO3��������CaO��Al2O3��Fe2O3��FeO��MnO��SiO2�����ʡ���Ҫ��ش����⣺
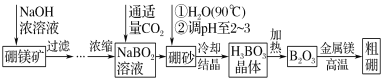
��1��������Mg2B2O5��H2O��B�Ļ��ϼ�Ϊ_____��
��2������ɰ������ˮ����ϡ�����pH��2��3��ȡH3BO3���÷�Ӧ�����ӷ���ʽΪ____��
��3��д����NaClO�Ĺ����з�����Ӧ�����ӷ���ʽ��________��________��
��4������þ���м���������Ϊ�����Ƿ���У�___��(����������������)��������____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���3molA�����1molB����ͨ��һ�ݻ��̶�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g)![]() xC(g)������д���пհף�
xC(g)������д���пհף�
(1)��Ӧ1minʱ���ʣ��1.8molA��C��Ũ��Ϊ0.4mol/L����1min�ڣ�B��ƽ����Ӧ����Ϊ___________��xΪ___________��
(2)����Ӧ��2min�ﵽƽ�⣬ƽ��ʱC��Ũ��___________0.8mol/L(����ڡ�����С�ڡ����ڡ�)
(3)����֪��ƽ��ʱ���������ڻ��������ѹǿΪP�����������ʼѹǿΪP0������P0��P����ʾ��ƽ��ʱ��Ӧ��A��ת����a(A)Ϊ___________��
(4)�ܼӿ췴Ӧ���ʵĴ�ʩ��___________��
�������¶�
������������䣬������������Ar
������ѹ�����䣬�����������Ar
��ʹ�ô���
�ݽ����������Сһ��
(5)�ܹ�˵���÷�Ӧ�ﵽƽ��ı�־��___________��
A. �����ڻ��������ܶȱ��ֲ���
B. �����ڻ�������ѹǿ���ֲ���
C. A��B��Ũ��֮��Ϊ3:1
D. ��λʱ���ڶϿ�3nmolA-A����ͬʱ����nmolB-B��
E. v(A)=3v(B)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��40��ʱ���ڰ���ˮ��ϵ�в���ͨ��CO2���������ӵ�Ũ�ȱ仯������ͼ��ʾ������˵������ȷ����
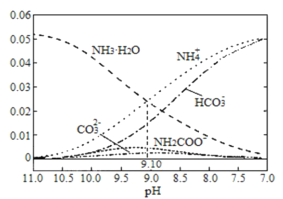
A.40��ʱ��K(NH3��H2O)=10-9.10
B.��ͬpH����Һ�о����ڹ�ϵ��c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)
C.����CO2��ͨ�룬![]() ���ϼ�С
���ϼ�С
D.����ҺpH���Ͻ��ͣ����ɵ��м����NH2COONH4�ֲ���ת��ΪNH4HCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л����������ȷ����( )
A.�ƾ���������ȡ��ˮ�еĵⵥ��
B.���ۡ������ʺ���֬��������Ȼ�л��߷��ӻ�����
C.����ϩ��ȡ������ϩ�ķ�Ӧ����ʽΪnCH2=CHCl![]()
![]()
D.��ϩ�������Ҵ����ܱ����Ը��������Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
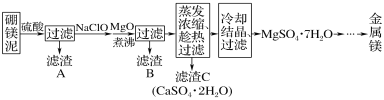
����Ŀ����ͼ���������������Ҵ�������Ļ����ɰ����в�����з��룺
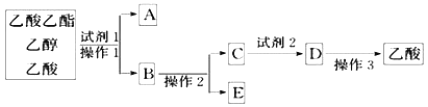
(1)�Լ�1���ѡ��_______��
(2)����1��_______;
(3)�Լ�2���ѡ��_______��
(4)����2��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����������ת����
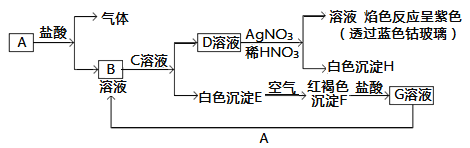
�Իش�
(1)д��B�Ļ�ѧʽ________��D�Ļ�ѧʽ________��
(2)д����Eת���F�Ļ�ѧ����ʽ________________________��
(3)д����KSCN����G��Һ�����ӷ���ʽ________________����G��Һ����A���й����ӷ�Ӧ����ʽ________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com