
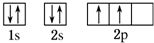
 ,B原子为Si,Si的核外电子排布式为:1s22s22p63s23p2,C为Cl,Cl原子的价电子排布式为:3s23p5,故答案为:
,B原子为Si,Si的核外电子排布式为:1s22s22p63s23p2,C为Cl,Cl原子的价电子排布式为:3s23p5,故答案为: ;1s22s22p63s23p2;3s23p5;
;1s22s22p63s23p2;3s23p5;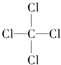 ,其中中心C原子采取 sp3 (杂化方式,是由极性键构成的非极性分子,故答案为:
,其中中心C原子采取 sp3 (杂化方式,是由极性键构成的非极性分子,故答案为: ;sp3;非极性.
;sp3;非极性.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、10.8 g X2O5中含有0.5 mol O,则X的相对原子质量为28 |
| B、4 g某气体含有的分子数为3.01×1023,则2 g该气体在标准状况下的体积是5.6 L |
| C、同温同压下,10 L X2气体跟30 L Y2气体化合生成20 L某Z气体,则Z的化学式为XY2 |
| D、标准状况下,相同质量的N2、O2、Cl2中,体积最大的是Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
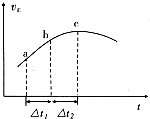 研究氮的氧化物、硫的氧化物、碳的氧化物等大气污染物的处理具有重要意义.
研究氮的氧化物、硫的氧化物、碳的氧化物等大气污染物的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象 |
| B、NaOH溶液和AlCl3溶液相互滴加的现象不同 |
| C、金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属 |
| D、Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与H2O发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离产生的C(H+)=10-13mol/L的溶液中:K+、Na+、SO32-、S2- | ||
| B、1.0mol?L-1KNO3溶液:H+、Fe2+、Cl-、SO42- | ||
C、
| ||
| D、过量氨水中:Ag+、Na+、K+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
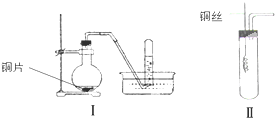 如图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:
如图是铜与稀硝酸反应的两个实验装置图,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com