
【题目】实验室用干燥的H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气)。下列说法不正确的是
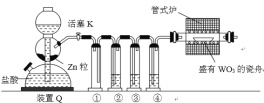
A.①的作用是防倒吸
B.②、③、④中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
C.管式炉中发生反应的化学方程式为:3H2+ WO3![]() W+3H2O
W+3H2O
D.装置Q不能用于二氧化锰与浓盐酸反应制备氯气
【答案】B
【解析】
图示装置利用启普发生器制取氢气,将制得的氢气依次经过一定的溶液进行除杂得到纯净的氢气,经纯净的氢气通入到管式炉中与WO3反应得到金属W,据此分析。
A.反应产生的气体可以与②瓶中的溶液发生反应,容易引起倒吸,引入①装置可以将②瓶倒吸的液体存留在①瓶中,阻止进一步倒吸到发生装置中,A正确;
B.Zn粒中往往含有硫等杂质,因此生成的氢气中可能混有H2S,所以KMnO4溶液除去H2S。另外装置含有空气,高温下能与W反应,焦性没食子酸溶液吸收氧气,最后通过浓硫酸干燥氢气,故②、③、④中依次盛装KMnO4溶液、焦性没食子酸溶液、浓H2SO4,B错误;
C.管式炉中发生氢气还原WO3的反应,WO3被还原为W单质,氢气被氧化为水,反应方程式为3H2+WO3![]() W+3H2O,C正确;
W+3H2O,C正确;
D.二氧化锰与浓盐酸制备氯气的反应需要加热,而启普发生器不能加热,所以不能用于该反应,D正确;
故选B。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料.它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:
SiO2![]() Si(粗)
Si(粗)![]() SiHCl3
SiHCl3![]() Si(纯)
Si(纯)
下列说法正确的是()
A.步骤①的化学方程式为:SiO2+C![]() Si+CO2↑
Si+CO2↑
B.SiO2既能与HF反应,又能与NaOH反应,所以SiO2属于两性氧化物
C.高纯硅是制造太阳能电池的常用材料,二氧化硅是制造光导纤维的基本原料
D.含硅化合物硅酸钠属于盐类,不属于碱,可以保存在磨口玻璃塞试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C为中学化学中常见的单质, A为是生产、生活中用量最大、用途最广的金属单质,室温下B是黄绿色气体,C为无色气体。在一定条件下相互转化的关系如图所示。
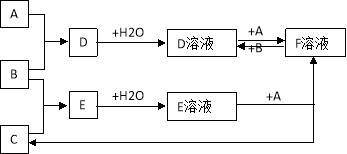
请回答以下问题:
(1)A、B、C分别是什么物质:A是 ,B是 ,C是,F是 (填化学式)
(2)写出A和B生成D的化学方程式: ,向D溶液中加
入 溶液可看到溶液变血红色。
(3)写出F溶液中加入B的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2SO2+O2![]() 2SO3,在一定温度下的定容容器中进行,下列说法正确的是
2SO3,在一定温度下的定容容器中进行,下列说法正确的是
A.反应达到限度时,各反应物和生成物的浓度之比等于化学计量数之比
B.反应达到限度时,SO2将全部转化为SO3
C.反应达到限度时,O2物质的量不再改变
D.反应达到限度时,v(正反应)=v(逆反应)=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明N2O与CO在Fe+作用下发生可逆反应的能量变化及反应历程如图所示。下列说法不正确的是
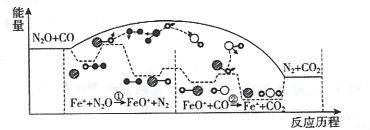
A.反应中Fe+是催化剂,FeO+是中间产物B.总反应速率由反应②的速率决定
C.升高温度,总反应的平衡常数K减小D.当有14g N2生成时,转移1mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】救灾物资中的一瓶“84消毒液”的包装说明上有如下信息:含25%NaClO(次氯酸钠)、1000 mL、密度1.19 g/cm3,稀释100倍(体积比)后使用。
请回答下列问题:
(1)上述“84消毒液”的物质的量浓度为___mol/L。
(2)该同学取100 mL上述“84消毒液”,稀释后用于消毒,稀释100倍后的溶液中c(Na+)=___mol/L(假设稀释后溶液密度为1.0 g/cm3),该消毒液长时间放置在空气中能吸收标准状况下CO2的体积为____L。(已知:酸性:H2CO3> HClO> HCO3-)
(3)灾区志愿者根据上述“84消毒液”的包装说明,欲用NaClO固体(NaClO易吸收空气中的H2O、CO2)配制480 mL含25%NaClO的消毒液。下列说法正确的是___。
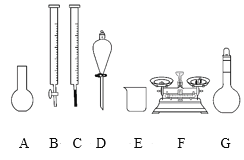
a.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
b.容量瓶用蒸馏水洗净后,要烘干才能用于溶液的配制
c.利用购买的商品NaClO来配制可能会导致结果偏低
d.需要NaClO固体的质量为143g
(4)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-bmg/L,现用ClO2将CN-氧化,只生成两种无毒气体,其离子反应方程式为_____,处理100 m3这种污水,至少需要ClO2_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4用于治疗缺铁性贫血。为探究硫酸亚铁的分解产物,按如下装置进行实验。打开K1和K2,缓慢通入N2,加热。实验后反应管中残留固体为红色粉末。分析实验回答下列问题:
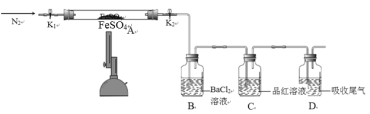
(1)加热前通入N2的目的是__________。
(2)实验过程中可观察到装置B中的现象为_____。C中观察到品红溶液褪色,则可证明混合气体中含有的物质是_____。
(3)反应后A中残留红色粉末的用途有__________(任写一条)。
(4)写出FeSO4高温分解反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________。
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度________________
(2)该溶液的质量分数_________________________
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
溶质的质量分数 | 溶液的密度(g·cm-3) | |
第一份溶液 | w1 | ρ1 |
第二份溶液 | w2 | ρ2 |
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=________。(用以上字母表示)
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3___w4;若ρ1<ρ2,w3______w4(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究小组设计用含氯的有机物A合成棉织物免烫抗皱整理剂M的路线如下(部分反应试剂和条件未注明):
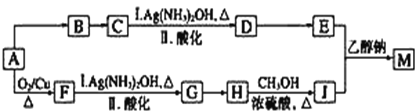
已知:①E的分子式为C5H8O4,能发生水解反应,核磁共振氢谱显示E分子内有2种不同化学环境的氢原子,其个数比为3∶1;
②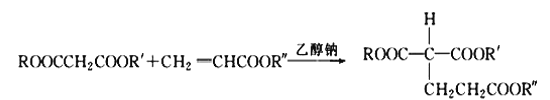 (R、R′、R″代表相同或不相同的烃基)。
(R、R′、R″代表相同或不相同的烃基)。
(1)A分子中的含氧官能团的名称是_________。
(2)A→B反应所需的试剂是_________。
(3)G→H反应的化学方程式是______。
(4)已知1 mol E与2 mol J反应生成1 mol M,则M的结构简式是________。
(5)E的同分异构体有下列性质:①能与NaHCO3反应生成CO2;②能发生水解反应,且水解产物之一能发生银镜反应,则该同分异构体共有_______种,其中任意1种的结构简式是__________。
(6)J可合成高分子化合物,该高分子化合物的结构简式是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com