
下列电解质溶液中有关浓度关系不正确的是
| A.浓度均为0.1 mol/L的HF、KF混合溶液中:2c(H+)+c(HF)=2c(OH-)+c(F-) |
| B.0.1 mol/L的Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C.常温下,pH=5的NaHSO3溶液中,水电离出的c(H+)=1.0×10-9 mol/L |
| D.铵根离子浓度均为0.1 mol/L的 ①NH4Cl、②NH4Al(SO4)2、③NH4HCO3三种溶液的浓度:③>①>② |
B
解析试题分析:A.根据物料守恒可得2c(K+)= c(HF)+c(F-);根据电荷守恒可得c(K+)+ c(H+)= c(OH-)+c(F-)。将第二个式子变形可得c(K+)= c(OH-)+c(F-) -c(H+)。代入第一个式子。整理可得2c(H+)+c(HF)=2c(OH-)+c(F-)。正确。B.0.1 mol/L的Na2CO3溶液中:根据物料守恒可得c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3).错误。C.常温下,pH=5的NaHSO3溶液中,c(H+)=10-5mol/L,c(OH-)=10-14÷10-5=10-9mol/L.在水溶液中只有水电离产生OH-。所以 c(H+)(水)=c(OH-)=10-9 mol/L。正确。D.三个溶液中都存在铵根离子的水解反应:NH4++H2O NH3·H2O+H+。在②中还存在Al3++3H2O
NH3·H2O+H+。在②中还存在Al3++3H2O  Al(OH)3+3H+会对铵根离子水解起抑制作用。所以铵根离子浓度均为0.1 mol/L溶液的浓度①大于②的。在③中还存在HCO3-+H2O
Al(OH)3+3H+会对铵根离子水解起抑制作用。所以铵根离子浓度均为0.1 mol/L溶液的浓度①大于②的。在③中还存在HCO3-+H2O H2CO3+OH-。对铵根离子的水解起促进作用,所以当铵根离子浓度相同时,溶液的浓度:③>①。因此物质是浓度的关系为③>①>②。正确。
H2CO3+OH-。对铵根离子的水解起促进作用,所以当铵根离子浓度相同时,溶液的浓度:③>①。因此物质是浓度的关系为③>①>②。正确。
考点:考查电解质溶液中有关离子浓度关系的知识。主要包括物料守恒、电荷守恒、盐的水解、弱电解质的电离的知识。


科目:高中化学 来源: 题型:单选题
不能用于判断HA是弱电解质(弱酸)的依据是( )
A.浓度相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多
B.pH相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多
C.浓度相等的HCl与HA两溶液,c(H+)HCl约是c(H+)HA的100倍
D.pH相等的HCl与HA两溶液,c(HA)约是c(HCl)的100倍
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知298 K时下列物质的溶度积(单位略)。
| | CH3COOAg | AgCl | Ag2CrO4 | Ag2S |
| Ksp | 2.3×10-3 | 1.77×10-10 | 1.12×10-12 | 6.7×10-15 |
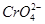 和Cl-的溶液中慢慢滴入AgNO3溶液时,
和Cl-的溶液中慢慢滴入AgNO3溶液时,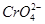 先沉淀
先沉淀查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下pH最小的是下列各项中的( )
| A.pH=0的溶液 | B.0.04 mol·L-1H2SO4 |
| C.0.5 mol·L-1HCl | D.0.05 mol·L-1CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
100℃时,水的离子积为1×10-12 mol2·L-2,若该温度下某溶液中的H+浓度为1×10-7 mol·L-1,则该溶液是( )
| A.酸性 | B.碱性 | C.中性 | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示用一定浓度的NaOH溶液Y滴定10 mL一定物质的量浓度的盐酸X,依据图示推出X和Y的物质的量浓度是下列各组中的( )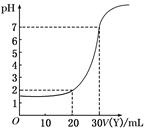
| | A | B | C | D |
| X物质的量浓度/mol·L-1 | 0.12 | 0.04 | 0.03 | 0.09 |
| Y物质的量浓度/mol·L-1 | 0.04 | 0.12 | 0.09 | 0.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对水垢的主要成分是CaCO3和Mg(OH)2而不是CaCO3和MgCO3的解释,说法正确的是( )
| A.Mg(OH)2的溶度积大于MgCO3的溶度积,且在水中发生了沉淀转化 |
| B.Mg(OH)2比MgCO3更难溶,且在水中发生了沉淀转化 |
C.MgCO3电离出的CO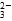 发生水解,使水中OH-浓度减小,对Mg(OH)2沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀 发生水解,使水中OH-浓度减小,对Mg(OH)2沉淀溶解平衡而言,Qc<Ksp,生成Mg(OH)2沉淀 |
D.MgCO3电离出的CO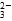 发生水解,促进水中OH-浓度增大,对Mg(OH)2沉淀溶解平衡而言,Qc>Ksp,生成Mg(OH)2沉淀 发生水解,促进水中OH-浓度增大,对Mg(OH)2沉淀溶解平衡而言,Qc>Ksp,生成Mg(OH)2沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关AgCl沉淀的溶解平衡的说法中,正确的是( )
| A.AgCl沉淀生成和溶解不断进行,但速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升高温度,AgCl的溶解度减小 |
| D.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是( )
| A.Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
| B.Cu2++H2S=CuS↓+2H+ |
| C.Zn2++S2-+2H2O=Zn(OH)2↓+H2S↑ |
| D.FeS+2H+=Fe2++H2S↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com