
下列有关AgCl沉淀的溶解平衡的说法中,正确的是( )
| A.AgCl沉淀生成和溶解不断进行,但速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.升高温度,AgCl的溶解度减小 |
| D.向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度不变 |
科目:高中化学 来源: 题型:单选题
向20 mL 0.5 mol·L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中错误的是( )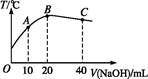
| A.醋酸的电离平衡常数:B点>A点 |
| B.由水电离出的c(OH-):B点>C点 |
| C.从A点到B点,混合溶液中可能存在:c(CH3COO-)=c(Na+) |
| D.从B点到C点,混合溶液中一直存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列电解质溶液中有关浓度关系不正确的是
| A.浓度均为0.1 mol/L的HF、KF混合溶液中:2c(H+)+c(HF)=2c(OH-)+c(F-) |
| B.0.1 mol/L的Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C.常温下,pH=5的NaHSO3溶液中,水电离出的c(H+)=1.0×10-9 mol/L |
| D.铵根离子浓度均为0.1 mol/L的 ①NH4Cl、②NH4Al(SO4)2、③NH4HCO3三种溶液的浓度:③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Na2S溶液中各种离子的物质的量浓度关系不正确的是( )
| A.c(Na+)>c(S2-)>c(OH-)>c(HS-) | B.c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-) |
| C.c(Na+)=2c(HS-)+2c(S2-)+2c(H2S) | D.c(OH-)=c(H+)+ c(HS-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.pH=4的醋酸中:c(H+)= 4.0molL-1 |
| B.饱和小苏打溶液中:c(Na+)= c(HCO3-) |
| C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)= 1.0×10-2 molL-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.pH=5的NH4 Cl溶液或醋酸中,由水电离出的c(H+)均为10-9 mol/L |
| B.常温时将pH=3的醋酸和pH=ll的NaOH溶液等体积混合后,pH >7 |
| C.在c(H+):c(OH-)=1:l012的溶液中,N a+、I-、NO3-、SO42-能大量共存 |
| D.0.1 mol/L Na2 CO3溶液和0.1 mol/L NaHSO4溶液等体积混合,溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某温度时,BaSO4在水中的沉淀溶解平衡曲线如下图所示。下列说法正确的是( )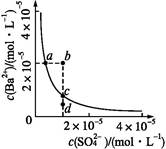
提示:BaSO4(s) Ba2+(aq)+S(aq)的平衡常数Ksp=c(Ba2+)·c(S),称为溶度积常数。
Ba2+(aq)+S(aq)的平衡常数Ksp=c(Ba2+)·c(S),称为溶度积常数。
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于盐类水解反应的应用说法正确的是( )
| A.可以把FeCl3固体直接溶于水制FeCl3溶液 |
| B.热的纯碱溶液去油污效果好 |
| C.Al(NO3)3溶液与K2S溶液混合后无明显现象 |
| D.Mg粉投入到饱和NH4Cl溶液中无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲酸的下列性质中,可以证明它是弱电解质的是( )
| A.1 mol/L甲酸溶液的c(H+)=0.01 mol/L |
| B.甲酸能与水以任何比例互溶 |
| C.10 mL 1 mol/L甲酸恰好与10 mL 1 mol/L NaOH溶液完全反应 |
| D.甲酸溶液的导电性比盐酸的弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com