
不能用于判断HA是弱电解质(弱酸)的依据是( )
A.浓度相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多
B.pH相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多
C.浓度相等的HCl与HA两溶液,c(H+)HCl约是c(H+)HA的100倍
D.pH相等的HCl与HA两溶液,c(HA)约是c(HCl)的100倍
A
解析试题分析:HCl与HA都是一元酸,HCl是强酸。无论HA是强酸还是弱酸,若浓度相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl都一样多。错误。B.pH相等的HCl与HA两溶液,则c(H+)相同。当它们体积相同时,n(H+)相同。二者跟镁反应生成氢气HA比HCl多,说明HA能够产生的n(H+)。则HA为弱酸。当反应消耗H+后,HA H++A-正向移动,产生更多的H+。因此放出的氢气不HCl多。正确。C.HCl与HA都是一元酸。HCl是强酸。若HA是强酸,则当浓度相等的HCl与HA两溶液,c(H+)HCl=,c(H+)HA。若c(H+)HCl约是c(H+)HA的100倍,则c(H+)HA是c(H+)HCl的100分之一。因此证明HA为弱酸。正确。D.若HA是强酸, pH相等的HCl与HA两溶液,c(HA)= c(HCl).=10-pH。若c(HA)约是c(HCl)的100倍,则证明HA只有一部分发生电离。因此HA是弱酸。正确。
H++A-正向移动,产生更多的H+。因此放出的氢气不HCl多。正确。C.HCl与HA都是一元酸。HCl是强酸。若HA是强酸,则当浓度相等的HCl与HA两溶液,c(H+)HCl=,c(H+)HA。若c(H+)HCl约是c(H+)HA的100倍,则c(H+)HA是c(H+)HCl的100分之一。因此证明HA为弱酸。正确。D.若HA是强酸, pH相等的HCl与HA两溶液,c(HA)= c(HCl).=10-pH。若c(HA)约是c(HCl)的100倍,则证明HA只有一部分发生电离。因此HA是弱酸。正确。
考点:考查判断HA是弱电解质(弱酸)的依据的知识。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:单选题
下列电解质溶液中有关浓度关系不正确的是
| A.浓度均为0.1 mol/L的HF、KF混合溶液中:2c(H+)+c(HF)=2c(OH-)+c(F-) |
| B.0.1 mol/L的Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C.常温下,pH=5的NaHSO3溶液中,水电离出的c(H+)=1.0×10-9 mol/L |
| D.铵根离子浓度均为0.1 mol/L的 ①NH4Cl、②NH4Al(SO4)2、③NH4HCO3三种溶液的浓度:③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Na2S溶液中各种离子的物质的量浓度关系不正确的是( )
| A.c(Na+)>c(S2-)>c(OH-)>c(HS-) | B.c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-) |
| C.c(Na+)=2c(HS-)+2c(S2-)+2c(H2S) | D.c(OH-)=c(H+)+ c(HS-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.pH=4的醋酸中:c(H+)= 4.0molL-1 |
| B.饱和小苏打溶液中:c(Na+)= c(HCO3-) |
| C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)= 1.0×10-2 molL-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
A.0.1 mol·L-1的醋酸溶液加水稀释,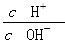 减小 减小 |
| B.体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量),后者用时少 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 |
| D.常温下,V1 L pH=11的NaOH溶液与V2 L pH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
以MnO2为原料制得的MnCl2溶液中常含有少量Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl2。根据上述实验事实,可推知MnS具有的相关性质是( )
| A.具有吸附性 |
| B.溶解度与CuS、PbS、CdS等相同 |
| C.溶解度大于CuS、PbS、CdS |
| D.溶解度小于CuS、PbS、CdS |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Mg(OH)2在水中达到溶解平衡:Mg(OH)2(s) Mg2++2OH-,下列哪种情况可使Mg(OH)2(s)的量减少( )
Mg2++2OH-,下列哪种情况可使Mg(OH)2(s)的量减少( )
| A.加入MgCl2溶液 | B.加入少量NaOH |
| C.加入NH4NO3溶液 | D.加入K2S溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于盐类水解反应的应用说法正确的是( )
| A.可以把FeCl3固体直接溶于水制FeCl3溶液 |
| B.热的纯碱溶液去油污效果好 |
| C.Al(NO3)3溶液与K2S溶液混合后无明显现象 |
| D.Mg粉投入到饱和NH4Cl溶液中无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知在常温下测得浓度均为0.1 mol·L-1的下列三种溶液的pH:
| 溶质 | NaHCO3 | Na2CO3 | NaCN |
| pH | 9.7 | 11.6 | 11.1 |
 减小
减小查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com