
【题目】常温下,向20mL的某稀H2S04溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴人氨水体积变化如图。下列分析正确的是( )
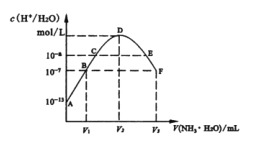
A.稀硫酸的浓度为0.1mol/L
B.C点溶液pH=14-a
C.E溶液中存在:c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D.B到D、D到F所加氨水体积一定相等
【答案】C
【解析】
试题分析:A、根据20mL的稀H2S04溶液中,水电离出的氢离子浓度是10-13,结根据水的离子积得到硫酸电离出的氢离子浓度是0.1mol/L,稀硫酸的浓度为0.05mol/L,A错误;B、C点的溶液中水电离出的氢离子浓度是10-a,此时的溶液显示酸性,铵根离子水解所致,所以水电离程度增大,pH=a,B错误;C、E溶液显示酸性,硫酸铵和氨水的混合物,得到的溶液中铵根离子的水解程度较强,所以c(NH4+)>c(SO42-)>c(H+)>c(OH-),C正确;D、B到D水的电离程度增加,是硫酸铵生成阶段,铵根离子水解显酸性,促进水的电离,D到F,是因为加入的氨水抑制水的电离,使水的电离程度逐渐减小,两个阶段铵根离子的水解程度不一样,所以加氨水体积不相等,D错误.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】下列有关细胞中元素和化合物的叙述,正确的是( )
A. Mg虽然是微量元素但在光合作用中起很重要的作用,不可缺少
B. 脂肪分子中含氢比糖类多,是主要的能源物质
C. 氨基酸脱水缩合产生水,水中的氧来自氨基酸的羧基
D. RNA和DNA主要组成元素的种类不同,碱基种类不完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列影响化学反应速率的因素中,是通过改变活化分子百分数来实现的是
①改变气体物质的浓度 ②改变气体的压强
③加入催化剂 ④改变气体的温度
A.只有①② B.只有③④ C.只有①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应热的叙述中正确的是
①已知2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为△H=-241.8 kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)![]() Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(s) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:
共价键 | C—C | C===C | C—H | H—H |
键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
上表数据可以计算出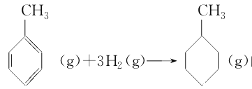 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2固体时,放出的热量相等
⑥25℃,101 kPa时,1 mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
A.①②③④ B.③④⑤ C.④⑤ D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是( )
A.已知2C(s)+2O2(g)=2CO2(g) ΔH=a kJ·mol-1;2C(s)+O2(g)=2CO(g) ΔH=b kJ·mol-1,则a>b
B.由H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ
C.由C(石墨)=C(金刚石) ΔH=+1.9 kJ·mol-1可知,金刚石比石墨稳定
D.在100 kPa时,1 g H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示。下列有关微生物电池的说法错误的是( )
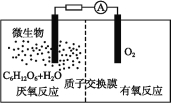
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2=6CO2+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com