
【题目】某元素的微粒37X-的核外电子数为18,则该元素原子的中子数是 ( )
A.17B.18C.19D.20
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】氰化钠是一种重要的基本化工原料,同时也是一种剧毒物质。一旦泄漏需要及时处理,一般可以通过喷洒双氧水或过硫酸钠(Na2S2O8)溶液来处理,以减轻环境污染。
Ⅰ.已知:氰化钠是一种白色结晶颗粒,化学式为NaCN,有剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1)请用最常见的试剂和简单操作设计实验证明N、C元素的非金属性强弱:__________________(只说明操作及现象)。
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的离子方程式是___________________________。
Ⅱ.工业制备过硫酸钠的反应原理如下:
主反应:(NH4)2S2O8+2NaOH![]() Na2S2O8+2NH3
Na2S2O8+2NH3![]() +2H2O
+2H2O
副反应:2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
某化学兴趣小组利用上述原理在实验室制备过硫酸钠,并检测用过硫酸钠溶液处理后的氰化钠废水是否达标排放。
(实验一)实验室通过如图所示装置制备Na2S2O8。
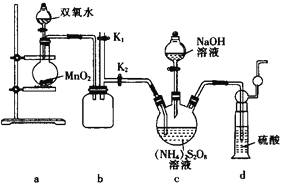
(3)欲控制通入O2的通入速率,采取的有效措施为____________________(答一条)
(4)装置a中反应产生的气体需要持续通入装置c的原因是____________________。
(5)上述装置中还需补充的实验仪器或装置有_______(填字母)。
A.温度计 B.洗气瓶 C.水浴装置 D.酒精灯
(实验二)测定用过硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50 mg·L-1。
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI![]() ,AgI呈黄色,且CN-优先与Ag+反应。实验如下:取100.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4 mol·L-1的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50 mL。
,AgI呈黄色,且CN-优先与Ag+反应。实验如下:取100.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4 mol·L-1的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50 mL。
(6)滴定终点的现象是________________________________________。
(7)处理后的废水中氰化钠的浓度为________mg·L-1。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将4molA和3molB充入体积为1L的密闭容器中,发生如下反应:aA(g)+2B(g)![]() 3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是工业上铝土矿(含有Al2O3和Fe2O3等)冶炼铝的工艺流程图:

(1)操作①的名称是:___________。操作①剩余的矿渣主要成分为:__________(填化学式)。
(2)图中①为了提高NaOH和铝土矿的反应速率可采取哪些措施__________________________(写两条)。
(3)图中①的离子方程式_____________________________________________________________;图中③、④的化学反应方程式______________________________________________________。
(4)洗涤Al(OH)3沉淀的具体操作是: ________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是

A. 正极电极反应式为:2H++2e—→H2↑
B. 此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C. 此过程中铜并不被腐蚀
D. 此过程中电子从Fe移向Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PVAc是一种具有热塑性的树脂,可合成重要高分子材料M,合成路线如下:
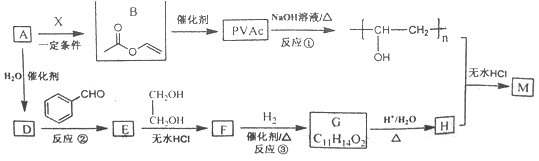
己知:R、R'、R"为H原子或烃基。
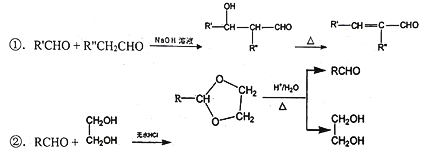
③羟基连在碳碳双键或碳碳三键上不稳定。
(1)已知标准状况下,3.36L气态烃A的质量是3.9g, A—B为加成反应,则X的结构简式为________;B中官能团的名称是_______。
(2)E能使溴的四氯化碳溶液褪色,反应②的反应试剂和条件是____,在E→F→G→H的转化过程中,乙二醇的作用是______。
(3)反应①的化学方程式为_______。
(4)己知M的链节中除苯环外,还含有六元环状结构,则M的结构简式为____________。
(5)E的同分异构体中含有苯环和甲基,且甲基不与苯环直接相连的同分异构体有_____种。
(6)以甲醇、本乙醛以及上述合成路线中的必要有机试剂为原料合成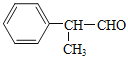 (其他无机试剂任选),请写出合成路线_______。
(其他无机试剂任选),请写出合成路线_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述不正确的是( )
A. 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
B. 反应①、过滤后所得沉淀为Fe2O3
C. 图中所示转化反应都不是氧化还原反应
D. 试剂X可以是氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的的是

A. 用甲装置比较碳、氮和硅三种元素的非金属性强弱
B. 用乙装置分离碘的四氯化碳溶液
C. 用丙装置制取干燥的氨气
D. 用丁装置吸收氨气,并防止倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法正确的是 ( )
A.标准状况下,2.24 L CHCl3含有的分子数为0.1NA
B.0.1 mol CnH2n+2中含有的碳碳单键数为0.1nNA
C.2.8 g乙烯和丙烯的混合气体中所含碳原子为0.2NA
D.1 mol苯乙烯中含有碳碳双键数为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com