
【题目】下列说法正确的是( )
A.氢气的燃烧热为△H=﹣285.5kJ?mol﹣1 , 则电解水的热化学方程式为2H2O(l) ![]() 2H2(g)+O2(g)△H=+285.5k?Jmol﹣1
2H2(g)+O2(g)△H=+285.5k?Jmol﹣1
B.反应SO2(g)+2H2S(g)═3S(s)+2H2O(l)在常温下能自发进行,则该反应的△H<0
C.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=﹣38.6k?Jmol﹣1
D.由C(石墨,s)=C(金刚石,s)△H=+1.90 k?Jmol﹣1可知,金刚石比石墨稳定
【答案】B
【解析】解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,所以水分解的热化学方程式:H2O(l)=H2(g)+ ![]() O2(g)△H=+285.5 kJmol﹣1 , 但是电解水的热化学方程式中,根据能量守恒,电能的介入会导致热能减少,吸收的热量变小,故A错误;
O2(g)△H=+285.5 kJmol﹣1 , 但是电解水的热化学方程式中,根据能量守恒,电能的介入会导致热能减少,吸收的热量变小,故A错误;
B.反应SO2(g)+2H2S(g)═3S(s)+2H2O(l)在常温下能自发进行,满足△H﹣T△S<0,反应△S<0,则该反应的△H<0,故B正确;
C.0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,因反应为可逆反应,则1molN2和3molH2置于密闭的容器中充分反应生成NH3(g),放热不是38.6kJ,则热化学反应方程式中的反应热数值错误,故C错误;
D.由C(石墨,s)=C(金刚石,s)△H=+1.90 kJmol﹣1可知,反应过程是吸热反应,金刚石能量高于石墨,则说明石墨比金刚石稳定,故D错误;
故选B.
【考点精析】利用反应热和焓变对题目进行判断即可得到答案,需要熟知在化学反应中放出或吸收的热量,通常叫反应热.


科目:高中化学 来源: 题型:
【题目】实验室用MnO2催化KClO3分解制取氧气,实验后要分离提纯回收其中的MnO2进行的操作为( )
A. 溶解、过滤、蒸发 B. 溶解、过滤、洗涤、干燥
C. 溶解、过滤、结晶 D. 溶解、结晶、干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钡(BaI22H2O)是一种白色粉末,常用于制取其他含碘化合物.一种制备流程如图1: 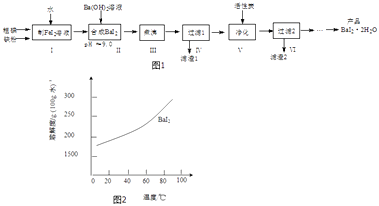
(1)步骤Ⅰ制FeI2溶液时,提高反应速率的可行措施有(填序号).
a.铁粉和碘粉用球磨机磨成细粉
b.增大n(铁粉):n(碘)的配料比
c.适当升高反应温度和搅拌速度
d.向反应器中加水至I2全部溶解
(2)步骤Ⅱ发生反应的化学方程式为;用pH试纸测定溶液pH的方法是
(3)步骤Ⅲ小心“煮沸”约20分钟,可使Fe(OH)2颗粒长大,其目的是;步骤V加入活性炭的目的是 .
(4)从过滤2所得滤液中获得BaI22H2O(溶解度曲线如图2所示)的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从含铜废料(如:覆铜板、印刷线路板及铅冰铜等)中提取铜,既可提高资源的利用率又可减少重金属污染.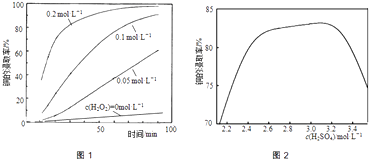
(1)废覆铜板(Cu和Sn组成)可用CuSO4和H2SO4混合溶液作电解质溶液,直接电解回收精铜,阳极上发生的电极反应为 .
(2)废印刷线路板中的铜常用含盐酸的FeCl3溶液或H2O2﹣HCl﹣NaCl混合溶液浸取回收.
①用FeCl3溶液浸取铜时发生反应的离子方程式为;若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀,产生红褐色沉淀的原因是 .
②将粉碎后的废印刷线路板放入三口烧瓶中,分别加入由0.3molL﹣1盐酸、0.5molL﹣1NaCl及不同浓度的H2O2组成的混合溶液,在温度、搅拌速率及固液比等均相同时,铜的浸取率随H2O2的浓度和时间的变化如图1所示.当c(H2O2)=0molL﹣1时,也有少量的铜被浸出,其原因是 .
③用H2O2﹣HCl﹣NaCl混合溶液浸取时,其浸取过程包括:
(Ⅰ) Cu+H2O2+2H+=Cu2++2H2O
(Ⅱ) Cu2++Cu2Cu+
(Ⅲ) Cu++nCl﹣CuCln(n﹣1)﹣
(Ⅳ) 2CuCln(n﹣1)﹣+2H++H2O2=2Cu2++2H2O+2nCl﹣
其他条件相同时,增大下列离子浓度可以加速Cu从废电路板中浸出的是(填序号).
a.Na+ b.Cu2+ c.Cl﹣d.OH﹣
(3)铅冰铜(PbS、Cu2S及FeS的混合物)可用HCl﹣H2O2混合溶液浸取.
①Cu2S被HCl﹣H2O2混合溶液浸取得到硫酸铜和氯化铜溶液的化学方程式为 .
②若由H2SO4代替HCl﹣H2O2中的HCl,其他条件相同,铜的浸取率随硫酸浓度的变化如图2所示.当H2SO4浓度大于3.1molL﹣1时,硫酸浓度越大,铜的浸取率反而越小,其原因可能是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸盐与钴(Ⅲ)形成的一种配合物1Co(NH3)5NO2]Cl2的制备流程如图: ![]()
(1)Co2+基态核外电子排布式为 .
(2)配合物1Co(NH3)5Cl]Cl2中与Co3+形成配位键的原子为(填元素符号);配离子 1Co(NH3)5NO2]2+的配体中氮原子的杂化轨道类型为 .
(3)与NO2﹣互为等电子体的单质分子为(写化学式).
(4)H2O2与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为 .
(5)亚硝酸盐在水体中可转化为强致癌物亚硝胺,亚硝胺NDMA的结构简式如图 ![]() 所示,1molNDMA分子中含有σ键的数目为mol.
所示,1molNDMA分子中含有σ键的数目为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的熔、沸点高低只与范德华力有关的是( )
A.Li、Na、K、PbB.HF、HCl、HBr、HI
C.LiCl、NaCl、KCl、RbClD.F2、Cl2、Br2、I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1和图2是A、B两种物质的核磁共振氢谱。已知A、B两种物质都是烃类,都含有6个氢原子。请根据图1和图2两种物质的核磁共振氢谱谱图选择出可能属于图1和图2的两种物质是
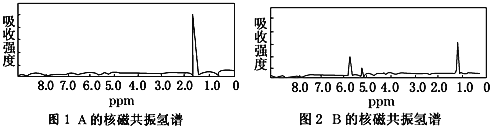
A. A是C3H6;B是C6H6 B. A是C2H6;B是C3H6
C. A是C2H6;B是C6H6 D. A是C3H6;B是C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种碳架如图的烃(小黑球表示碳原子,黑球之间的连线表示共价键),下列说法正确的是( )
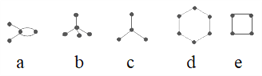
①a和e互为同分异构体 ②b是天然气的主要成分 ③d为平面型分子,属于芳香烃 ④b和c互为同系物 ⑤a、d、e的最简式相同
A. ①③⑤ B. ①②③ C. ②③④ D. ①④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com